如图所示,把试管放入盛有25 ℃饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5 mL稀盐酸,试完成下列问题。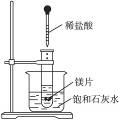
(1)实验中观察到的现象是__________________。
(2)产生上述现象的原因是__________________。
(3)写出有关反应的离子方程式__________________。
(4)由实验推知,MgCl2溶液和H2的总能量__________________(填“大于”“小于”或“等于”)镁片和盐酸的总能量。
如图所示,把试管放入盛有25 ℃饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5 mL稀盐酸,试完成下列问题。
(1)实验中观察到的现象是__________________。
(2)产生上述现象的原因是__________________。
(3)写出有关反应的离子方程式__________________。
(4)由实验推知,MgCl2溶液和H2的总能量__________________(填“大于”“小于”或“等于”)镁片和盐酸的总能量。