酚酞是常用的酸碱指示剂,结构简式为: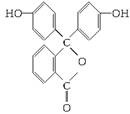
(1)酚酞的分子式为______________________________。
(2)酚酞属于_____________________、________________类衍生物。
(3)酚酞分别在1 mol·L-1 HCl和1 mol·L-1 NaOH溶液中溶解,在_____________中的溶解度大,原因是_________________________________________________________________。
酚酞是常用的酸碱指示剂,结构简式为:
(1)酚酞的分子式为______________________________。
(2)酚酞属于_____________________、________________类衍生物。
(3)酚酞分别在1 mol·L-1 HCl和1 mol·L-1 NaOH溶液中溶解,在_____________中的溶解度大,原因是_________________________________________________________________。