已知:A是硫酸盐,且A和G、C和D、F和H元素组成相同。G和KSCN溶液混合后溶液显血红色。反应过程中产生的水在图示中已略去。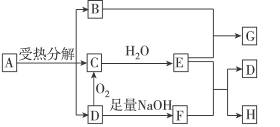
完成下列问题:
(1)写出G和H的化学式:G_____________,H_____________。
(2)工业生产中D转化为C的反应条件是:_____________。
(3)B跟E反应的离子方程式是_____________。
已知:A是硫酸盐,且A和G、C和D、F和H元素组成相同。G和KSCN溶液混合后溶液显血红色。反应过程中产生的水在图示中已略去。
完成下列问题:
(1)写出G和H的化学式:G_____________,H_____________。
(2)工业生产中D转化为C的反应条件是:_____________。
(3)B跟E反应的离子方程式是_____________。