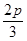在一个固定容积的密闭容器中,加入m mol A和n mol B,发生下列反应:
mA(g)+nB(g) pC(g)
pC(g)
平衡时C的浓度为w mol·L-1。若维持容器体积和温度不变,起始时放入a mol A、b mol B、c mol C,要使平衡时C的浓度仍为w mol·L-1,则a、b、c必须满足的关系是( )
A.a∶b∶c=m∶n∶p
B.a∶b=m∶n, +b=p
+b=p
C. +a=m,
+a=m,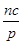 +b=n
+b=n
D.a=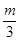 ,b=
,b=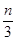 ,c=
,c=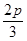
在一个固定容积的密闭容器中,加入m mol A和n mol B,发生下列反应:
mA(g)+nB(g) pC(g)
pC(g)
平衡时C的浓度为w mol·L-1。若维持容器体积和温度不变,起始时放入a mol A、b mol B、c mol C,要使平衡时C的浓度仍为w mol·L-1,则a、b、c必须满足的关系是( )
A.a∶b∶c=m∶n∶p
B.a∶b=m∶n, +b=p
+b=p
C. +a=m,
+a=m,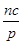 +b=n
+b=n
D.a=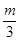 ,b=
,b=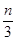 ,c=
,c=