有机物A的结构简式为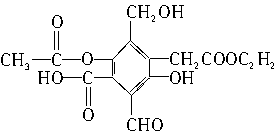
(1)A与过量NaOH完全反应时,A与参加反应的NaOH物质的量之比为____________。
(2)A与新制Cu(OH)2完全反应时,A与参加反应的Cu(OH)2物质的量之比为_________,其中A与被还原的Cu(OH)2的物质的量之比为__________。
(3)A与过量NaHCO3完全反应时,A与参加反应的NaHCO3物质的量之比为___________。
有机物A的结构简式为
(1)A与过量NaOH完全反应时,A与参加反应的NaOH物质的量之比为____________。
(2)A与新制Cu(OH)2完全反应时,A与参加反应的Cu(OH)2物质的量之比为_________,其中A与被还原的Cu(OH)2的物质的量之比为__________。
(3)A与过量NaHCO3完全反应时,A与参加反应的NaHCO3物质的量之比为___________。