(1)某温度下,纯水中的c(H+)=2.0×10—7mol/L,此时溶液的c(OH—)=mol/L;若温度不变,滴入稀盐酸使c(H+)=5.0×10—4mol/L,则溶液中c(OH—)=mol/L,由水电离产生的c(H+)=mol/L,此时温度25℃(填“高于”、“低于”或“等于”)。
(2)室温时,将pH=5的H2SO4稀释10倍,则c(H+)∶c(SO42—)=,将稀释后的溶液再稀释1000倍,则c(H+)∶ c(SO42—)=。
(3)有稀硫酸和稀盐酸的混合溶液20ml,向此溶液中滴加0.025mol/LBa(OH)2溶液时,生成沉淀的质量和溶液pH的变化情况如图所示,求:
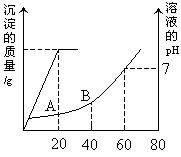
⑴原混合溶液中硫酸和盐酸的物质的量浓度?
⑵滴到A、B两点时溶液的pH 各是多少?