(4分)已知Ba(AlO2)2可溶于水。右图表示的是向KA1(SO4)2溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。完成下列问题:
(1)a点时反应的离子方程式是
(2)a、b两点消耗Ba(OH)2的物质的量之比是 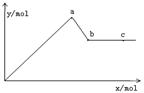
(4分)已知Ba(AlO2)2可溶于水。右图表示的是向KA1(SO4)2溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。完成下列问题:
(1)a点时反应的离子方程式是
(2)a、b两点消耗Ba(OH)2的物质的量之比是 