25℃时,若体积为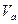 、pH=a的某一元强酸与体积为
、pH=a的某一元强酸与体积为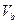 、pH=b的某一元强碱混合,恰好中和,且已知
、pH=b的某一元强碱混合,恰好中和,且已知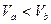 和a=0.5b,请填写下列空白:
和a=0.5b,请填写下列空白:
⑴a值可否等于3(填“可”或“否”)________,其理由是_______________________。
⑵a值可否等于5(填“可”或“否”)________,其理由是_____________________。
⑶试确定a的取值范围_________________________________。
25℃时,若体积为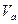 、pH=a的某一元强酸与体积为
、pH=a的某一元强酸与体积为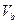 、pH=b的某一元强碱混合,恰好中和,且已知
、pH=b的某一元强碱混合,恰好中和,且已知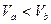 和a=0.5b,请填写下列空白:
和a=0.5b,请填写下列空白:
⑴a值可否等于3(填“可”或“否”)________,其理由是_______________________。
⑵a值可否等于5(填“可”或“否”)________,其理由是_____________________。
⑶试确定a的取值范围_________________________________。