苯环上原有的取代基对新取代导入苯环上的取代基的位置有一定的影响,其规律是:
(1)苯环上新导入的取代基所占的位置主要决定于原有取代基的性质。
(2)可以把原有取代基分成两类:第一类取代基主要使新导入的取代基进入苯环的邻位和对位,如—OH、—CH3(或烃基)、—Cl、—Br、—O—COR等,第二类取代基主要使新导入的取代基进入苯环的间位。例如—NO2、—SO3H、—CHO等。
请写出下图中②④⑤三步反应的化学方程式。
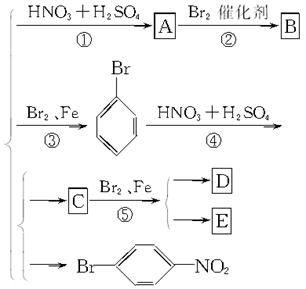
苯环上原有的取代基对新取代导入苯环上的取代基的位置有一定的影响,其规律是:
(1)苯环上新导入的取代基所占的位置主要决定于原有取代基的性质。
(2)可以把原有取代基分成两类:第一类取代基主要使新导入的取代基进入苯环的邻位和对位,如—OH、—CH3(或烃基)、—Cl、—Br、—O—COR等,第二类取代基主要使新导入的取代基进入苯环的间位。例如—NO2、—SO3H、—CHO等。
请写出下图中②④⑤三步反应的化学方程式。
