2,4,5-三氯苯酚和氯乙酸反应可制造除草剂2,4,5-三氯苯氧乙酸。某生产该除草剂的工厂曾在一次事故中泄漏出有毒的二NF749英,简称TCDD。有关物质的结构式如下: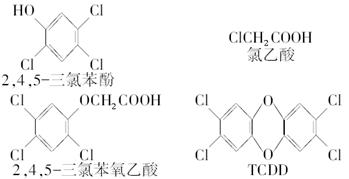
请写出:
(1)生成2,4,5-三氯苯氧乙酸的化学方程式: _________________________
(2)由2,4,5-三氯苯酚生成TCDD的化学方程式:_________________________
2,4,5-三氯苯酚和氯乙酸反应可制造除草剂2,4,5-三氯苯氧乙酸。某生产该除草剂的工厂曾在一次事故中泄漏出有毒的二NF749英,简称TCDD。有关物质的结构式如下:
请写出:
(1)生成2,4,5-三氯苯氧乙酸的化学方程式: _________________________
(2)由2,4,5-三氯苯酚生成TCDD的化学方程式:_________________________