通常情况下,多个羟基连在同一个碳原子上的分子结构是不稳定的,容易自动失水,生成碳氧双键的结构:
下面是9个化合物的转变关系: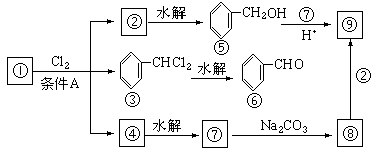
(1)化合物①是__________,它跟氯气发生反应的条件A是__________。
(2)化合物⑤跟⑦可在酸的催化下去水生成化合物⑨, ⑨的结构简式是:_______;名称是______________________________________。
(3)化合物⑨是重要的定香剂,香料工业上常用化合物⑧和②直接合成它。写出此反应的化学方程式。
通常情况下,多个羟基连在同一个碳原子上的分子结构是不稳定的,容易自动失水,生成碳氧双键的结构:
下面是9个化合物的转变关系:
(1)化合物①是__________,它跟氯气发生反应的条件A是__________。
(2)化合物⑤跟⑦可在酸的催化下去水生成化合物⑨, ⑨的结构简式是:_______;名称是______________________________________。
(3)化合物⑨是重要的定香剂,香料工业上常用化合物⑧和②直接合成它。写出此反应的化学方程式。