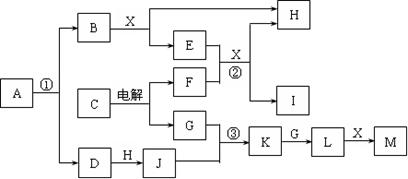
 下图所示各物质均由短周期元素组成,部分反应的产物略去。A的摩尔质量为65g/mol,B、F为金属单质,D、H、G为无色气态非金属单质,C、K、L和X都属于氧化物,E、J、M均为重要的化工产品。
下图所示各物质均由短周期元素组成,部分反应的产物略去。A的摩尔质量为65g/mol,B、F为金属单质,D、H、G为无色气态非金属单质,C、K、L和X都属于氧化物,E、J、M均为重要的化工产品。
回答下列问题:
⑴ X的电子式为 ▲ 。 ⑵反应②的离子方程式为 ▲ 。
⑶反应③的化学方程式为 ▲ 。 ⑷A的化学式为 ▲ 。
 下图所示各物质均由短周期元素组成,部分反应的产物略去。A的摩尔质量为65g/mol,B、F为金属单质,D、H、G为无色气态非金属单质,C、K、L和X都属于氧化物,E、J、M均为重要的化工产品。
下图所示各物质均由短周期元素组成,部分反应的产物略去。A的摩尔质量为65g/mol,B、F为金属单质,D、H、G为无色气态非金属单质,C、K、L和X都属于氧化物,E、J、M均为重要的化工产品。
回答下列问题:
⑴ X的电子式为 ▲ 。 ⑵反应②的离子方程式为 ▲ 。
⑶反应③的化学方程式为 ▲ 。 ⑷A的化学式为 ▲ 。