有机物A(分子式C6H10O3)是合成某种隐形眼镜材料的单体,A可发生如下变化:
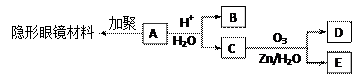 |
已知:Ⅰ.物质B是最简单的二元醇,可用作汽车发动机抗冻剂;物质D不能发生银镜反应,但能与NaHCO3溶液反应放出气体。
Ⅱ.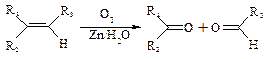
回答下列问题:
⑴隐形眼镜材料的结构简式为 ;
⑵写出物质B在铜催化下与O2反应的化学方程式 ;
⑶与C互为同分异构体,分子为链状的酯类物质共有 种;
⑷请设计合理方案,用物质D制取乙二酸(其他无机原料自选,用反应流程图表示,并注明必要的反应条件)。
例如:
有机物A(分子式C6H10O3)是合成某种隐形眼镜材料的单体,A可发生如下变化:
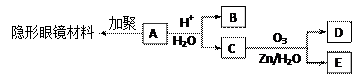 |
已知:Ⅰ.物质B是最简单的二元醇,可用作汽车发动机抗冻剂;物质D不能发生银镜反应,但能与NaHCO3溶液反应放出气体。
Ⅱ.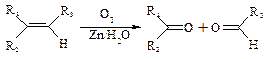
回答下列问题:
⑴隐形眼镜材料的结构简式为 ;
⑵写出物质B在铜催化下与O2反应的化学方程式 ;
⑶与C互为同分异构体,分子为链状的酯类物质共有 种;
⑷请设计合理方案,用物质D制取乙二酸(其他无机原料自选,用反应流程图表示,并注明必要的反应条件)。
例如: