工业生产粗硅的主要原理为:SiO2+2C 3273K Si(粗)+2CO↑。
(1)若在制粗硅的过程中同时生成了碳化硅,且生成的硅和碳化硅的物质的量之比为5∶1,则参加反应的C和SiO2的质量比为 。
(2)工业上可通过如下流程由粗硅制取纯硅:
|
|||||
|
|
||||


 Si(粗) SiCl4(l) Si(纯)
Si(粗) SiCl4(l) Si(纯)若上述反应中Si(粗)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产100.8t纯硅需纯度为75%的石英砂多少吨?
(3)工业上还可以通过下图所示的流程来制取纯硅:
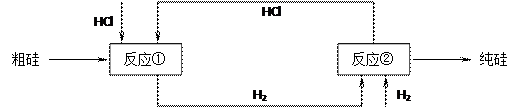
反应①: Si(粗)+3HCl(g) 553~573K SiHCl3(l)+H2(g)
反应②: SiHCl3+H2 1373K Si(纯)+3HCl
假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率为75%,反应②中H2的利用率为80%,则在下轮次的生产中,需补充投入HCl和H2的体积比为多少?
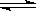 CH3OH(g)。
CH3OH(g)。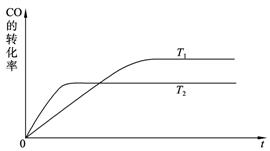
 的催化剂d. 充入He,使体系总压强增大
的催化剂d. 充入He,使体系总压强增大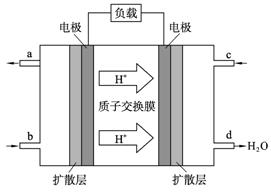
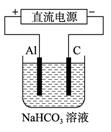
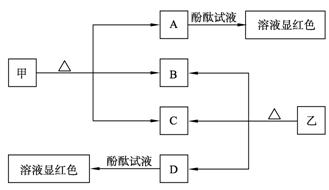
 ________。
________。 色,说明溶液均显性,其原理是否相同?请用必要的文字加以解释并写出离子方程式:
色,说明溶液均显性,其原理是否相同?请用必要的文字加以解释并写出离子方程式: 元素原子的最外层电子数是其次外层电子数的=3/4倍;C与E同主族。
元素原子的最外层电子数是其次外层电子数的=3/4倍;C与E同主族。
 ①能使溴水因发生化学反应而褪色
①能使溴水因发生化学反应而褪色 模型如右图所示(图中球与球之间的连线表示单键或双键)。
模型如右图所示(图中球与球之间的连线表示单键或双键)。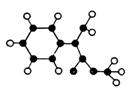
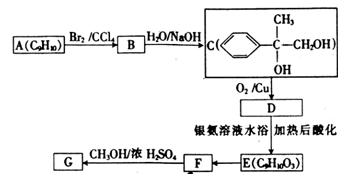
 E→F的反应类型是。
E→F的反应类型是。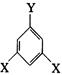 表示(其中X、Y均不为H),试写出符合上述通式且能发生银镜反应的其中两种物质的结构简式:
表示(其中X、Y均不为H),试写出符合上述通式且能发生银镜反应的其中两种物质的结构简式:

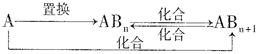
 粤公网安备 44130202000953号
粤公网安备 44130202000953号