在一定温度下,冰醋酸加水稀释过程中溶液的导电能力如下图所示,请回答: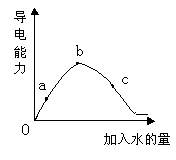
⑴“O”点导电能力为0的理由是: 。
⑵a、b、c三点溶液中,[H+]由小到大的顺序是: 。
⑶a、b、c三点溶液中,醋酸的电离程度最大的是: 。
⑷若使c点溶液中[CH3COO-]增大,而[H+]减小,可采取的措施主要有:① ;② ;③ ;④ 。
在一定温度下,冰醋酸加水稀释过程中溶液的导电能力如下图所示,请回答:
⑴“O”点导电能力为0的理由是: 。
⑵a、b、c三点溶液中,[H+]由小到大的顺序是: 。
⑶a、b、c三点溶液中,醋酸的电离程度最大的是: 。
⑷若使c点溶液中[CH3COO-]增大,而[H+]减小,可采取的措施主要有:① ;② ;③ ;④ 。