A、B、C是在中学化学中常见的3种化合物,它们各由两种元素组成,甲、乙是两种单质,这些化合物和单质之间存在如下的关系:
单质甲 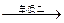 化合物A
化合物A 化合物B
化合物B  化合物B
化合物B
化合物A和化合物C 单质乙和化合物C
据此判断:
(1)在A、B、C这3种化合物中,必定含有乙元素的是 (用A、B、C字母填写)
(2)单质乙必定是 (填“金属”或“非金属”),其理由是 。
(3)单质乙的分子式可能是 ,则化合物B的分子式是
A、B、C是在中学化学中常见的3种化合物,它们各由两种元素组成,甲、乙是两种单质,这些化合物和单质之间存在如下的关系:
单质甲 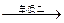 化合物A
化合物A 化合物B
化合物B  化合物B
化合物B
化合物A和化合物C 单质乙和化合物C
据此判断:
(1)在A、B、C这3种化合物中,必定含有乙元素的是 (用A、B、C字母填写)
(2)单质乙必定是 (填“金属”或“非金属”),其理由是 。
(3)单质乙的分子式可能是 ,则化合物B的分子式是