(1)某反应池中,发生“生物硝化过程”,如果不考虑过程中硝化细菌的增殖,其净反应如下式所示: ①
①
配平上面化学方程式,将系数填入方框中。
②将铵态氮中的1 mg氮转化成硝酸根中的氮,需氧气多少毫克?
③为什么在反应中需要不断添加碱?
(2)3级反应池中发生的“生物反硝化过程”,通常需要外加甲醇,净反应如下所示: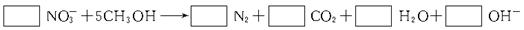
配平上面化学方程式,将系数填入方框中。
(1)某反应池中,发生“生物硝化过程”,如果不考虑过程中硝化细菌的增殖,其净反应如下式所示: ①
①
配平上面化学方程式,将系数填入方框中。
②将铵态氮中的1 mg氮转化成硝酸根中的氮,需氧气多少毫克?
③为什么在反应中需要不断添加碱?
(2)3级反应池中发生的“生物反硝化过程”,通常需要外加甲醇,净反应如下所示: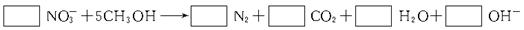
配平上面化学方程式,将系数填入方框中。