 化合物是一种香料,存在于金橘中,可用如下路线合成:
化合物是一种香料,存在于金橘中,可用如下路线合成:



已知:
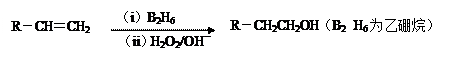

 回答下列问题:
回答下列问题:
 (1)11.2(标准状况)的烃在氧气中充分燃烧可以产生88 和45 。
(1)11.2(标准状况)的烃在氧气中充分燃烧可以产生88 和45 。
 的分子式是
的分子式是
 (2)和均为一氯代烃,它们的名称(系统命名)分别为;
(2)和均为一氯代烃,它们的名称(系统命名)分别为;
 (3)在催化剂存在下1 与2 反应,生成3-苯基-1-丙醇。F的结构简式是
(3)在催化剂存在下1 与2 反应,生成3-苯基-1-丙醇。F的结构简式是
 (4)反应①的反应类型是;
(4)反应①的反应类型是;
 (5)反应②的化学方程式为
(5)反应②的化学方程式为
 (6)写出所有与具有相同官能团的的芳香类同分异构体的结构简式:
(6)写出所有与具有相同官能团的的芳香类同分异构体的结构简式:

 化合物是一种香料,存在于金橘中,可用如下路线合成:
化合物是一种香料,存在于金橘中,可用如下路线合成:



已知:
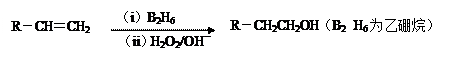

 回答下列问题:
回答下列问题:
 (1)11.2(标准状况)的烃在氧气中充分燃烧可以产生88 和45 。
(1)11.2(标准状况)的烃在氧气中充分燃烧可以产生88 和45 。
 的分子式是
的分子式是
 (2)和均为一氯代烃,它们的名称(系统命名)分别为;
(2)和均为一氯代烃,它们的名称(系统命名)分别为;
 (3)在催化剂存在下1 与2 反应,生成3-苯基-1-丙醇。F的结构简式是
(3)在催化剂存在下1 与2 反应,生成3-苯基-1-丙醇。F的结构简式是
 (4)反应①的反应类型是;
(4)反应①的反应类型是;
 (5)反应②的化学方程式为
(5)反应②的化学方程式为
 (6)写出所有与具有相同官能团的的芳香类同分异构体的结构简式:
(6)写出所有与具有相同官能团的的芳香类同分异构体的结构简式:
