吉林省长春市新高三起点调研考试化学试卷
下列化学用语正确的是
| A.重水的分子式H218O | B.Mg2+的结构示意图 |
| C.乙酸的结构式CH3COOH | D.次氯酸的电子式 |
下列变化不属于取代反应的是
A.CH3COOC2H5+H2O CH3COOH+C2H5OH CH3COOH+C2H5OH |
B.CH3=CH2+H2 CH3CH3 CH3CH3 |
C. +HNO3 +HNO3  +H2O +H2O |
D.CH4+Cl2 CH3Cl+HCl CH3Cl+HCl |
下列说法正确的是
| A.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| B.能自发进行的化学反应,一定是△H<0、△S>0 |
| C.焰色反应是物质燃烧时火焰呈现的颜色变化,属于化学变化 |
| D.钢铁发生电化学腐蚀时,负极的电极反应式为 Fe–3e- = Fe3+ |
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.常温常压下,46 g NO2与N2O4的混合气体中含有的分子总数为NA |
| B.0.1 mol乙烯和乙醇的混合物完全燃烧所消耗O2的分子数为0.3 NA |
| C.25℃时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.1 NA |
| D.一定量的钠与8 g氧气作用,若两者均无剩余,转移的电子数为NA |
用下列装置进行实验,设计正确且能达到实验目的的是
| A.用图1所示装置制取少量H2 |
| B.用图2所示装置分离Na2CO3溶液和CH3COOC2H5的混合物 |
| C.用图3所示装置验证Na和水反应为放热反应 |
| D.用图4所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
有机物A的产量是衡量一个国家石油工业发展水平的标志,可发生以下系列转化, B、D是生活中常见的两种有机物,下列说法不正确的是 
A.A的结构简式为CH2=CH2
B.1molB物质可以与足量Na反应生成0.5molH2
C.B、D、E三种物质可以用饱和Na2CO3溶液鉴别
D.由B、D制备E浓H2SO4只作吸水剂
25℃时,下列各组离子在指定溶液中能大量共存的是
| A.滴入甲基橙显红色的溶液中:NH4+、Ba2+、AlO2-、Cl- |
| B.PH=13的溶液:Na+、K+、SiO32-、HCO3- |
| C.含较多的SO32-的溶液:H+、Ca2+、Fe3+、NO3- |
| D.澄清透明溶液中:K+、MnO4-、H2O、SO42- |
某反应的反应过程中能量变化如下图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是
| A.该反应为放热反应 | B.催化剂能改变反应的焓变 |
| C.催化剂能降低反应的活化能 | D.逆反应的活化能大于正反应的活化能 |
根据下图的转化关系判断下列说法正确的是(反应条件已略去)
| A.反应①②③④⑤均属于氧化还原反应和离子反应 |
| B.反应⑤说明该条件下铝可用于制熔点较高的金属 |
| C.相同条件下生成等量的O2,反应③和④转移的电子数之比为1∶1 |
| D.反应①中氧化剂与还原剂的物质的量之比为1∶4 |
如图是立方烷的球棍模型,下列有关说法不正确的是
| A.其一氯代物只有一种 |
| B.其二氯代物有三种同分异构体 |
| C.它的分子式不符合CnH2n+2,所以它不是饱和烃 |
| D.它与苯乙烯(C6H5—CH=CH2)互为同分异构体 |
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下图转化关系。下列有关物质的推断正确的是
| A.若甲为N2,则丁可能是O2 | B.若甲为Fe,则丁可能是Cl2 |
| C.若甲为AlCl3,则丁可能是NH3 | D.若甲为NaHCO3,则丁可能是HCl |
下列表示对应化学反应的离子方程式正确的是
| A.NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH- =BaSO4↓+2H2O |
| B.向FeCl2溶液中通入氯气:Fe2+ + Cl2 = Fe3+ + 2Cl- |
| C.向Ca(ClO)2溶液中通入过量的SO2:C1O- + SO2 + H2O="HClO" + HSO3- |
| D.FeSO4酸性溶液中加H2O2:2Fe2++H2O2=2Fe3++2OH- |
在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应:X(g)+Y(g)2Z(g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
| t/min |
2 |
4 |
7 |
9 |
| n(Y)/mol |
0.12 |
0.11 |
0.10 |
0.10 |
下列说法正确的是
A.反应前2 min的平均速率ν(Z)=2.0×10-3 mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)
C.保持其他条件不变,起始时向容器中充入0.32 mol气体X和0.32 mol 气体Y,到达平衡时,n(Z)<0.24 mol
D.其他条件不变,向平衡体系中再充入0.16 mol气体X,与原平衡相比,达到新平衡时,气体Y的转化率增大,X的体积分数增大
常温下,下列各溶液的叙述中正确的是
| A.NaHSO3与Na2SO3混合溶液中:3c(Na+)=c(HSO3-)+c(SO32-) |
| B.0.1 mol/L的醋酸钠溶液20 mL与0.1 mol/L盐酸10 mL混合后溶液显酸性: c(CH3COO-)>c(CH3COOH) >c(Cl-)>c(H+) |
| C.等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| D.向1.00 L 0.3 mol/LNaOH溶液中缓慢通入0.2 mol CO2气体,溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
A、B、C、D、E均是短周期元素,其原子序数依次增大,A和B同周期,A和D同族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与 B 的单质在不同条件下反应,可生成C2B或C2B2,E是所在周期中原子半径最小的元素,请回答。
(1)D在元素周期表中的位置是 。
(2)C2B的电子式是 ;AB2的结构式是 。
(3)B、C、E离子半径的由大到小的顺序为 ;(用离子符号回答)A、D、E最高价氧化物对应水化物的酸性由强到弱的顺序为 。(用化学式回答)
(4)A、B气态氢化物沸点高的是 ;(用化学式回答)原因 。
(5)水中锰含量超标,容易使洁具和衣物染色,使水产生异味,EB2可以用来出去水中超标的Mn2+,生成黑色沉淀,当消耗13.50 g EB2时,共转移了1 mol电子,则反应的离子方程式为 。
Ⅰ、某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验,实验装置如图所示: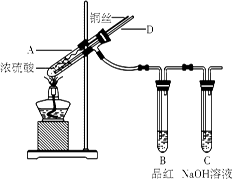
实验步骤:①先连接好装置,检验气密性,加入试剂;②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面。
(1)装置A中发生反应的化学方程式为 。
(2)拆除装置前,不需打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是 。
(3)若将B中品红溶液换成溴水,通入一段时间后溴水褪色,这说明了二氧化硫具有漂白性,你是否同意这个观点 ,(填“同意”或“不同意”),说明理由 (用离子方程式表示)。
Ⅱ、以浓硫酸、浓硝酸、粗铜、水和空气为原料可制得硫酸铜晶体。其过程如下图所示。
回答下列问题:
(4)配平在滤液(Ⅲ)中发生反应的化学方程式:
NOx+ H2O+ O2= HNO3
(5)写出制取硫酸铜的总反应方程式: 。
(6)在上述生产过程中,被循环使用的物质是 。
(1)25℃时,0.1 mol/L的HA溶液中c(H+)/c(OH-)=1010。请回答下列问题:
①HA是 (填“强电解质”或“弱电解质”)。
②在加水稀释HA溶液的过程中,随着水量的增加而增大的是 (填字母)。
A.c(H+)/c(HA) B.c(HA)/(A-) C.c(H+)与c(OH-)的乘积 D.c(OH-)
(2)已知:①CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2kJ·mol-1
②CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=-247.4 kJ·mol-1
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为 。
(3)下图是利用甲烷燃料电池电解50 mL 2 mol/L的氯化铜溶液的装置示意图:
请回答:
① 甲烷燃料电池的负极反应式为 。
② 当线路中有0.6mol电子通过时,B中阳极产物的质量为 g。
(1)将一定量纯净的氨基甲酸铵置于密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:H2NCOONH4(s)2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
| 温度(℃) |
15.0 |
20.0 |
25.0 |
30.0 |
35.0 |
| 平衡气体总浓度(×10-3 mol/L) |
2.4 |
3.4 |
4.8 |
6.8 |
9.4 |
氨基甲酸铵分解反应的焓变ΔH 0(填“>”、“<”或“=”)。
可以判断该分解反应已经达到化学平衡的是 。(填字母)
A.2v(NH3)=v(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
根据表中数据,计算25.0℃时的分解平衡常数为 。
(2)25℃时,NH3·H2O电离常数Kb=1.8×10-5,Mg(OH)2的溶度积常数Ksp=1.8×10-11,计算0.5 mol/L氨水的pH约为 。(已知lg3≈0.5)在某氯化镁溶液中加入一定量的某浓度的氨水后,测得混合液PH=11,则此温度下残留在溶液中的c(Mg2+)= 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号