全国普通高等学校招生统一考试理科综合能力测试化学
下列说法不正确的是()
| A. | 光催化还原水制氢比电解水制氢更节能环保、更经济 |
| B. | 氨氮废水(含 及 )可用化学氧化法或电化学氧化法处理 |
| C. | 某种光学检测技术具有极高的灵敏度,可检测到单个细胞( )内的数个目标分子,据此可推算该检测技术能测量到细胞内浓度约为 ~ 的目标分子 |
| D. | 向汽油中添加甲醇后,该混合燃料的热值不变 |
下列说法正确的是()
| A. | 金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理 |
| B. | 用pH计、电导率仪(一种测量溶液导电能力的仪器)均可检测乙酸乙酯的水解程度 |
| C. | 邻苯二甲酸氢钾可用于标定NaOH溶液的浓度,假如称量邻苯二甲酸氢钾时电子天平读数比实际质量偏大,则测得的NaOH溶液浓度比实际浓度偏小 |
| D. | 向某溶液中加入茚三酮试剂,加热煮沸后溶液若出现蓝色,则可判断该溶液含有蛋白质 |
如表所示的五种元素中,、、、为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法正确的是
、、三种元素最低价氢化物的沸点依次升高
由、和氢三种元素形成的化合物中只有共价键
物质、、均有熔点高、硬度大的特性
元素的单质具有半导体的特性,与元素可形成化合物
下列说法正确的是
 )仅能发生水解、氧化、消去反应
)仅能发生水解、氧化、消去反应
 )不是同系物,它们与氢气充分反应后的产物也不是同系物
)不是同系物,它们与氢气充分反应后的产物也不是同系物
镍氢电池()目前已经成为混合动力汽车的一种主要电池类型。中的表示储氢金属或合金。该电池在充电过程中的总反应方程式是:
已知:
下列说法正确的是
电池放电过程中,正极的电极反应式为:
充电过程中离子从阳极向阴极迁移
充电过程中阴极的电极反应式,中的被还原
电池中可以用溶液、氨水等作为电解质溶液
氯在饮用水处理中常用作杀菌剂,且的杀菌能力比强。25℃时氯气-氯水体系中存在以下平衡关系:


 =?
=?
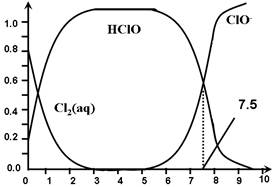
其中、和分别在三者中所占分数()随pH变化的关系如图所示。下列表述正确的是

雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有如下可溶性无机离子:、、、、、、 。某同学收集了该地区的雾霾,经必要的预处理后试样溶液,设计并完成了如下的实验:

已知:
根据以上的实验操作与现象,该同学得出的结论不正确的是( )
| A. |
试样中肯定存在、、和 |
| B. |
试样中一定不含 |
| C. |
试样中可能存在、 |
| D. |
该雾霾中可能存在、和 |
分某研究小组为了探究一种无机矿物质X(仅含四种元素)的组成和性质,设计并完成如下实验:

另取10.80在惰性气流中
(1)画出白色沉淀1中金属元素的原子结构示意图,写出气体甲的电子式。
(2)的化学式是,在惰性气流中加热至完全分解的化学反应方程式为。
(3)白色沉淀2在空气中变成红褐色沉淀的原因是(用化学反应方程式表示)。
(4)一定条件下,气体甲鱼固体1中的某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式,并设计实验方案验证该反应的产物。
煤炭燃烧过程中会释放出大量的,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以的形式固定,从而降低的排放。但是煤炭燃烧过程中产生的又会与发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
 (反应Ⅰ)
(反应Ⅰ)
 (反应Ⅱ)
(反应Ⅱ)
请回答下列问题:
(1)反应Ⅰ能自发进行的条件是
(2)对于气体参与的反应,表示平衡常数时用气体组分()的平衡压强代替该气体物质的量浓度,则反应Ⅱ的=
(3)假设某温度下,反应Ⅰ的速率()大于反应Ⅱ的速率(),则下列反应过程能量变化示意图正确的是

(4)通过监测反应体系中气体浓度的变化判断反应Ⅰ和Ⅱ是否同时发生,理由是
(5)图1为实验测得不同温度下反应体系中初始体积百分数与平衡时固体产物中质量百分数的关系曲线。则降低该反应体系中生成量的措施有
A.向该反应体系中投入石灰石
B.在合适的温度区间内控制较低的反应温度
C.提高的初始体积百分数
D.提高反应体系的温度
(6)恒温恒容条件下,假设反应Ⅰ和Ⅱ同时发生,,请在图2中画出反应体系中随时间变化的总趋势图。


葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:
6126(葡萄糖)+2+2→6127(葡萄糖酸)+2
26127(葡萄糖酸)+3→(6117)2(葡萄糖酸钙)+2+2
相关物质的溶解性见下表:
| 物质名称 |
葡萄糖酸钙 |
葡萄糖酸 |
溴化钙 |
氯化钙 |
| 水中的溶解性 |
可溶于冷水 易溶于热水 |
可溶 |
易溶 |
易溶 |
| 乙醇中的溶解性 |
微溶 |
微溶 |
可溶 |
可溶 |
实验流程如下:

请回答下列问题:
(1)第①步中溴水氧化葡萄糖时,下列装置最合适的是________。

制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其它试剂,下列物质中最适合的是________。
A.新制()2悬浊液 B.酸性4溶液
C.2/葡萄糖氧化酶 D.[(3)2]溶液
(2)第②步充分反应后3固体需有剩余,其目的是________;本实验中不宜用2替代3,理由是________。
(3)第③步需趁热过滤,其原因是________。
(4)第④步加入乙醇的作用是________。
(5)第⑥步中,下列洗涤剂最合适的是________。
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液
某兴趣小组以苯和乙烯为主要原料,采用以下路线合成药物普鲁卡因:

已知:

(1)对于普鲁卡因,下列说法正确的是
(2)写出化合物的结构简式
(3)写出反应所需的试剂
(4)写出的化学反应方程式
(5)写出同时符合下列条件的的所有同分异构体的结构简式
①分子中含有羧基
②谱显示分子中含有苯环,且苯环上有两种不同化学环境的氢原子
(6)通常采用乙烯为原料制得环氧乙烷后与反应合成,请用化学反应方程式表示以乙烯为原料制备的合成路线(无机试剂任选)
 粤公网安备 44130202000953号
粤公网安备 44130202000953号