上海市宝山区、嘉定区中考二模化学试卷
在炼钢中会发生如下反应:2FeO +Si 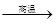 2Fe + SiO2,该反应中作还原剂的是
2Fe + SiO2,该反应中作还原剂的是
| A.FeO | B.Si | C.Fe | D.SiO2 |
用分子、原子的相关知识解释中正确的是
| A.金刚石和石墨的物理性质不同,是因为构成物质的原子不同 |
| B.水结成冰,体积发生变化,说明水分子的大小发生了变化 |
| C.氧气需加压后贮存钢瓶中,说明氧分子间有间隙 |
| D.双氧水分解能生成氧气,说明双氧水分子中含有氧分子 |
硝酸银在光照的条件下就会发生分解反应:2AgNO 3 2 Ag +O2 ↑+2X↑ ,则X的化学式是
2 Ag +O2 ↑+2X↑ ,则X的化学式是
| A.NO2 | B.N2O3 | C.N2O | D.N2 |
有关实验现象的描述正确的是
| A.镁带在空气中燃烧发出耀眼的白光 |
| B.硫在氧气中燃烧生成有刺激性气味二氧化硫 |
| C.红磷在氧气中燃烧产生大量的白雾 |
| D.木炭在氧气中燃烧生成黑色固体 |
化学方程式书写正确的是
A.CO+ CuO Cu + CO2↑ Cu + CO2↑ |
| B.Ca(OH)2+CO2→CaCO3↓+H2O |
C.2H2O  H2↑+O2↑ H2↑+O2↑ |
| D.Na2CO3+H2SO4 →NaSO4+H2O+CO2↑ |
物质的用途与性质对应正确的是
| A.稀有气体制霓虹灯——稀有气体化学性质稳定 |
| B.盐酸用于除铁锈——盐酸能与碱性氧化物反应 |
| C.一氧化碳可用于冶炼金属——一氧化碳有可燃性 |
| D.熟石灰用来改良酸性土壤——熟石灰微溶于水 |
工业上常将固体燃料粉碎或把液体燃料喷成雾状再燃烧,其目的是
| A.增加空气中氧气的体积分数 | B.降低可燃物的着火点 |
| C.延迟燃料燃烧的时间 | D.增加燃料与氧气的接触面积 |
在一定的条件下,与氢氧化钠溶液、碳酸钾溶液、氧化铜、锌和氯化钡溶液五种物质均能发生反应的是
| A.稀盐酸 | B.硫酸铜溶液 | C.稀硫酸 | D.二氧化碳 |
下列说法正确的是
| A.1摩尔氧中约含有6.02×l023个O2 |
| B.1摩尔CO2含有2个氧原子 |
| C.1摩尔CO2的质量为44克/摩尔 |
| D.1摩尔任何物质都约含6.02×l023个微粒 |
碳、一氧化碳和氢气分别跟灼热氧化铜反应,下列说法正确的是
| A.上述反应都属于置换反应 |
| B.反应中铜元素在固体中质量分数逐渐增大 |
| C.都可采用相同的实验装置 |
| D.反应后产物中的氧都来自于氧化铜中的氧 |
下列除杂方案中(括号中物质是除去杂质所用试剂和方法),正确的是
| A.N2中混有O 2(通过红热的木炭) |
| B.烧碱中混有纯碱(加适量稀盐酸、蒸发) |
| C.HCl溶液中混有H2SO4(加适量的硝酸钡溶液并过滤) |
| D.CaO中混有CaCO3(高温煅烧) |
下图是某反应过程在同一容器中反应前后物质种类的微观示意图。下列说法正确的是
| A.甲、丁都是氧化物 | B.该反应是置换反应 |
| C.该反应是复分解反应 | D.该反应中甲、乙的物质的量之比为1:1 |
下列各组溶液不另加试剂就能鉴别的是
| A.NaOH、CuSO4、Ca(OH)2、KNO3 |
| B.Na2CO3、HCl、BaCl2、AgNO3 |
| C.HCl、KOH、H2SO4、MgCl2 |
| D.NaCl、Fe2(SO4)3、KCl、Ba(OH)2 |
不能正确反映对应变化的图像是
| A.向一定量的氢氧化钠溶液中滴加一定量稀盐酸 |
| B.一定量的石灰石和与足量的稀盐酸反应 |
| C.向一定量盐酸和硫酸钠的混合溶液中,滴加氢氧化钡溶液 |
| D.等质量的镁和铁分别与足量的10%硫酸溶液反应 |
生活中处处有化学,通过学习已经知道:
①空气中体积分数为78%的气体的化学式是 。
②活性炭用于去除冰箱中异味,是利用活性炭的 性。
③在炒菜时,若将食盐或食盐水溅到煤气的火焰上,火焰就呈 色。
④农业上尿素是一种常用的氮肥,化学式是CO(NH2)2。它由 种元素组成,尿素的摩尔质量为 。
下图是我们研究常见物质组成、性质的几个实验: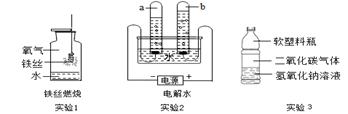
①实验1:写出该反应的化学方程式 。
②实验2:该实验证明水是由 组成的化合物。
③CO2与NaOH溶液反应无明显现象,为证明其反应,设计实验3。可观察到的实验现象是塑料瓶变瘪了,其原理是利用 。有同学却对此提出质疑,他认为上述实验不严谨,其理由是 ,要得到科学严谨的结论,仍利用该装置,补做的对比实验是将氢氧化钠溶液换成 ,与加入氢氧化钠溶液的实验现象进行对比。
若用检验生成物的方法证明二氧化碳与氢氧化钠发生反应,所用的试剂是 。
下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
| 温度/℃ |
0 |
20 |
40 |
80 |
100 |
|
| 溶解度/ g/100g水 |
Ca(OH)2 |
0.173 |
0.165 |
0.121 |
0.094 |
0.076 |
| NaOH |
31 |
91 |
111 |
313 |
336 |
①从上表数据可以看出,氢氧化钙的溶解度随温度的升高而 。
②40℃时,将20g水配成氢氧化钠饱和溶液,需氢氧化钠的质量为 克。若将40℃时422克的氢氧化钠饱和溶液稀释为20%的溶液,需加水⒁克。
③80℃时含有Ca(OH)2和NaOH两种溶质的饱和溶液,若要从中得到较纯净的NaOH晶体,应采取的物理方法是 。
④现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液), 此时甲乙两杯溶液中 。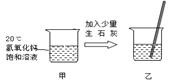
A.甲的溶质的质量分数与乙的相同
B.甲的溶质的质量分数大于乙的
C.甲的溶质的质量小于乙的
D.甲、乙都是饱和溶液
某小组在探究铁、铜、镁、银的金属活动性顺序时,做了如下三个实验(所用金属的形状与大小和稀盐酸的用量均相同):
①通过实验Ⅰ和Ⅱ可比较出镁和铁的金属活动性强弱。你认为他们依据的实验现象是 。写出实验Ⅰ中反应的化学方程式: 。
②通过观察到实验Ⅲ的现象可得出的结论是 。
③上述三个实验不能够得出四种金属的活动性顺序。探究小组在上述实验的基础上,补充了一个实验(如图所示),实现了探究目的。他们的实验:金属X、Y溶液分别是 。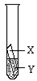
某实验室用30克氯酸钾和5克二氧化锰的混合物加热制取氧气,反应一段时间后,冷却称量,得到25.4g剩余固体物质。试计算:
①生成氧气的物质的量为 摩尔。
②参加反应的氯酸钾的物质的量为 摩尔。(根据化学方程式列式计算)
下图是实验室制取气体、探究物质组成的常用装置。
请回答下列问题:
Ⅰ.仪器①的名称是 ,仪器②的名称是 。
Ⅱ.在A装置中加入双氧水溶液和二氧化锰制取氧气,该反应的化学方程式为 。
Ⅲ.为了验证某混合气体是由H2、CO和H2O(气体)组成,设计上述实验,实验中B装置的作用是 ;证明有一氧化碳存在的实验现象是 ;会导致 。
Ⅳ.下列装置中能制取二氧化碳,并能控制反应的发生与停止,但与启普发生器原理不相同的装置是 。
氯化钠和氯化镁是重要的化工原料。某粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4等物质,为了从中提取较纯的氯化镁和氯化钠,设计以下实验方案: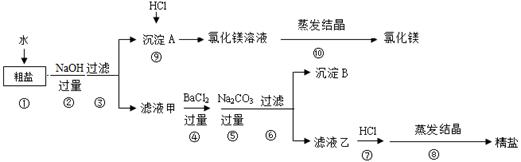
请回答下列问题:
Ⅰ.步骤①溶解过程中用玻璃棒搅拌的目的是 。
Ⅱ.步骤④⑤的顺序颠倒会引发的后果是 。
Ⅲ.滤液乙中所含的溶质除氯化钠外还含有 ;沉淀B中除含碳酸钙、碳酸钡外还含有 ;在步骤⑦中若加入的盐酸略过量是否对实验结果有影响?原因是 。
Ⅳ.写出步骤⑨中反应的化学方程式 。
Ⅴ.实验最终所得的精盐的质量大于粗盐中氯化钠的质量,整个过程中产生新的NaCl的反应共有 个。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号