[上海]2014届上海市浦东区中考一模(即期末)化学试卷
物质俗名与化学式均正确的是
| A.食盐 HCl | B.干冰CO | C.胆矾CuSO4·5H2O | D.熟石灰CaO |
物质在氧气中燃烧的实验现象,描述正确的是
| A.氢气:产生白烟 | B.铁丝:生成四氧化三铁 |
| C.镁带:黄色火光 | D.硫粉:明亮的蓝紫色火焰 |
对性质和用途的关系分析错误的是
| |
性质 |
用途 |
| A |
石墨软又滑 |
做电极 |
| B |
稀有气体稳定 |
作保护气 |
| C |
氢气有可燃性 |
作火箭燃料 |
| D |
活性炭有吸附性 |
用于防雾霾口罩 |
可减少PM2.5的行为是
| A.尽量开私家车出行 | B.过年燃放烟花爆竹 |
| C.使用太阳能热水器 | D.燃烧秸秆节约能源 |
CO2可转化为金刚石:4Na+3CO2 2Na2CO3+C,反应中的还原剂为
2Na2CO3+C,反应中的还原剂为
| A.Na | B.CO2 | C.Na2CO3 | D.C |
正确的化学方程式为
A.2CuO + C  2 Cu + CO2 2 Cu + CO2 |
B.2H2O2  2H2O + O2↑ 2H2O + O2↑ |
C.2KClO3 2KCl + 3O2 ↑ 2KCl + 3O2 ↑ |
D.3CO+ Fe2O3  2Fe + 3CO2↑ 2Fe + 3CO2↑ |
从下图获取的信息中错误的是
| A.空气是一种混合物 | B.该过程为物理变化 |
| C.氮气沸点比氧气高 | D.氧气由氧分子构成 |
潜水艇中可用过氧化钠制取氧气:2Na2O2+2CO2=2Na2CO3+O2,正确的说法是
| A.1mol Na2O2的质量为78g |
| B.1mol Na2O2含有1mol氧分子 |
| C.0.5mol Na2O2含有6.02×1023个原子 |
| D.反应前后氧元素的存在形态未发生改变 |
某同学用足量氯酸钾与二氧化锰的混合物制取氧气,快速收集一瓶氧气后发现产生气体速率明显下降(实验情况如右图),接下来他应该
| A.将酒精灯位置升高 | B.将酒精灯向右微移 |
| C.再向试管中加入氯酸钾 | D.再向试管中加入二氧化锰 |

能正确表示对应变化关系的是
| A.氢气还原氧化铜 |
| B.t℃时,CO2和O2的溶解度与压强的关系 |
| C.氧气是否充足对碳燃烧放出热量的影响 |
| D.向烧杯a(有MnO2)、b(无MnO2)中分别加入50g5%的双氧水 |
密闭容器中有甲~丁四种物质,右图为反应前后各物质的质量分数,说法错误的是
| A.丙是化合物 |
| B.该反应是化合反应 |
| C.参加反应的甲、乙质量比是21:4 |
| D.反应前甲和乙的质量之和大于生成丙的质量 |
化学与生活息息相关。
(1)空气中供人呼吸的气体是 (填化学式,下同),促进光合作用的气体是 。
(2)会引起酸雨的气体是 。
(3)我国新版饮用水标准中要求使用消毒剂一氯胺(NH2Cl)。NH2Cl由 种元素组成,其中氮、氢元素质量比是 ;NH2Cl用于消毒时发生反应:NH2Cl+X NH3+HClO,其中X的化学式为 。
NH3+HClO,其中X的化学式为 。
下图是甲 、乙两种固体(不含结晶水)在不同温度下的溶解度(单位:g/100g水)
| 温度(℃) |
0 |
20 |
40 |
60 |
80 |
90 |
100 |
| 甲 |
13.3 |
32 |
64 |
110 |
169 |
202 |
246 |
| 乙 |
35.7 |
36 |
36.6 |
37.3 |
38.4 |
39 |
39.8 |
(1)60℃时甲的溶解度为 g/100g水,将60g甲放入50g水中充分溶解得到溶液 g。
(2)从乙的溶液中提取乙的方法是 (填“降温结晶”或“蒸发结晶”)。
(3)分别将100g甲、乙的饱和溶液从60℃降温至20℃,对所得溶液的叙述正确的是 。
A.甲、乙均为饱和溶液 B.溶液质量:甲>乙
C.所含溶剂质量:甲<乙 D.溶质质量分数:甲>乙
水是弥足珍贵的资源。
(1)除去水中难溶性杂质的操作是 ,其中玻璃棒的作用是 ;
(2)水能与多种物质发生化学反应,试举一例(写出化学方程式) ;
(3)下图中甲是淡化海水的模拟装置,乙是电解水的装置。
Ⅰ.甲中水的状态变化为:液态 气态
气态 液态,这个过程中水分子的 发生了改变。冷凝器中用水作冷却剂是利用其
液态,这个过程中水分子的 发生了改变。冷凝器中用水作冷却剂是利用其
a.水分子的缔合性 b.比热容大 c.分散性
Ⅱ.乙中试管“2”内气体的检验方法是 ,水分解过程中的最小微粒是 (填字母)( 可表示一个水分子)
可表示一个水分子)
Ⅲ.“嫦娥三号”探月使用的液氢即为电解水所得。制取3molH2需电解水的物质的量为 (根据方程式列式计算)
请根据装置回答。
(1)写出仪器名称:a b 。
(2)实验室用过氧化氢制取氧气时,为使反应平稳进行可选择的发生装置为 (填字母,下同)。收集较纯净的氧气可选择的装置为 。
(3)实验室制取CO2时反应的化学方程式为 ,可用装置B与装置 进行组合制取CO2,若用装置C代替B进行实验,其优点为 。
同学们对实验“煅烧石灰石”展开深入探究。
(1)煅烧石灰石。可观察到石灰石的表面 。
(2)为证明石灰石已分解,三位同学从其他角度设计方案如下:
Ⅰ.甲同学按图一所示进行实验(煤气灯亦能达到石灰石分解的温度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式__ __。
II.乙同学按图二所示进行试验,观察到B中液体变 色,A中实验的作用 。
III.丙同学取一块石灰石进行煅烧,一段时间后发现固体质量减轻mg(即CO2的质量),证明石灰石已分解。
IV.大家认为甲同学的方案不合理,请分析原因 _ 。
(3)为测定石灰石的纯度,丙同学将他刚才煅烧后的固体放入足量稀盐酸中,又产生mg气体,结合上述数据计算可知,丙所取的这块石灰石中含碳酸钙 _ mol(用m表示)。
正确的实验操作是实验成功的重要保证,请对一下实验进行分析。
| 实验内容 |
实验装置 |
过程与分析 |
| 铁丝在纯氧中燃烧 |
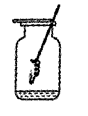 |
如图所示,点燃火柴后立即连同铁丝快速深入集气瓶中下部(未接触水),但铁丝未燃烧,针对上述操作,请提出一条改进建议 。 |
| 测定空气中O2的含量 |
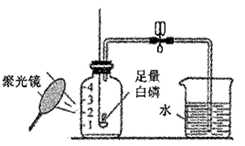 |
①用聚光镜引燃白磷后夹紧弹簧夹。 ②反应停止冷却至室温,打开弹簧夹,进入瓶内的水超过瓶容积的1/5。 ③从操作角度分析,产生误差的原因可能是(写一点) 。 |
| 用草酸钠(Na2C2O4)分解产生的CO还原CuO(铁架台略) |
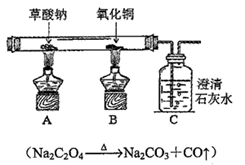 |
①实验开始,应先点燃A处酒精灯,过一会再点燃B处酒精灯,这样操作的目的是_____ _______。 ②B处玻璃管内的现象是___ ____,发生反应的化学方程式为 。 ③该装置有待改进之处是 。 |


 粤公网安备 44130202000953号
粤公网安备 44130202000953号