[湖南]2013年初中毕业升学考试(湖南湘潭卷)化学
宇航员在太空舱中常用 作催化剂,将呼出的气体和某些物质转化为氧气.已知其中 元素为+2价,则 元素的化合价为()
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
下列做法不会危及食品安全的是
如图所示是甲、乙粒子的结构示意图,下列有关说法正确的是( )

| A. | 甲粒子是阳离子 | B. | 乙粒子是原子 |
| C. | 两种粒子属于同种元素 | D. | 甲粒子的化学性质比乙粒子稳定 |
2013年3月在上海和安徽相继发现 型禽流感,达菲是一种抗病毒药物,能有效防治 型禽流感,其化学式为 ,下列有关说法不正确的是()
| A. | 达菲由四种元素组成 |
| B. | 一个达菲分子由50个原子构成 |
| C. | 达菲中碳、氢、氧三种元素的质量之比为48:7:16 |
| D. | 达菲完全燃烧后只生成二氧化碳和水 |
有
三种金属:把它们投入稀盐酸中,只有
表面有气泡冒出,把
投入到
的硝酸盐溶液中,
表面有
析出,则
三种金属的活动性由强到弱的顺序是
小明旅游时经常使用一种用纸代替金属材料制成的锅煮面,轻便易携带,你觉得煮面时纸锅不会被烧掉的原因是( )

| A. | 纸锅的着火点很高 |
| B. | 面汤使纸锅的着火点升高了 |
| C. | 面汤隔绝了氧气使纸锅不能燃烧 |
| D. | 加热时面汤蒸发吸热使纸锅温度达不到其着火点 |
新装修的房间常因苯超标而损害人体健康,苯(以 表示)燃烧的化学方程式如下: , 的化学式为( )
| A. | B. | C. | D. |
以下各组溶液,不用其它试剂就能鉴别出来的是()
| A. |
、 、 、 |
| B. |
、 、 、 |
| C. |
、 、 、 |
| D. |
、 、 、 |
在托盘天平的两边各放一只烧杯,调节天平至平衡,向两烧杯中分别注入等质量、等质量分数的稀硫酸(足量),然后向右盘的烧杯中放入一定质量的 粉,同时向左盘的烧杯中放入与 粉等质量的 粉,反应过程中可能出现的现象是()
| A. | 天平最终仍然平衡 | B. | 天平指针先偏向左盘,后偏向右盘 |
| C. | 天平指针始终偏向右盘 | D. | 天平指针先偏向右盘,后偏向左盘 |
除去下列各组物质中的杂质,所用的试剂和方法不正确的是
| 物质 |
杂质 |
所用的试剂和方法 |
|
| A |
|
|
加适量的硝酸银溶液,过滤 |
| B |
|
|
加水溶解、过滤、蒸发结晶 |
| C |
|
|
加过量的铁粉,过滤 |
| D |
|
加
溶液,过滤 |
下列图象不能反映客观事实的是

往 溶液中逐滴加入稀硫酸
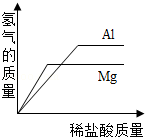
往等质量的铝和镁中加入足量的稀盐酸

往稀 的混合溶液中逐滴加入 溶液
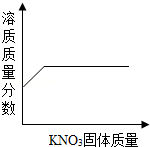
等温条件下往接近饱和的硝酸钾溶液中不断加入硝酸钾固体
物质的性质决定用途.从下列物质中选择适当的物质填入下表(填序号).
①生石灰;②干冰;③熟石灰;④氢氧化铝.
| 物质用途 |
改良酸性土壤 |
用于食品干燥 |
治疗胃酸过多 |
用于人工降雨 |
| 物质序号 |
|
|
|
|
化学与生活息息相关,我们的生活离不开化学.
(1)国家提倡使用的加碘盐,是在食盐中加入适量的碘酸钾,加碘食盐里的"碘"指的是(填"单质"、"元素"或"原子").已知碘酸钾受热不稳定,因此,你认为炒菜时宜(填"早"或"迟")加入加碘盐更有利.
(2)仔细观察如图后回答:

①该图反映的环境问题是;
②针对上述环境问题,请你提出一条合理化建议.
3月22日是"世界水日".水与人类的生活和生产密切相关.
(1)天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化.其中净化程度最高的是.
(2)硬水给生活和生产带来很大不利影响,生活中可用来区分硬水和软水.
(3)生活中通过可以降低水的硬度.
(4)日常生活中你经常采用的节水措施有.
甲、乙、丙三种物质的溶解度曲线如图所示,据图回答下列问题:

(1)
时,甲物质的溶解度是.
(2)
时,甲、乙、丙三种物质的溶解度由大到小的顺序是.
(3)要使
时接近饱和的丙溶液变成饱和溶液,可采用的一种方法是.
(4)向100g
时的水中,加入31g甲固体充分搅拌,发现甲全部溶解,一段时间后又有部分甲析出.你认为甲开始能"全部溶解"的原因可能是.
据央视报道,有不法酒类生产企业在白酒中添加酯类物质以增强口感.下表中是几种常见的酯.

| 酯的名称 |
甲酸甲酯 |
甲酸乙酯 |
乙酸甲酯 |
乙酸乙酯 |
| 化学式 |
(1)比较归纳是学习化学的重要方法,上述物质的共同特点有
(2)甲酸甲酯(
)中碳、氢、氧的原子个数比为
(3)据表推测
的化学式为
(4)实验测得由甲酸甲酯(
)、甲酸乙酯(
)组成的混合物中碳元素的质量分数是43.2%,则氧元素的质量分数是
有一包固体粉末,可能由
中的一种或几种所组成.小文为了确定它的成分,进行了如下实验:

(1)操作
的名称是(填"蒸发"或"过滤"),其中必须要用到的玻璃仪器有烧杯、玻璃棒和.
(2)写出蓝色沉淀的化学式:.
(3)白色固体是,它与盐酸反应的化学方程式为,该反应所属基本反应类型为.
(4)小文通过实验后认为,这包固体粉末中只有两种物质,他的判断是(填"正确"或"错误")的,理由是.
实验室制取氧气所需装置如图1所示.回答下列问题:

(1)写出仪器名称:a
(2)用过氧化氢溶液和二氧化锰制取氧气时,所选用的发生装置是
(3)若用锌与稀硫酸制取氢气,反应的化学方程式是
(4)若采用如图2所示装置制取氧气并测定其体积,实验前应检查装置的气密性.为了准确测定氧气的体积,有人提出读数时应该注意以下事项:①容器中气体必须冷却至室温;②长颈漏斗不能倾斜;③必须使量气管和长颈漏斗两边液面相平;④视线应与液体凹液面最低处保持水平.你认为必须要做到的是
天然气作为燃料已进入千家万户,其主要成分是

【提出猜想】生成物中一定有
【实验探究】该小组同学生成的混合气体,依次通过如图所示的装置,验证猜想.
【现象与结论】
(1)观察到A中
(2)C中浓硫酸的作用是
(3)观察到D中粉末由黑色变成
【交流讨论】(4)小武认为:从E装置中澄清石灰水变浑浊也能推断出混合气中有一氧化碳,那么B中
溶液的作用是
(5)小文则提出:从环保的角度看,此装置有一个不足之处,你认为是
某实验小组为检验露置在空气中的NaOH固体是否变质并确定其组成,开展了一下探究活动.
【讨论与交流】
(1)NaOH能与空气中的 (填化学式)发生反应生成Na2CO3.
(2)Na2CO3的水溶液呈碱性.
【查阅资料】
(3)NaOH在空气中不会转化成NaHCO3;
(4)CaCl2、NaCl的水溶液均呈中性.
【猜想假设】猜想一:固体全部为NaOH.
猜想一:固体全部为 .
猜想一:固体为NaOH和Na2CO3的混合物.
【实验探究】将待检固体溶于水配成溶液.按以下两种方案进行实验:
方案一:用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH (填“>”、“<”或“=”),说明猜想一成立.、
方案二:取该溶液少许,往其中加入足量CaCl2溶液,有白色沉淀产生;待沉淀不再产生,过滤,再往滤液中滴入酚酞试液,溶液变成 色,说明猜想三成立.
【归纳与总结】很明显,方案一的结论 (填“正确”或“错误”),理由是 .
【探究与拓展】为进一步确定原固体的组成,该实验小组的同学称取26.6g待检固体,按如图所示过程实验(步骤②产生的气体全部逸出),请参照图中提供的数据计算:
(5)26.6g固体混合物中Na2CO3的质量.
(6)所用稀盐酸中溶质的质量分数.
(7)实验最终所得351g溶液中溶质的质量分数.




 稀释浓硫酸
稀释浓硫酸 称量固体
称量固体 氧气验满
氧气验满 点燃酒精灯
点燃酒精灯 粤公网安备 44130202000953号
粤公网安备 44130202000953号