[河南]2012-2013学年河南省许昌市六校高一第六次联考化学试卷
氯元素在自然界有35Cl和37C1两种同位素,在计算式34.969×75.77 %+36.966×
24.23%=35.453中 ( )
| A.75.77%表示35C1的质量分数 | B.24.23%表示35C1的浓度 |
| C.35.453表示氯元素的相对原子质量 | D.36. 966表示37C1的质量数 |
下列说法正确的是( )
| A.在常温下,放热反应一般能自发进行,吸热反应都不能自发进行 |
| B.NH4HCO3(s)=====NH3(g)+H2O(g)+CO2(g)△H="+185.57" kJ·mol-1,能自发进行,原 因是体系有自发地向混乱度增加的方向转变的倾向 |
| C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自 发性的判据 |
| D.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向 |
在密闭容器内充入4 mol S02和3mol 02,在一定条件下建立平衡:
2SO2(g)+02(g)  2SO3(g) △H="-Q" kJ·mol-1(Q>0),测得SO2的转化率为90%,
2SO3(g) △H="-Q" kJ·mol-1(Q>0),测得SO2的转化率为90%,
则在此条件下反应放出的热量为( )
| A.1.8Q kJ | B.2Q kJ | C.Q kJ | D.0.9 QJ |
下列有关化学用语表示正确的是( )
A.N2的电子式: |
B.S2-的结构示意图: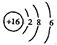 |
C.NH4Br的电子式: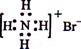 |
D.原子核内有l8个中子的氯原子: |
已知一定温度下,下列反应的平衡常数:H2(g)+S(s)  H2S(g) K1,
H2S(g) K1,
S(s)+02(g)  SO2(g) K2。则相同温度下反应H2(g)+SO2(g)
SO2(g) K2。则相同温度下反应H2(g)+SO2(g)  O2(g)+H2S(g)的
O2(g)+H2S(g)的
平衡常数为( )
| A.K1+K2 | B.K1-K2 | C.K1·K2 | D.K1/K2 |
已知反应:3A(g)+B(g)  2C(g)+2D(g) △H<0。右图中曲线a、b分别表示在不同条件下,A与B反应时,D的体积分数随时间t的变化情况。若想使曲线b(实线)变为曲线a(虚线),可采用的措
2C(g)+2D(g) △H<0。右图中曲线a、b分别表示在不同条件下,A与B反应时,D的体积分数随时间t的变化情况。若想使曲线b(实线)变为曲线a(虚线),可采用的措
施是( )
①增大A的浓度 ②升高温度
③增大D的浓度④加入催化剂
⑤恒温下,缩小反应容器的体积
⑥加入稀有气体,保持容器内压强不变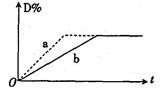
| A.①②③ | B.④⑤ | C.③④⑤ | D.④⑤⑥ |
下列关于原子结构、元素性质的说法正确的是( )
| A.非金属元素组成的化合物中只含共价键 |
| B.IA族金属元素是同周期中金属性最强的元素 |
| C.同种元素的原子均有相同的质子数和中子数 |
| D.ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强 |
下列有关化学反应速率的描述中正确的是 ( )
| A.在任何化学反应中,只要提高反应温度,就可提高反应速率 |
| B.在任何化学反应中,只要增大某一反应物的用量,就会增大反应速率 |
| C.在任何化学反应中,增大压强时,都会使反应速率增大 |
| D.在任何化学反应中,只要缩小容器的体积,都会使反应速率增大 |
下表是部分短周期元素的相关信息:
| 元素代号 |
L |
M |
T |
Q |
R |
| 原子半径/nm |
0.154 |
0.130 |
0.118 |
0.102 |
0.073 |
| 主要化合价 |
+1 |
+2 |
+3 |
+6、-2 |
-2 |
下列判断正确的是( )
A.沸点:H2Q>H2R
B. 碱性:T(OH)3>M(OH)2
C. T和Q 两者最高价氧化物对应的水化物可以发生反应
D. L与R形成的化合物中只能含有离子键
一定温度下,在固定容积的密闭容器中,有可逆反应mA(g)+nB(g)  pC(g)+qD(g),
pC(g)+qD(g),
当m、n、p、q为任意正整数时,下列状态:
①体系的压强不再发生变化 ②体系的密度不再发生变化
③各组分的物质的量浓度不再改变 ④各组分的质量分数不再改变
⑤反应速率v(A):v(B):v(C):v(D)=m:n:p:q,
其中一定能说明反应已达到平衡的是( )
A. 只有③④ B. ②③④
C. ①②③④ D. ①②③④⑤
一定条件下,通过下列反应可实现燃煤烟气中硫的回收: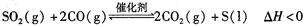 若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
| A.平衡前,随着反应的进行,容器内压强始终不变 |
| B.平衡时,其他条件不变,分离出硫,正反应速率加快 |
| C.平衡时,其他条件不变,升高温度可提高SO2的转化率 |
| D.其他条件不变,使用不同催化剂,该反应的平衡常数不变 |
在一化学平衡状态体系中,发生下列量的变化,其中一定会使平衡发生移动的是( )
| A.反应物的浓度 | B.反应物的转化率 |
| C.正、逆反应速率 | D.体系的压强 |
某温度下,将2 mol A和3 mol B充入一密闭的容器中,发生反应:
xA(g)+B(g)  C(g)+D(g),5 min后达到平衡。已知各物质的平衡浓度关系为
C(g)+D(g),5 min后达到平衡。已知各物质的平衡浓度关系为
cx(A)·c(B)=c(C)·c(D),若在温度不变的情况下将容器的体积扩大为原来的10倍,
A的转化率不发生变化,则B的转化率为( )
A. 40% B. 60% C. 24% D. 4%
有关化学平衡常数(K)的说法中不正确的是( )
| A.K值越大,正反应进行的程度越大 |
| B.一般地说,K>105时,该反应进行得就基本完全了 |
| C.压强越大,K值越大 |
| D.K与反应物或生成物的浓度变化无关 |
可逆反应在一定条件下达到平衡后,速率差值[即v(正)—v(逆)]与压强的变化曲线如右图所示,其中与曲线①相符的反应为( )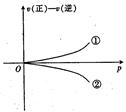
A.2SO3(g)  2SO2(g)+02(g) 2SO2(g)+02(g) |
B.H2(g)+I2(g)  2HI(g) 2HI(g) |
C.C(s)+H2O(g)  C0(g)+H2(g) C0(g)+H2(g) |
D.N2(g)+3H2(g)  2NH3(g) 2NH3(g) |
在密闭容器中,一定条件下进行反应:mA(g)+nB (g)  pC(g)+qD(g)。若增大压强或升高温度,重新达到平衡,随时间变化过程均如图所示,则对该反应的叙述中正确的是( )
pC(g)+qD(g)。若增大压强或升高温度,重新达到平衡,随时间变化过程均如图所示,则对该反应的叙述中正确的是( )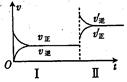
| A.正反应是放热反应,m+n<p+q |
| B.逆反应是放热反应,m+n>p+q |
| C.正反应是放热反应,m+n>p+q |
| D.逆反应是放热反应,m+n<p+q |
A、B的混合气体在密闭容器中发生如下反应:xA(g)+yB(g)  zC(g) △H<0。
zC(g) △H<0。
达到化学平衡后测得A的浓度为0.5 mol·L-1;在恒温下,将密闭容器的容积压缩至
原来的二分之一,再次达到平衡时,测得A的浓度为0.9 mol·L-1。则下列叙述中
正确的是( )
A. 平衡向正反应方向移动了 B. x+y<z
C. B的转化率下降 D. C的体积分数减小
反应:2X (g)+Y(g)  2Z(g)在不同温度和压强下的产物Z的物质的量和反应时
2Z(g)在不同温度和压强下的产物Z的物质的量和反应时
间t的关系如下图所示:下列判断正确的是( )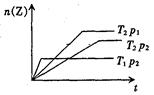
| A.P1>P2 T1>T2△H<0 |
| B.P1>P2 T1<T2△H<0 |
| C.P1<P2 T1>T2△H>0 |
| D.P1<P2 T1<T2△H>0 |
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主
族,可形成离子化合物ZX,Y、M同主族,可形成MY2、MY3两种分子。请回答下列问题:
(1)Y在元素周期表中的位置为 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式),
非金属气态氢化物还原性最强的是 (写化学式)。
(3)X2M的燃烧热△H=-a kJ·mol-1,写出X2M燃烧反应的热化学方程式: 。
(4)ZX的电子式为 ;ZX与水反应放出气体的化学方程式为 。
(1)一定条件下,可逆反应:A2(g)+B2(g)  2C(g)达到平衡时,各物质的
2C(g)达到平衡时,各物质的
平衡浓度分别为:c(A2)=0.5 mol·L-1;c(B2)=0.1 mol·L-1;c(C)=1.6 mol·L-1。
若用a、b、c分别表示A2、B2、C的初始浓度(mol·L-1),则:
①a、b应满足的关系式是 。
②a的取值范围是 。
(2)氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,肼(N2H4)可
作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)="===" N2O4 (1) △H1= -19.5kJ·mol-1
②N2H4(1)+O2(g)="===" N2(g)+2H2O(g) △H2= -534.2kJ·mol-1
写出肼和N2O4反应的热化学方程式 ;
(1)火箭残骸中常现红棕色气体,原因为: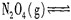
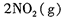
当温度升高时,气体颜色变深,则反应为 (填“吸热”或“放热”)
反应。
(2)一定温度下,上述反应的焓变为△H。现将1mol N2O4充入一恒压密闭容器中,
下列示意图正确且能说明反应达到平衡状态的是 。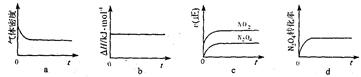
若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数
(填“增大”“不变”或“减小”),反应3s后NO2的物质的量为0.6mol,
则0~3s内的平均反应速率v(N2O4)= mol·L-1·s-1。
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲
醇。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、
-283.0kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 ;
(2)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考查温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);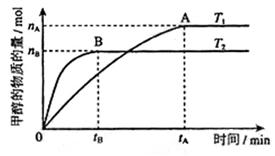
下列说法正确的是 (填序号)
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=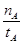 mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时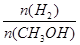 增大
增大
(3)在T1温度时,将1molCO2和3molH2充入一密闭恒容容器中,充分反应达到平衡后,若CO2转化率为α,则容器内的压强与起始压强之比为 ;
已知A(g)+B(g)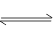 C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| 温度/℃ |
700 |
900 |
830 |
1000 |
1200 |
| 平衡常数 |
1.7 |
1.1 |
1.0 |
0.6 |
0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。
则6s时c(A)= mol·L-1, C的物质的量为 mol;
若反应经一段时间后,达到平衡时A的转化率为 ,
如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为 ;
(3)判断该反应是否达到平衡的依据为 (填正确选项前的字母):
a.压强不随时间改变 b.气体的密度不随时间改变
c. c(A)不随时问改变 d.单位时间里生成c和D的物质的量相等
(4)1200℃时反应C(g)+D(g)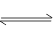 A(g)+B(g)的平衡常数的值为 。
A(g)+B(g)的平衡常数的值为 。
 2C(g) △H=-QkJ·mol-1 (Q>0)在一个密闭容
2C(g) △H=-QkJ·mol-1 (Q>0)在一个密闭容 粤公网安备 44130202000953号
粤公网安备 44130202000953号