[河北]2011-2012学年河北省迁安市高二第一学期期中考试化学试卷
热化学方程式中化学式前面的计量数表示
| A.分子个数 | B.原子个数 | C.物质的质量 | D.物质的量 |
可逆反应2SO2(g)+O2(g)  2SO3(g)正在逆向进行时,正反应速率和逆反应速率的大小是
2SO3(g)正在逆向进行时,正反应速率和逆反应速率的大小是
| A.v正>v逆 | B.v正< v逆 | C.v正=v逆 | D.不能确定 |
关于如图所示装置的叙述,正确的是
| A.铜是负极,铜片上有气泡产生 |
| B.铜片质量逐渐减少 |
| C.电流从锌片经导线流向铜片 |
| D.氢离子在铜片表面被还原 |
下列反应中生成物总能量高于反应物总能量的是
| A.碳酸钙受热分解 | B.乙醇燃烧 |
| C.铝粉与氧化铁粉末反应 | D.氧化钙溶于水 |
14CO2与碳在高温条件下发生反应:14CO2+C 2CO,达到化学平衡后,平衡混合物中含14C的微粒有
2CO,达到化学平衡后,平衡混合物中含14C的微粒有
| A.14CO2 | B.14CO2、14CO | C.14CO2、14CO、14C | D.14CO |
“活化分子”是衡量化学反应速率快慢的重要依据,下列对“活化分子”的说法中不正确的是
| A.活化分子之间的碰撞一定是有效碰撞 |
| B.增大反应物的浓度,可使单位体积内活化分子增多,反应速率加快 |
| C.对于有气体参加的反应增大压强,可使单位体积内活化分子增多,反应速率加快 |
| D.催化剂能降低反应的活化能,使单位体积内活化分子百分数大大增加 |
下列说法错误的是
| A.NH4NO3溶于水虽然吸热,但其溶于水是自发过程 |
| B.加热液体(温度高于沸点)会自发转变成气体,可用焓变解释 |
| C.对于同一物质来讲,熵值的大小与其状态有关,固态物质的熵值通常最小 |
| D.要正确判断化学反应能否自发进行,要综合考虑反应的ΔH和ΔS。 |
在火烧圆明园时流失了大量的国宝,如:铜铸的鼠首和兔首。普通铜器时间稍久容易出现铜绿,其主要成分是〔Cu2(OH)2CO3〕,这两件1760年铜铸的国宝在240多年后看上去仍然熠熠生辉不生锈,下列对其原因的分析最可能的是:
| A.它们的表面都电镀上了一层耐腐蚀的黄金 |
| B.环境污染日趋严重,它们表面的铜绿被酸雨溶解洗去 |
| C.铜的金属活动性比氢小,因此不易被氧化 |
| D.它是含一定比例金、银、锡、锌的铜合金 |
下列事实,不能用勒夏特列原理解释的是
A.在溴水中存在如下平衡:Br2+H2O  HBr+HBrO当加入NaOH溶液后颜色变浅 HBr+HBrO当加入NaOH溶液后颜色变浅 |
B.对2HI H2+I2(g)平衡体系增加压强使颜色变深 H2+I2(g)平衡体系增加压强使颜色变深 |
C.反应CO+NO2 CO2+NO ΔH<0升高温度使平衡向逆方向移动 CO2+NO ΔH<0升高温度使平衡向逆方向移动 |
D.合成氨反应:   ,ΔH<0 为使氨的产率提高,理论上应采取低温高压的措施 ,ΔH<0 为使氨的产率提高,理论上应采取低温高压的措施 |
打开右图所示装置中的止水夹,一段时间后,可能观察到的现象是
| A.烧杯中有气泡产生 | B.试管内有黄绿色气体产生 |
| C.铁丝网的表面产生锈迹 | D.烧杯内溶液变红色 |
已知有如下平衡体系:3A(g) + B(g) 2C(g),现等物质的量的投料反应物A、B于恒温恒容体系I和恒温、恒压体系II中,达平衡时体系I中A的物质的量浓度为M,体系II中A的物质的量浓度为m,则M与m的关系为
2C(g),现等物质的量的投料反应物A、B于恒温恒容体系I和恒温、恒压体系II中,达平衡时体系I中A的物质的量浓度为M,体系II中A的物质的量浓度为m,则M与m的关系为
A.M = m B.M > m C.M < m D.以上情况都有可能
下列与化学反应能量变化相关的叙述正确的是
| A.生成物总能量一定低于反应物总能量 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下,H2(g)+Cl2(g) |
铅蓄电池的电极材料是Pb和PbO2,电解液是硫酸溶液。现用铅蓄电池电解饱和硫酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法不正确的是
| A.蓄电池放电时,每消耗0.1molPb,共生成0.1molPbSO4 |
| B.电解池的阳极反应式为:4OH-- 4e-==2H2O + O2↑ |
| C.电解后,c(Na2SO4)不变,且溶液中有晶体析出 |
| D.蓄电池中每生成2molH2O,电解池中就消耗1molH2O |
右图是298K 时N2与H2反应过程中能量变化的曲线图。下列叙述不正确的是
A.该反应的热化学方程式为:N2(g) + 3H2(g)  2NH3(g) ΔH = -92kJ·mol-1 2NH3(g) ΔH = -92kJ·mol-1 |
| B.b曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂, 该化学反应的活化能和反应热都改变 |
| D.在温度体积一定的条件下, 通入lmol N2和3molH2反应后放出的热量为Q1kJ, 若通入2molN2和6molH2反应后放出的热量为Q2kJ 则184>Q2 >2Q1 |
对下列实验的描述正确的是
| A.图1所示的实验:根据检流计(G)中指针偏转的方向比较Zn、Cu的金属活泼性 |
| B.图2所示的实验:根据小试管中液面的变化判断铁钉发生析氢腐蚀 |
| C.图3所示的实验:根据温度计读数的变化用浓硫酸和NaOH反应测定中和热 |
D.图4所示的实验:根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)判断2NO2(g) N2O4(g)是吸热反应 N2O4(g)是吸热反应 |
爱迪生电池在充电和放电时发生的反应:Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2,下列对该蓄电池推断错误的是:
Fe(OH)2+Ni(OH)2,下列对该蓄电池推断错误的是:
①放电时,Fe参与负极反应,NiO2参与正极反应
②充电时,阴极上的电极反应式为:Fe(OH)2 + 2e-=" Fe" + 2OH-
③放电时,电解质溶液中的阴离子向正极方向移动
④放电时,负极上的电极反应式为:Fe + 2H2O-2e- = Fe(OH)2 + 2H+
⑤蓄电池的电极必须浸入某种碱性电解质溶液中
| A.只有③ | B.③④ | C.④⑤ | D.①②⑤ |
右图为反应2SO2+O2 2SO3的速率v(SO2)变化的图像,则横坐标可能是
2SO3的速率v(SO2)变化的图像,则横坐标可能是
| A.反应时间 | B.温度 |
| C.压强 | D.SO2的浓度 |
通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估计化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表是一些化学键的键能。
| 化学键 |
C—H |
C—F |
H—F |
F—F |
| 键能/(kJ·mol-1) |
414 |
489 |
565 |
155 |
根据键能数据估算下列反应CH4(g)+4F2(g)===CF4(g)+4HF(g)的反应热ΔH为
A.-1940kJ·mol-1 B.1940kJ·mol-1 C.-485kJ·mol-1 D.485kJ·mol-1
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)  2NH3(g),ΔH<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
2NH3(g),ΔH<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
| A.点a的n(H2)和点b的n(NH3)比值为3:2 |
| B.点 c处反应达到平衡 |
| C.点d (t1时刻) 和点 e (t2时刻) 处n(N2)不一样 |
| D.其他条件不变,773K下反应至t1时刻,n(H2)比上图中d点的值大 |
一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g)  Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是
Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是
| A.达到平衡时X浓度为0.04 mol/L |
| B.将容器体积变为20 L,Z的平衡浓度变为0.015mol/L |
| C.若增大压强,平衡向正方向移动,平衡常数变大 |
| D.若升高温度,X的体积分数增大,则该反应的DH>0 |
(12分)⑴已知甲醇在常温下为液体,其热值为22.7kJ•g-1,则甲醇的标准燃烧热的热化学方程式为_______________________________________________。
⑵将甲醇、氧气和氢氧化钾溶液设计成燃料电池,该电池正极反应式为
____________________________________。
⑶右图为工业上氯碱工业的电解槽示意图,据图回答:
①图中a、b、c处物质名称分别是: a_________________;b________________;c___________________。
②若没有阳离子交换膜,则电解一段时间后在电解槽的溶液中可能发生的化学反应方程式为__________________________。
⑷反应2A B+C 在某一温度时达到平衡。
B+C 在某一温度时达到平衡。
①若温度升高,平衡向正反应方向移动,则正反应是__________热反应;
②若B为固体,降低压强平衡向逆反应方向移动,则A呈____________态;
③若A是气态时,加压时,平衡不移动,则B为_________态,C为________态。
(9分)认真观察下列装置,回答下列问题:
⑴装置B中PbO2上发生的电极反应方程式为 。
⑵装置A中总反应的离子方程式为 。
⑶若装置E中的目的是在Cu材料上镀银,则X为 ,极板N的材料为 。
若装置E的目的是验证金属的电化学防腐,则极板N的材料为__________________ 。
⑷当装置A中Cu电极质量改变6 .4g时,装置D中产生的气体体积为 L(标准状况下)。
(9分)研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
⑴NO2可用水吸收,相应的化学反应方程式为____________________________。利用反应6NO2+ 8NH3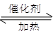 7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH= kJ·mol-1。
SO3(g)+NO(g)的ΔH= kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K= 。
(14分)影响化学反应速率的因素很多,某课外兴趣小组用实验的方法通过图1所示装置研究反应速率的有关问题。
图1 图2
⑴取一段镁条,用砂纸擦去表面的氧化膜,使镁条浸入锥形瓶内足量的稀盐酸中。足量镁条与一定量盐酸反应生成H2的量与反应时间的关系曲线如图2所示。
①请在图3 的方框中画出上述反应的速率与时间的关系曲线。
图3
②在前4min内,镁条与盐酸的反应速率逐渐加快,在4min之后,反应速率逐渐减慢,请简述其原因:___________________________________________________________
__________________________________________________________________________。
(2)某同学发现,纯度、质量、表面积都相同的两铝片与H+浓度相同的盐酸和硫酸在同温同压下反应时产生氢气的速率差别很大,铝和盐酸反应速率更快。他决定对其原因进行探究。填写下列空白:
①该同学认为:由于预先控制了反应的其他条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:
原因Ⅰ:Cl-对反应具有促进作用,而SO2- 4对反应没有影响;
原因Ⅱ:Cl-对反应没有影响,而SO2- 4对反应具有阻碍作用;
原因Ⅲ:____________________________________________________;
原因Ⅳ:Cl-、SO2- 4均对反应具有促进作用,但Cl-影响更大;
原因Ⅴ:________________________________________________________。
②该同学设计并进行了两组实验,即得出了正确结论。他取了两片等质量、外形和组成相同、表面经过砂纸充分打磨的铝片,分别放入到盛有同体积、c(H+)相同的稀硫酸和盐酸的试管(两试管的规格相同)中:
a.在盛有硫酸的试管中加入少量NaCl或KCl固体,观察反应速率是否变化;
b.在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否变化。
若观察到实验a中_________________________,实验b中________________________,则说明原因Ⅰ是正确的。依次类推。该同学通过分析实验现象,得出了结论:Cl-对反应具有加速作用。
在一定温度下有甲、乙两容积相等的密闭容器(两容器容积保持不变)。
(1)向甲容器中通入3 mol N2和4 mol H2,反应达到平衡时,生成NH3amol。此时,NH3的物质的量分数是________。(用含有“a”的表达式表示)。若在达到平衡状态的甲容器中通入少量的N2,则达到新平衡时,体系中N2的体积分数将________(选填“增大”、“减小”或“不变”)。
(2) 若起始时,向乙中通入6mol N2和8mol H2,达到平衡时,生成的NH3的物质的量为b mol, (选填“>”、“<”或“=”)。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号