[河南]2012届河南省许昌新乡平顶山高三第一次调研考试理科综合试题(化学部分)
下列说法正确的是
| A.在标准状况下,22.4L SO3所含有的氧原子数为3×6.02×1023 |
| B.在标准状况下,22.4LNO和NO2的混合气中,所含有氮原子的个数为6.02×1023 |
| C.20mL0.1mol·L—1NaCl与10mL0.1mol·L—1BaCl2溶液中氯离子物质的量浓度相等 |
| D.在Na2O2与水的反应中,生成1mol O2转移的电子数为4×6.02×1023 |
下列各组液体混合物中,能用分液漏斗分离的是
| A.淀粉溶液和食盐溶液 | B.CCl4和水 |
| C.乙酸和乙酸乙酯 | D.乙酸和乙醇 |
下列化合物的分子中,所有原子都处于同一平面的是
| A.乙酸 | B.甲苯 | C.甲醇 | D.四氟乙烯 |
几种短周期元素的原子半径及主要化合价见下表:
| 元素代号 |
a |
b |
c |
d |
e |
| 原子半径/nm |
0.089 |
0.074 |
0.160 |
0.143 |
0.102 |
| 主要化合价 |
+2 |
-2 |
+2 |
+3 |
+6 -2 |
下列说法正确的是
A.b和e所形成的化合物一定能使酸性高锰酸钾溶液褪色
B.a的单质与稀硫酸反应的速率比c快
C.d的氢氧化物为两性氢氧化物
D.这些元素应位于周期表中的同一周期
常温下,某溶液中由水电离产生的氢离子和氢氧根离子浓度的乘积为1×10—20。则一定能在该溶液中大量共存的离子组是
| A.Ca2+、Na+、Cl—、NO3— | B.NO3—、Fe3+、Mg2+、SO42— |
| C.ClO—、CH3COO—、Na+、Br— | D.K+、Cl—、Al3+、SO32— |
下列离子反应方程式正确的是
A.H2O2+2OH— 2H2O +O2↑ 2H2O +O2↑ |
B.Cl2+6OH— ClO3—+5Cl—+3H2O ClO3—+5Cl—+3H2O |
| C.2MnO4—+H2O2+6H+=2Mn2++3O2↑+4H2O |
| D.3MnO42—+4H+=2MnO4—+MnO2+2H2O |
Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4—SOCl2。电池的总反应可表示为:4Li+2SOCl2 =" 4LiCl" +S +SO2。下列说法中不正确的是
| A.该电池的负极反应为2SOCl2 + 4e— = S +SO2+4Cl— |
| B.该电池的负极反应为4Li = 4Li+ + 4e— |
| C.反应SOCl2 + H2O = SO2↑ + 2HCl↑为非氧化还原反应 |
| D.组装该电池必须在无水的条件下进行 |
化合物A俗称石灰氮,以前是一种常用的肥料,其含氮量可高达 35.0%,钙含量为50%。它可以用CaCO3通过下列步骤方便地制出:
(1)已知固态二元化合物D中钙含量为62.5%,则D的化学式为 。
(2)请推算出A的化学式。 。
(3)分别写出上述过程中生成D和A的化学方程式。 ; 。
(4) 将A放入水中,会重新生成CaCO3并放出刺激性气味的气体,请写出发生反应的化学方程式。 。
(5)已知CaCO3与CaSO4的溶度积分别为2.8×10—9、9.1×10—6。由此可知二者的溶解度的大小关系为CaCO3 CaSO4。在锅炉除垢操作中,要先用碳酸钠溶液将水垢中的硫酸钙转化成为碳酸钙。其主要原因是 。
。
二氧化硫和氮的氧化物是重要的化工原料,同时也是造成大气污染的主要物质。对其性质的研究是化学的重要任务。
(1)硫酸生产中,SO2催化氧化生成SO3:
2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如右图所示。根据图示回答下列问题: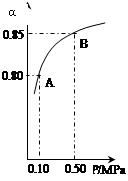
①将2.0mol SO2和1.0mol O2置于10L密闭容器中,反应达平衡后,体系总压强为0.10MPa。该反应的平衡常数等于_____。
②平衡状态由A变到B时.平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)N2O5在四氯化碳溶液中的分解反应为:2N2O5=4NO2+O2。实验测得在67℃时反应体系中N2O5的物质的量浓度随时间的变化如下表所示。
| t/min |
0 |
1 |
2 |
3 |
4 |
5 |
| c(N2O5)/mol·L—1 |
1.00 |
0.71 |
0.50 |
0.35 |
0.25 |
0.17 |
①实验进行的前1分钟和最后1分钟,用N2O5的物质的量浓度变化表示的平均反应速率分别是 、 。
②实验进行的最后1分钟,用NO2的物质的量浓度变化表示的平均反应速率是 ;5分钟时NO2的物质的量浓度是 。
(3)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ·mol-1
若用标准状况下4.48L CH4还原NO2至N2,整个过程中放出的热量为____kJ。
S2Cl2是一种易挥发的液体(熔点:—76℃,沸点:138℃),且易与水发生水解反应,可能生成H2S、SO2、H2SO3、H2SO4等物质。它是橡胶硫化剂。在熔融的硫中通以氯气即可生成S2Cl2。下图是实验室用S和Cl2制备S2Cl2的装置 (夹持装置、加热装置均已略去)。
(1)已知S2Cl2分子结构与H2O2相似,则S2Cl2的分子中共含有 条共价键。
(2)装置a中应放试剂为 ;装置d的名称是 ,它的作用是 。
(3)该实验的操作顺序应为 (用序号表示)。
①加热装置c ②通入Cl2 ③通冷凝水 ④停止通Cl2 ⑤停止加热装置c
(4)图中f装置中应放置的试剂为 ,其作用为 。
(5)将S2Cl2的水解气体产物通入氯水中,若观察到 的现象,则可证明水解产物中有硫化氢生成。
【化学——选修2:化学与技术】
水是一种重要的自然资源,是人类赖以生存不可缺少的物质。水质优劣直接影响人体健康。请回答下列问题:
(1)天然水中溶解的气体主要有 、 。
(2)天然水在净化处理过程中加入的混凝剂可以是 ,其净水作用的原理是 。
(3)水的净化和软化的区别是 。
(4)硬度为1°的水是指每升水含10mgCaO或与之相当的物质(如7.1mgMgO)。若某天然水中c(Ca2+)=1.2×10—3mol/L,c(Mg2+)=6×10—4mol/L,则此水的硬度为 。
(5)若(4)中的天然水还含有c(HCO3—)=8×10—4mol/L,现要软化10m3这种天然水,则需先加入Ca(OH)2 g,后加入Na2CO3 g。
【化学——选修3:物质结构与性质】
在A、B、C三种元素中,A元素原子的价电子排布为2s22p5,B元素K、L能层上的电子数与M、N层上的电子数相同。C元素的原子序数等于A、B两元素原子序数之和,C的单质在生产生活中具有许多用途,它可在硫酸铜溶液中用电解法进行精炼。请回答以下问题:
(1)已知C元素的电负性数值为1.9,则A、C两元素的原子之间应形成 键(填“共价”或“离子”);
(2)C元素的价电子排布式为____;
(3)在A元素氢化物的水溶液中,存在有 种不同类型的氢键;
(4)SO42—中S原子的杂化轨道类型是____,SO42—的立体构型是____;
(5)一种铜金合金晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为_______;该晶体中,原子之间的作用力是________;
(6)在A、B两元素所形成晶体的晶胞中,位于六面体顶点 和面心上的元素为 (填具体的元素符号)。
和面心上的元素为 (填具体的元素符号)。

 够水解生成化合物B的有 种。这其中核磁共振氢谱图有四组不同类型峰的同分异构体的结构简式为 。
够水解生成化合物B的有 种。这其中核磁共振氢谱图有四组不同类型峰的同分异构体的结构简式为 。 粤公网安备 44130202000953号
粤公网安备 44130202000953号