2022年山东省潍坊市中考化学试卷
据《礼记》记载,西周时期已有相当丰富的酿酒经验和完整的酿酒技术规程。下列酿酒过程中只发生物理变化的是( )
| A. |
“糖化”:将淀粉水解为葡萄糖 |
| B. |
“发酵”:将葡萄糖转化为酒精 |
| C. |
“蒸馏”:根据沸点不同分离得到白酒 |
| D. |
“窖藏”:封存白酒产生具有醇厚香味的物质 |
规范的操作方法是实验安全和成功的保障。下列实验操作正确的是( )
| A. |
|
B. |
|
| C. |
|
D. |
|
2022年6月5日是第51个世界环境日,主题是“共建清洁美丽世界”。下列做法不符合这一理念的是( )
| A. |
垃圾分类回收 |
B. |
露天焚烧作物秸秆 |
| C. |
煤炭添加固硫剂 |
D. |
合理施用化肥农药 |
日前,金属材料顶级期刊《Acta材料》刊登我国科学家成功研制用于外太空核反应堆的高强韧钼合金。钼元素在元素周期表中的信息如图所示。下列说法错误的是( )

| A. |
钼属于金属元素 |
| B. |
钼的原子序数是42 |
| C. |
钼的相对原子质量为95.96g |
| D. |
钼合金比钼硬度大、强度高 |
下列溶液的pH最大的是( )
| A. |
使石蕊试液显红色的溶液 |
| B. |
使酚酞试液显红色的溶液 |
| C. |
使石蕊试液显紫色的溶液 |
| D. |
使酚酞试液显无色的溶液 |
逻辑推理是化学学习中常用的一种思维方法。以下推理正确的是( )
| A. |
酸雨的pH<7,则pH<7的降雨一定是酸雨 |
| B. |
阴离子带负电荷,则带负电荷的粒子一定是阴离子 |
| C. |
化学反应伴随能量变化,则食物的腐烂过程一定伴随能量变化 |
| D. |
活泼金属能和稀盐酸反应放出气体,则能和稀盐酸反应放出气体的一定是活泼金属 |
2022年5月10日,中国科学家发现的新冠治疗新药“千金藤素”获得国家发明专利授权,千金藤素的化学式为 。下列有关千金藤素的叙述正确的是( )
| A. |
千金藤素属于有机化合物 |
| B. |
千金藤素由83个原子构成 |
| C. |
千金藤素是由碳、氢、氮、氧原子构成的 |
| D. |
千金藤素中氢元素和氧元素质量比为 |
(不定项)氢气和氧气在Pd基催化剂表面可反应生成过氧化氢,其微观示意图如图所示。下列说法正确的是( )

| A. |
该过程不遵循质量守恒定律 |
| B. |
生成过氧化氢的微观过程的顺序是④③①② |
| C. |
过程③中,结构被破坏的分子是氧分子 |
| D. |
该反应的化学方程式为 |
(不定项)我国化学家侯德榜创立的联合制碱法促进了世界制碱技术的发展。如图是反应过程涉及到的 、 、 和 四种物质的溶解度曲线。下列有关说法错误的是( )
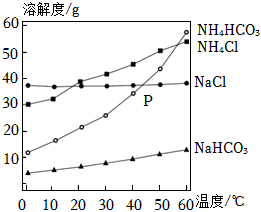
| A. |
30℃时将等质量的 和 分别配制成饱和溶液,所得溶液质量 大于 |
| B. |
在20℃时将30g 加入50g水中充分搅拌后得到 的饱和溶液 |
| C. |
与 的溶解度曲线相交于p点,该温度下两溶液溶质的质量分数相等 |
| D. |
将60℃时四种物质的饱和溶液降温到10℃析出晶体最多的是 |
(不定项)利用如图装置探究燃烧的条件。试管①中充满氮气,试管②、③中充满氧气,升温至40℃,仅观察到②中的白磷燃烧。下列叙述错误的是( )

| A. |
对比①、③可验证燃烧需要氧气 |
| B. |
试管②中白磷燃烧产生大量白雾 |
| C. |
对比②、③可得出红磷的着火点比白磷高 |
| D. |
图中小气球有密闭装置、缓冲气压的作用 |
(不定项)铁及其化合物用途广泛。部分含铁物质的分类与相应化合价关系如图所示。下列推断合理的是( )

| A. |
铁锈的主要成分是b |
| B. |
a在氧气中燃烧可得到e |
| C. |
a与稀硫酸发生反应可制得d |
| D. |
高温条件下,用 还原e可得到a |
(不定项)向 和 的混合溶液中加入一定量 粉,充分反应后过滤,向滤渣中滴加稀盐酸,有气泡冒出。下列说法正确的是( )
| A. |
滤渣中一定有 |
B. |
滤渣中一定有 和 |
| C. |
滤液中可能只有 |
D. |
滤液中可能存在 |
(不定项)向一定质量的 溶液中滴加一定质量的 溶液,反应一段时间后改为滴加 溶液,当恰好不再产生沉淀时,再滴加稀盐酸至沉淀消失。反应过程中产生沉淀的质量与加入物质的质量关系如图所示。下列说法错误的有( )
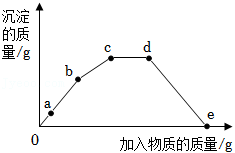
| A. |
a点溶液中溶质只有 |
| B. |
c﹣d段发生反应的化学方程式为 |
| C. |
整个过程溶液中的溶质种类最多含有2种 |
| D. |
d﹣e段有气泡产生 |
2022年北京冬奥会向世界完美展现了“绿色奥运,科技奥运,人文奥运”的理念。请完成下列问题。
(1)火炬“飞扬”采用氢气作燃料,实现了碳的“零排放”,燃烧的化学方程式为 ;国家速滑馆“冰丝带”采用最先进的二氧化碳跨临界直冷制冰技术,保持二氧化碳化学性质的最小微粒是 ;我国自主研发的锂离子动力电池,可以在极寒环境下为新能源汽车提供强劲动能,画出锂离子的结构示意图 。
(2)颁奖服和比赛服也将“科技奥运”呈现得淋漓尽致。颁奖服内胆使用了第二代石墨烯发热材料,石墨烯属于 (填“单质”或“化合物”);制作比赛服的合成纤维和聚氨酯材料属于 (填“有机合成”或“复合”)材料。
(3)开幕式采用24节气倒计时。24节气是中国的传统历法文化,“小满不满,麦有一险”提示我们需要在小满季节,及时为小麦补充充足的水分和 (填“氮”“磷”或“钾”)肥,以提高小麦的产量和质量。
化学是一门以实验为基础的科学。请根据下列实验装置完成相关问题。
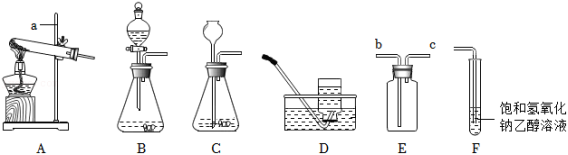
(1)写出仪器a的名称 。
(2)写出利用A装置制取氧气的化学方程式 ,基本反应类型是 。用D装置收集氧气有下列操作步骤:①将导管伸入集气瓶口,气体进入瓶中。②将装满水的集气瓶倒置在水槽中。③当气体收集满时,用毛玻璃片盖住瓶口,将集气瓶移出水槽正放在桌上。正确的操作顺序是 (填编号)。
(3)制取二氧化碳时,要获得平稳气流,最佳发生装置是 (填装置序号),用E装置检验气体集满的方法是 。
(4)将干燥纯净的二氧化碳通入装置F,可观察到澄清的溶液变浑浊,原因是 (已知:20℃时,氢氧化钠在乙醇中的溶解度为17.3g,而碳酸钠在乙醇中几乎不溶解)。
2022年4月16日,神舟十三号载人飞船成功返回地面,圆满完成任务。氧气和水是保障航天员生命的重要物质。如图为核心舱环控生保半封闭系统工作原理示意图。请分析过程,回答下列问题。
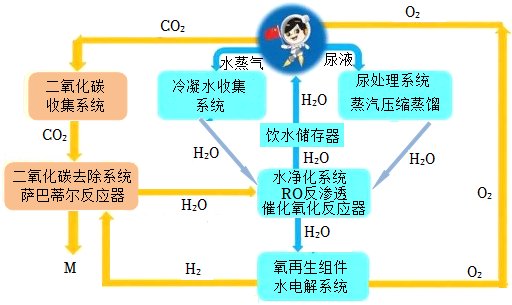
(1)从微观角度分析液态水与气态水的区别是 。
(2)通过环控生保系统得到的饮用水为软水。水净化系统在沉降过程中,可用明矾作絮凝剂,其化学式为 ,n的值为 ,生活中常用 区分硬水和软水。
(3)二氧化碳收集系统中的分子筛表面布满孔穴,结构类似于活性炭,具有 作用。
(4)早期空间站内二氧化碳可用超氧化钾( )吸收,生成碳酸钾和氧气,该反应的化学方程式是 。萨巴蒂尔反应器内,在温度570~580K和钌作催化剂的作用下便可生成水和M(M是最简单的有机物),试写出萨巴蒂尔反应器中发生反应的化学方程式 ,该技术的优点是 。
某兴趣小组利用“盐酸、硫酸铜、氢氧化钠、碳酸钠、硝酸钾”五种溶液对“复分解反应发生的条件”进行再探究。
【知识回顾】(1)回忆向滴有酚酞试剂的氢氧化钠溶液中滴加稀盐酸的实验。
(2)观察两者反应的微观示意图(图1),该反应过程没有变化的微粒是 ,两者反应的微观实质是溶液中的 。
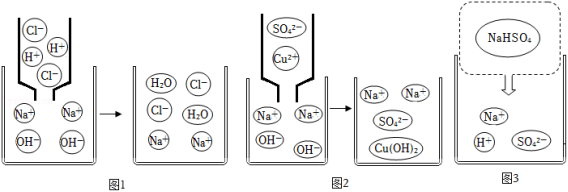
【实质再探】(1)向氢氧化钠溶液中滴加硫酸铜溶液反应的化学方程式是 ,图2是二者反应的微观示意图,两者反应的实质是溶液中的 。
(2)向碳酸钠溶液中滴加稀盐酸,产生大量气泡,实质是溶液中 反应生成了水和二氧化碳气体。
【归纳小结】复分解反应发生的微观实质是溶液中的 。
【拓展应用】(1)将碳酸钠溶液和硝酸钾溶液混合没有发生变化,分析两者不发生反应的原因是 。
(2)图3是硫酸氢钠在水中解离的微观示意图,溶液中存在的离子是 ,滴加 (用化学式表示)溶液既能降低该溶液的酸性又能生成沉淀。
工业上常采用“盐硝联产工艺”生产高纯度食盐和硫酸钠。方法是先用火碱和烟道空气中的 为原料净化卤水(主要成分是 ,还含有少量 、 、 、 、 ),然后进一步制得高纯食盐和硫酸钠,该方法符合低碳经济发展要求。请结合流程图回答下列问题。

(1)反应器1中主要除去的离子是 (用符号表示)。
(2)脱硫塔中发生反应的化学方程式是 。
(3)反应器2中生成沉淀的化学方程式为 (写出一个即可),脱水塔的作用相当于实验室中的 (填一种基本实验操作)。
(4)如表为 和 在不同温度时的溶解度。
|
温度/℃ |
10 |
20 |
32.4 |
40 |
60 |
80 |
100 |
|
|
溶解度/g |
|
35.8 |
36.0 |
36.4 |
36.6 |
37.3 |
38.4 |
39.8 |
|
|
9.1 |
19.5 |
52.0 |
48.8 |
45.3 |
43.7 |
42.5 |
|
为提高 纯度,析硝罐中需采用 (填“升温”或“降温”)结晶方法。
(5)流程中可循环使用的物质有 。
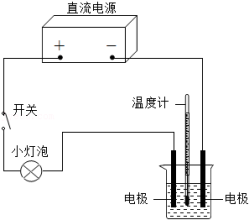
在学习人教版九年级化学下册第十单元课题1“常见的酸和碱”时,教师演示了饱和氢氧化钙溶液导电性实验,如图所示。
请根据要求回答下列问题。
实验用品:
直流电源、导线、石墨电极、灯泡、带刻度的烧杯、温度计、开关。
100mL饱和 溶液。
实验现象:
灯泡发光,两电极分别有气泡产生,烧杯内液面下降,与电源正极相连的石墨电极周围出现较多白色浑浊物,溶液温度升高。
分析:液面下降是因为水被电解。电源正极产生的气体为 (用化学式表示)。
【提出问题】溶液出现白色浑浊物的原因是什么?
【查阅资料】氢氧化钙微溶于水
【作出猜想】
猜想Ⅰ:溶液温度升高,氢氧化钙溶解度变小,溶质析出。
猜想Ⅱ: ,溶质析出。
猜想Ⅲ:石墨电极与生成气体发生反应,导致产生白色浑浊物。
【实验探究】溶液出现白色浑浊物的原因
|
实验 |
实验操作 |
实验现象 |
实验结论 |
|
① |
取相同条件下的100mL饱和 溶液于大烧杯中,加热至演示实验溶液上升的温度(温度升高约4℃)。 |
溶液中几乎无白色浑浊物。 |
猜想Ⅰ |
|
② |
将相同条件下的 mL饱和 溶液加热蒸发掉部分水(蒸发掉水的体积与演示实验减少水的体积相同)。 |
溶液中出现少量白色浑浊物。 |
猜想Ⅱ成立但不是溶液变浑浊主要原因。 |
|
③ |
向90mL相同浓度饱和 溶液中加入10mL蒸馏水,搅拌,其余条件不变,重复进行演示实验操作。 |
两电极分别有气泡冒出, 。 |
猜想Ⅲ成立且是溶液变浑浊主要原因。 |
|
④ |
使用铂电极代替石墨电极,重复进行实验③。 |
两电极分别有气泡冒出,溶液中无白色浑浊物。 |
【总结反思】
(1)白色浑浊物的成分为 (用化学式表示)。
(2)用化学方程式表示主要浑浊物的成因 。
 点燃酒精灯
点燃酒精灯 读取液体体积
读取液体体积 移走蒸发皿
移走蒸发皿 过滤粗盐水
过滤粗盐水
 粤公网安备 44130202000953号
粤公网安备 44130202000953号