2022年贵州省毕节市中考化学试卷
小丹妈妈在家做饭时,油锅突然起火,这时正确处理的方法是( )
| A. |
丢下油锅往外跑 |
| B. |
把油锅扔到屋外去 |
| C. |
接一盆水浇上去 |
| D. |
迅速关闭燃气阀门,盖上锅盖 |
对下列宏观现象的微观解释错误的是( )
选项 |
宏观现象 |
微观解释 |
A |
香水、汽油的气味不同 |
两者挥发出的微粒不同 |
B |
湿衣服在阳光下比在阴凉处干得快 |
温度升高,分子运动加快 |
C |
少量蔗糖放进水中后,很快就“消失”了 |
蔗糖分子逐步向水里扩散 |
D |
氧气在加压下可装入容积为 的钢瓶中 |
压强增大,分子本身变小 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
测体温,防疫情。某额温计的红外温度传感器所用材料含有钽酸锂( ),其中锂元素( )的化合价为 、钽元素( )在周期表中的信息如图。下列有关说法错误的是( )

| A. |
元素锂、钽均属于金属元素 |
| B. |
钽酸根离子可表示成
|
| C. |
钽的相对原子质量为 |
| D. |
钽原子的核外电子数为 |
“庄稼一枝花,全靠肥当家。”下列关于碳酸铵、氯化铵、硫酸钾和磷矿粉四种化肥鉴别的方案及结论,错误的是( )
| A. |
通过直接观察固体颜色就可以鉴别出磷矿粉 |
| B. |
取样溶解后加入硝酸钡溶液能鉴别出硫酸钾 |
| C. |
与熟石灰混合研磨后有两种化肥能闻到氨味 |
| D. |
只用氢氧化钡溶液可将前三种化肥鉴别出来 |
化学学习小组对某工业废水进行实验探究,部分过程如下:

下列有关说法正确的是( )
| A. |
步骤①置换出 两种单质 |
| B. |
操作a需要漏斗、酒精灯等仪器 |
| C. |
实验能探明三种金属活动性强弱 |
| D. |
步骤④加盐酸是为了除去 粉 |
室温时,向 某固体中分批次加入水,充分搅拌,结果如图所示(保持温度不变):

室温时该固体的溶解度可能是( )
| A. |
|
B. |
|
C. |
|
D. |
|
已知 溶液显中性。向 与盐酸混合溶液中逐滴滴加 溶液,边加边搅拌,用 计测得混合溶液 的变化如图。下列相关叙述正确的是( )

| A. |
实验中 个数保持不变 |
| B. |
AB对应反应为中和反应 |
| C. |
BC对应反应无明显现象 |
| D. |
CD表明 属于碱 |
化学使生活更美好。回答下列问题:
(1)我国提出争取在2030年前实现碳达峰,2060年前实现碳中和。“碳达峰”“碳中和”中的“碳”指的是_____(填选项序号)。
a.碳元素
b.碳原子
c.碳单质
d.二氧化碳
(2)如图是我国制定的某类材料回收标志,这类材料属于_____(填“无机化合物”或“有机化合物”)。

“五色新丝缠角粽,菖蒲酒美清尊共。”下表是某品牌粽子的营养成分表(其中“钠”由 提供):
项目 |
能量 |
蛋白质 |
脂肪 |
碳水化合物 |
钠 |
每 |
|
|
|
|
|
人体所需六大基本营养素中,“项目”里没有涉及的有_____(填名称)和水。
A~F是初中化学常见的物质,它们之间的转化关系如图所示,图中“一”表示两种物质能发生化学反应,“→”表示两种物质间的转化关系。
已知:
 (三者均为氧化物、反应前后各元素化合价均未改变),D广泛用于玻璃、造纸、纺织和洗涤剂的生产等,农业上可用E、F等配制成具有杀菌作用的波尔多液作为农药使用。回答下列问题:
(三者均为氧化物、反应前后各元素化合价均未改变),D广泛用于玻璃、造纸、纺织和洗涤剂的生产等,农业上可用E、F等配制成具有杀菌作用的波尔多液作为农药使用。回答下列问题:
(1)D的化学式为_____。
(2)组成元素与B完全相同的另一种物质是_____(填化学式)。
(3)如果“C→B”为置换反应,该反应的化学方程式为__________,其中C物质发生_____(“氧化”或“还原”)反应。
(4)为鉴定F溶液中的金属离子,某同学进行了如下实验:
F溶液 蓝色沉淀
蓝色沉淀 沉淀溶解、得到蓝色溶液
沉淀溶解、得到蓝色溶液
上述蓝色沉淀溶解反应的化学方程式是__________。

实验室常用下列A、B、C装置制取气体,D、E装置收集气体。
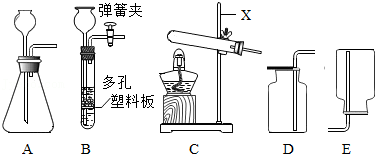
回答下列问题:
(1)C装置中仪器X的名称是_____。
(2)用石灰石和稀盐酸作原料制取二氧化碳,反应的化学方程式为__________,选用的收集装置为_____(填代号,下同)。
(3)用锌粒和稀硫酸作原料制取氢气,为实现气体随开随用、随关随停,选用的制取装置为_____
(4)实验室用醋酸钠和碱石灰(主要成分是 和 )固体混合物作原料、在加热条件下制取 ,选用的制取装置为_____,收集装置为_____。
(5)如图所示装置用于收集某干燥的气体,下列气体中能用它收集的是_____(填选项序号)。
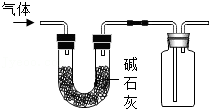
a.
b.
c.
d.
一种“贴身暖宝宝”的使用说明书如下,某化学兴趣小组围绕袋内物质展开探究。
品名:XX牌贴身暖宝宝 成分:袋内物质:铁粉、水、活性炭、食盐等 内袋材料:微孔透气无纺布 外袋材料:不透气塑料 用法:临使用前,打开外袋取出内袋,直接贴在衣服上,打开外袋后保持温暖12小时 |
【提出问题】袋内是否含有铁粉?
【进行实验】①取出袋内粉末于滤纸上,与磁铁充分接触。②将少量磁铁吸出的粉末加入足量稀硫酸中。
【收集证据】磁铁吸出的粉末与稀硫酸剧烈反应得到浅绿色溶液、同时_____。
【得出结论】袋内含有铁粉。
【做出猜想】被磁铁吸出的铁粉能在空气中燃烧。
【获取事实】将少许铁粉撒在酒精灯火焰上,铁粉立即剧烈燃烧、火星四射。
【反思交流】铁粉燃烧反应的化学方程式为__________。铁丝不能而铁粉能在空气中燃烧的原因是__________。
【拓展探究】用不同燃料测定空气里氧气的含量:分别在图甲所示装置的燃烧匙内放置铁粉、红磷(均足量),电加热引燃。氧气含量随时间变化情况如图乙、图丙:

(1)温度传感器显示,实验过程中瓶内温度均_____(填“升高”或“降低”)。
(2)待铁粉熄灭并恢复至室温后,打开弹簧夹,进入瓶内的水约占原水面上方空间体积的_____。
(3)分析图乙、图丙可知,实验中消耗氧气更彻底的是_____(填“铁粉”或“红磷”,下同),消耗氧气速率更快的是_____。
我国科学家在人工合成淀粉领域取得了突破性进展,其基本变化过程为“ 。”淀粉中C、H元素的质量之比为 _____,C的质量分数为_____ (计算结果保留一位小数,下同)。
 检查装置的气密性
检查装置的气密性 滴加液体
滴加液体 准备收集气体
准备收集气体 加入固体粉末
加入固体粉末
 粤公网安备 44130202000953号
粤公网安备 44130202000953号