2019年湖北省宜昌市中考化学试卷
下列人体内的一些液体和排泄物的正常pH范围中,酸性最强的是( )
A.血浆(7.35~7.45)B.胃液(0.9~1.5)
C.唾液(6.6~7.1)D.胆汁(7.1~7.3)
打赢蓝天保卫战,我们在行动。下列做法不属于防治大气污染措施的是( )
A.大力削减燃煤污染B.深化治理工业污染
C.精准管控扬尘污染D.严格控制噪音污染
保“舌尖上的安全”。下列做法符合食品安全要求的是( )
A.亚硝酸钠作调味剂B.碳酸钙用作补钙剂
C.工业酒精勾兑白酒D.地沟油提炼食用油
如图是碳铵化肥包装袋上的部分信息。关于该化肥的说法错误的是( )

A.属于复合肥料
B.主要含有四种元素
C.不宜与碱性物质混合使用
D.储存和运输时,不宜受潮或曝晒
为探究二氧化碳能否和水反应,用四朵石蕊溶液染成紫色的干燥小花完成如图四个实验。实验I、Ⅳ中小花变红,实验Ⅱ、Ⅲ中小花不变色。下列说法不正确的是( )
A.实验Ⅰ、Ⅱ说明醋酸可以使小花变红
B.实验Ⅲ说明二氧化碳不能使小花变红
C.实验Ⅱ、Ⅲ、Ⅳ说明二氧化碳能与水发生化学反应
D.上述实验说明二氧化碳和醋酸具有相似的化学性质
危险化学品泄漏或爆炸事件常给我们敲响安全警钟,操作不当就会存在安全隐患。下列做法不正确的是( )
A.点燃氢气,提前验纯B.燃气泄漏,点火检查
C.矿井作业,注意通风D.油库重地,严禁烟火
如图是某元素原子的结构示意图。下列说法不正确的是( )

A.图中x=34
B.该元素位于元素周期表第四周期
C.该元素属于金属元素
D.该元素原子易得电子形成阴离子
下列宏观现象和微观解释不一致的是( )
A.水蒸发变成水蒸气﹣﹣水分子体积变大
B.6000L氧气通过加压能装入40L的钢瓶中﹣﹣分子之间有间隔
C.一滴水中大约有1.67×1021个水分子﹣﹣分子的质量和体积都很小
D.湿衣服在阳光下比在阴凉处干得更快﹣﹣温度越高,分子运动越快
如图是硫在空气和氧气中燃烧的实验。下列说法不正确的是( )

A.氧气含量越多硫燃烧越剧烈
B.硫在氧气中燃烧发出蓝紫色火焰
C.瓶底的水可以吸收生成的有害气体
D.硫在空气和氧气中燃烧的生成物不同
硅是重要的半导体材料。X+H2 3HCl+Si(高纯)是工业制硅流程中的一个化学反应方程式,则X为( )
A.SiClB.SiCl3C.SiHCl3D.SiH2Cl3
下列实验方法能够达到实验目的是( )
实验目的 |
实验方法 |
|
A |
除去氢气中混有的少量水蒸气 |
将混合气体通过足量浓硫酸 |
B |
除去生石灰中混有的少量碳酸钙 |
加足量水,过滤 |
C |
除去氮气中混有的少量氧气 |
将混合气体通过灼热的炭层 |
D |
除去氯化钙溶液中混有的少量氯化钠 |
加入足量碳酸钠溶液,过滤 |
A.AB.BC.CD.D
下列归纳总结完全正确的一组是( )
A.燃烧的条件 |
B.有机合成材料 |
①可燃物 ②氧气(或空气) ③温度达到100℃ |
①合金 ②合成纤维 ③合成橡胶 |
C.化学之最 |
D.元素与健康 |
①汞﹣熔点最低的金属 ②碳﹣地壳中含量最多的元素 ③金刚石﹣天然存在的最硬物质 |
①缺氟﹣龋齿 ②缺钙﹣﹣佝偻病 ③缺碘﹣甲状腺肿大 |
A.AB.BC.CD.D
一氧化碳在工业上有重要作用。
(1)作燃料:一氧化碳在空气中燃烧的化学方程式 ;
(2)作还原剂:一氧化碳还原氧化铜的化学方程式 。
下列图中 ”
” ”和
”和 ”分别表示不同元素的原子。
”分别表示不同元素的原子。
(1)表示混合物的有 (填字母序号,下同);
(2)表示单质的有 ,可以表示氧化物的有 。
下表是通过实验测得两种固体物质在不同温度时的溶解度,如图是市售果味型汽水配料表。请据图回答问题:
温度/℃ |
0 |
20 |
40 |
60 |
80 |
|
溶解度/g |
氯化钠 |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
氯化钾 |
27.6 |
34.0 |
40.0 |
45.5 |
51.1 |
|
(1)20℃时,氯化钠的溶解度是 g。
(2)40℃时,将50g氯化钾放入100g水中,充分搅拌,所得溶液的质量为 g;
(3)60℃时,将45g氯化钠和45g氯化钾分别放入100g水中充分搅拌,所得氯化钠溶液溶质的质量分数 氯化钾溶液溶质的质量分数(填“<”或“>”或“=”);
(4)打开如图所示果味型汽水瓶盖时,观察到汽水中有大量气泡产生,结合配料成分可知,此时汽水是 的饱和溶液(填配料表中的具体物质)。

下列是实验室常用仪器,据图回答问题:

(1)认识仪器:仪器A的名称是 ;
(2)量取液体:量取5mL水,需要选择的仪器是 (填字母序号,下同);
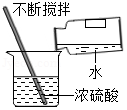
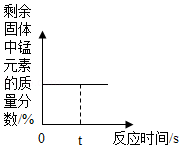
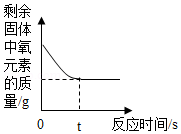
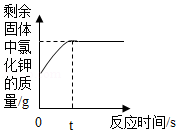
(3)制取气体:实验室用高锰酸钾制取氧气的化学方程式是 ,用该原理制取氧气时,除上述仪器外,还缺少一种仪器的名称是 ,用向上排空气法收集氧气时,检验氧气是否收集满的方法是 。
(4)分离物质:实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式是 ,充分反应后,分离剩余的物质需进行过滤,过滤需选择的仪器是 。
构建知识网络是一种重要的学习方法。如图是初中化学常见的单质、氧化物、酸、碱、盐五种不同类别的物质与CO2的知识网络图,“一”表示相连的两种物质能发生化学反应,“→”表示一种物质一步转化成另一种物质(部分反应条件未标出)。
请回答:
(1)A的化学式是 ,E的化学式是 ;
(2)C﹣D的化学方程式是 。

金属的用途与性质密切相关。

铜 |
铝 |
|
密度/(g•cm﹣3) |
8.92 |
2.70 |
地壳中含量(质量分数/%) |
0.007 |
7.73 |
导电性(以银的导电性为100做标准) |
|
|
图2
(1)图1所示赤铁矿的主要成分是 (填化学式);
(2)家用电线常用铜制,但在高压远距离输电中,常用铝代替铜,请根据图2的信息分析,其原因是 ;
(3)在空气中,铝具有很好的抗腐蚀性,其原因用化学方程式表示为 ;
(4)为探究铁、铜的金属活动性,分别将铁丝、铜丝插入稀硫酸中(图3所示),说明铁比铜的金属活动性更强的实验现象是 ,反应的化学方程式是 。
(5)将一定量铝、铜粉末混合物加入硝酸银溶液中,充分反应后过滤,滤液为蓝色。则滤渣中一定含有 (填化学式,下同),滤液中溶质的组成可能是 。
爱护水资源,落实长江大保护。
(1)树立保护水体意识。下列做法正确的有 ;
A.节约用水 B.工业用水重复利用 C.洗衣污水集中处理
(2)掌握水的净化方法。日常生活中,我们常使用活性炭制作净水器滤芯,是利用活性炭的 性,为降低水的硬度,我们常选择的方法是 ;
(3)学习净水材料制备。高铁酸钾(K2FeO4)是一种新型非氯高效水处理消毒剂,主要用于饮用水处理,制备高铁酸钾的一种模拟流程如图(部分反应条件未标出):
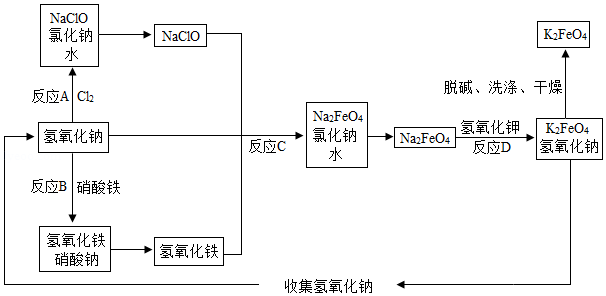
①K2FeO4中铁元素的化合价为 ;
②反应A、B、C、D中属于复分解反应的是 ;
③反应A的化学方程式是 。
利用物质的性质能帮助我们开展科学探究。
判断化学变化
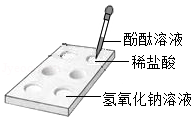
如图,在稀盐酸和氢氧化钠溶液中分别滴加几滴无色酚酞溶液,观察到能使无色酚酞变红的物质是 。
稀盐酸与氢氧化钠溶液能否发生化学反应呢?智慧小组同学开展了如下探究活动,请将横线部分填写完整。
编号 |
实验操作 |
实验现象 |
实验分析 |
实验一 |
取一定量稀盐酸于小烧杯中,加入氢氧化钠溶液 |
无明显现象 |
稀盐酸与氢氧化钠溶液混合后有新物质生成 |
实验二 |
取实验一所得溶液少量于试管中,滴入几滴无色酚酞溶液 |
无明显现象 |
|
实验三 |
取实验一所得溶液少量, |
|
实验结论:稀盐酸和氢氧化钠溶液反应的化学方程式为 。
探究溶液成分
有一瓶无色溶液,可能含有硝酸镁、硫酸钾、氯化钠中的一种或几种溶质,奋进小组同学设计了如图实验方案:
(1)若X为氢氧化钠,当步骤一和步骤二均无明显现象、步骤三有白色不溶物生成时,则原无色溶液中一定不含 (填溶质化学式,下同);
(2)若X为氯化钡,当步骤一和步骤三有白色不溶物生成、步骤二无明显现象时,则原无色溶液中一定含有
,步骤三一定发生反应的化学方程式是 (任写一个):
(3)若X为氢氧化钡,且无色溶液中存在上述三种溶质时,则:
①步骤一的现象是 ;
②步骤二证明原无色溶液中含有硝酸镁的化学方程式是 ;
③混合物C的溶液中存在的溶质最多有 种。


 粤公网安备 44130202000953号
粤公网安备 44130202000953号