2016年广西贺州市中考化学试卷
某有机物与氧气充分反应,产物只有二氧化碳和水,则该有机物一定含有的元素是( )
A.C、OB.H、OC.C、HD.C、H、O
在做《溶液的形成》这一课的演示实验时,老师先往一试管中加入1~2小粒高锰酸钾,然后加入5mL 的水,接下来的操作正确的( )
A. B.
B.
C. D.
D.
下列关于CO2性质的信息,组合正确的是( )
①可以助燃 ②能使澄清石灰水变浑浊 ③可溶于水,但不能与水反应 ④可供绿色植物进行光合作用.
A.②④B.①③C.①②D.②③
夏天的傍晩,小明和爸爸妈妈去散步前总喜欢往身上喷点花露水,蚊子闻到花露水的气味就不敢靠近他们了,这一现象说明( )
A.分子之间有间隙B.分子在不断运动
C.分子由原子构成D.分子的质量较大
下列说法或做法不正确的是( )
A.石油中主要含碳、氢两种元素
B.小明看见邻居家着火,立即拨打119
C.可燃物的燃烧,需要空气(或氧气)、温度达到着火点
D.煤气泄漏时,马上打开抽风机以利于煤气排出
如图是某反应的微观示意图,以下说法正确的是( )

A.该反应有单质生成
B.如图表示的微观变化过程中共有三种分子
C.分子是化学变化中最小粒子
D.参加反应的“●●”分子与“○○”分子的个数比为1:3
下列有关溶液的说法正确的是( )
A.溶液均是无色的、透明的
B.可溶性物质溶于水时一定会放出热量
C.石灰水的溶质是石灰
D.溶液的均一性是指同一溶液各部分的性质、组成相同
下列关于碳单质的用途及原因分析的描述不正确的是( )
用途 |
原因分析 |
|
A |
石墨可用作电极 |
石墨可导电 |
B |
金刚石可用来刻画玻璃 |
金刚石硬度很大 |
C |
活性炭可用于消毒面具 |
活性炭具有吸附性 |
D |
焦炭用于冶金工业 |
碳具有氧化性 |
A.AB.BC.CD.D
下列有关说法正确的是( )
A.铁在潮湿的环境中比在干燥的环境中更容易生锈
B.铝制品不用涂任何保层来防腐,因为铝不与空气反应
C.镁在氧气中燃烧,发出耀眼白光,生成黑色固体
D.我国的矿物储量比较丰富,所以废旧金属直接扔掉,没有必要回收
如图是某件衣服标签的部分内容,以下说法错误的是( )

A.羊毛是天然纤维
B.涤纶是合成纤维
C.可用灼烧的方法来区分羊毛和涤纶
D.合成纤维的吸水性和透气性要比天然纤维的好
绿茶中含有儿茶素(化学式为 C15H14O6H2O),关于儿茶素管说法不正确的是( )
A.儿茶素中含有3种元素
B.儿茶素中碳的质量分数为58.4%
C.儿茶素分子中碳和氢的原子个数比为15:14
D.儿茶素是一种有机物
下列物质在水溶液中能大量共存的是( )
A.NaCl Na2CO3 H2SO4
B.FeCl3 Na2SO4 KOH
C.BaCl2 AgNO3 Na2CO3
D.CuSO4 KNO3 Na2SO4
在“一定质量分数的氯化钠溶液的配制”和“粗盐中难溶性杂质的去除”两个实验中都能使用到的仪器是( )
A.烧杯、玻璃棒、托盘天平、量筒
B.烧杯、玻璃棒、托盘天平、试管
C.托盘天平、量筒、烧杯、漏斗
D.蒸发皿、酒精灯、烧杯、铁架台
把 CaCO 3、NaCl、MgCl 2三种固体物质组成的混合物逐一分离所需要的试剂依次是( )
A.H 2O NaOH HClB.H 20 KOH HCl
C.H 2O NaOH H 2S0 4D.H 20 KOH H 2S0 4
下列图象不能正确反映其对应变化关系的是( )
A.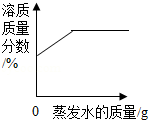 某温度下将一定量接近饱和的KNO3溶液恒温蒸发水分
某温度下将一定量接近饱和的KNO3溶液恒温蒸发水分
B. 一定质量的红磷在密闭容器中燃烧
一定质量的红磷在密闭容器中燃烧
C.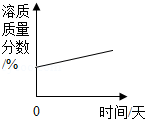 将一瓶浓硫酸露置于空气中
将一瓶浓硫酸露置于空气中
D.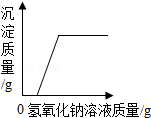 向一定质量的氯化镁和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液
向一定质量的氯化镁和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液
下列对部分化学知识的归纳完全正确的( )
A |
化学与生活:①生活中常用加热煮沸的方法软化硬水 ②氧气用于医疗急救 ③农业上用石灰乳和硫酸铜制波尔多液 |
B |
化学与环境:①焚烧植物秸杆不会造成空气污染 ②PM2.5是造成雾霾天气的元凶之一 ③使用可降解塑料可减少“白色污染” |
C |
化学与安全:①皮肤沾上浓硫酸一先用水冲洗,再涂稀醋酸 ②实验时碰倒酒精灯着火一用湿抹布盖灭 ③冬天用煤炉取暖一保证室内通风 |
D |
化学与健康:①人体缺铁会引起贫血症 ②可用硫磺薫蒸笋干使之颜色更好看 ③制作糕点过程中加入适量的碳酸氢钠,使糕点松软可口 |
A.AB.BC.CD.D
某同学就测定Na2CO3和NaCl固体混合物中NaCl的质量分数,分别取mg样品,按下列方案进行试验,合理的是( )
A.与足量稀盐酸充分反应,用排水法收集到VmL气体
B.与足量BaCl2溶液充分反应,将沉淀过滤、洗涤、干燥,得到m1 g固体
C.与足量AgNO3溶液充分反应,将沉淀过滤、洗涤、干燥,得到m2g固体
D.与足量浓盐酸充分反应,逸出的气体用NaOH固体充分吸收,固体质量增加m3g
贺州市矿产资源非常丰富,其中有色金属矿产有锡、钨、铅、锌、铜、锑等;化工原料矿产有赤铁矿、硫铁矿(主要成分:FeS2)等;建筑材料有大理石、花岗石、石灰石等.
(1)用于制作白炽灯灯丝的材料是 .
(2)如图是元素周期表中锑元素的信息,则锑的质子数为 .
(3)焊锡是锡与 的合金.
(4)可用于生产硫酸的矿石是 .
(5)天安门华表是由 做成的.

(1)现有H、O、Na、Mg、P五种元素,请根据下列要求写出由所给元素组成的物质(写化学式):
①属于金属氧化物的是 (写出两种即可).
②属于碱的是 .
(2)A、B、C三种物质的溶解度曲线如图所示,请回答:
①对于物质A而言,点P的含义为 .
②t3℃时,A、B、C三种饱和溶液中,溶质质量分数由大到小的排列为 .
③若A、B、C三种物质中有一种是易溶于水的气体,则其溶解度曲线是 .
④烧杯中有t2℃时20%的A溶液50g,要将该溶液变为同温度下的饱和溶液,至少需向烧杯中加入A物质 克.

金属在日常生活中有着广泛的用途,常见金属的活动性顺序如图:

请回答下面问题:
(1)金属活动性顺序表中的X是 元素。
(2)把一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,过了一会儿,观察到的现象有 ,该反应的化学方程式为 。
(3)向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间的变化情况如图所示,图中B点溶液中含有的溶质有 。

(1)盐酸、硫酸是常见的两种酸。①打开装浓盐酸的试剂瓶时,瓶口出现白雾,说明浓盐酸具有 性。②用水稀释浓硫酸时, 并用玻璃棒不断搅拌即可。
(2 )如图是化肥硝酸铵包装袋上的部分说明:
①从说明上可以判断硝酸铵应具有的性质有 (填字母)。
A.易溶于水 B.撞击易爆炸 C.受热易分解
②若把硝酸铵溶于水配成溶液并用 pH试纸检测溶液酸碱性,发现常温下溶液的pH=6,则该盐溶液呈 (填“酸性”、“碱性”或“中性”)。
③硝酸铵与碱反应生成硝酸盐,写出硝酸铵与熟石灰在加热条件下反应的化学方程式 。

(1)在自来水厂取水口管道入口处设有拦污栅,此处相当于实验基本操作中的 .水厂工人在清理拦污栅的垃圾时经常发现有:①菜叶②纸皮③香蕉皮④易拉罐⑤塑料饮料瓶,其中可回收的有 (填序号).
(2)地球上总水量虽然很大,但淡水资源很少,我们必须爱护水资源,一方面要 ,另一方面要 (从"节水、防治水体污染"两个角度回答的合理答案均得分).
(3)在常温下完全电解90mL的水,正极与负极产生的气体的体积比为 ,产生氧气的质量为 克(设常温下水的密度为1g/cm 3).
A、B、C、D、E是初中常见的五种物质,其中 D是黑色固体,且与C在一定条件下反应有红色物质生成,E的固体俗称干冰。①、②、③、④的反应类型分别是复分解反应、分解反应、化合反应和置换反应。图中“一”表示两端物质间能发生反应,“→”表示物质间的转化关系,部分反应物、生成物及反应条件已略去。
请回答下列问题:
(1)写出下列物质的化学式:D ,E 。
(2)写出下列反应的化学方程式:
① ;
④ 。

据下列仪器裝置图,请回答有关问题。
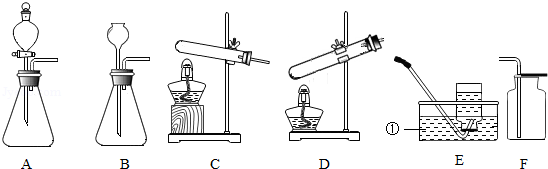
(1)图中仪器①的名称 。
(2)若实验室用高锰酸钾制取氧气,反应的化学方程式为 ,可用于该反应的气体发生装置是 (填字母序号),该装置的试管口还缺少 ,用装置F收集一瓶O2,如何检验O2是否已收集满?
(3)实验室没有大理石和石灰石,只有碳酸钠粉末和盐酸,为了顺利制取一瓶CO2气体,请你选择最佳的装置组合(填字母序号),选择该气体发生装置的理由是 。
某化学兴趣小组发现铜片在加热的条件下可以与浓硫酸反应,产生气泡并闻到刺激性气味,铜片溶解,溶液呈蓝色,请你参与实验探究。
【查阅资料】SO2是一种无色,有刺激性气味,有毒的气体。
(1)【提出问题】产生的气体是什么?
(2)【提出猜想】猜想一:SO2;猜想二:SO2和H2。
(3)你认为猜想二 (填:“正确”或“错误”)。
(4)提出问题】蓝色溶液的溶质是什么?
(5)【提出猜想】猜想一:CuSO4;猜想二:CuSO4和H2SO4。
(6)【进行实验】取一定量反应后的溶液进行稀释,并分装在A、B两支试管中,然后进行下列实验,并完成如表:
步骤 |
实验操作 |
实验现象 |
实验结论 |
步骤一 |
在试管A中加入少量的CuO粉末 |
① |
溶液中含有H2SO4 |
步骤二 |
在试管B中加入过量的NaOH溶液 |
② |
溶液中含有CuSO4 |
(7)【探究结论】通过实验,猜想二正确。
(8)写出步骤一发生反应的化学方程式: 。
(9)完成并配平方程式:□Cu+□H2SO4(浓) 。
(10)【反思评价】根据化学方程式:小王认为工业上可以用铜和浓硫酸反应大量制取硫酸铜,小李认为不适宜,理由是 。
重质碳酸钙粉体产业为我市一大支柱产业,产品远销全国各地.某化学兴趣小组对粉体中碳酸钙含量进行了探究,小组成员从一包粉体产品中取出样品5.10g放入烧杯中,并逐滴加入相同浓度的稀盐酸(假设样品中的杂质不参与盐酸反应),实验测得烧杯中物质总质量与加入稀盐酸的总质量关系如表所示.
稀盐酸的总质量(g) |
10.00 |
20.00 |
30.00 |
40.00 |
50.00 |
60.00 |
70.00 |
烧杯中物质总质量(g) |
14.66 |
24.22 |
m |
43.34 |
52.90 |
62.90 |
72.90 |
(1)碳酸钙的相对分子质量为 .
(2)表中m= .
(3)求样品中碳酸钙的质量分数(结果保留两位小数).
 粤公网安备 44130202000953号
粤公网安备 44130202000953号