广东省珠海市高三9月摸底考试化学试卷
下列说法中正确的是
| A.医用酒精的浓度通常为95% |
| B.单质硅是将太阳能转变为电能的常用材料 |
| C.淀粉、纤维素和油脂都属于天然高分子化合物 |
| D.合成纤维和光导纤维都是新型无机非金属材料 |
等浓度的下列稀溶液:①乙酸、②苯酚、③碳酸、④乙醇,它们的PH由小到大排列正确的是
| A.④②③① | B.③①②④ |
| C.①②③④ | D.①③②④ |
下列叙述错误的是
| A.用金属钠可区分乙醇和乙醚 |
| B.用溴水可区分己烷和3--己烯 |
| C.用水可区分苯和溴苯 |
| D.用新制的氢氧化铜悬浊液可区分甲酸甲酯和乙醛 |
NA为阿伏加德罗常数,下列叙述正确的是
| A.25℃时,l L pH=13的 Ba(OH)2 溶液中含有的OH-数为0.2 NA |
| B.18g D2O中含有的质子数为9NA |
| C.Fe在少量Cl2中燃烧生成0.5 mol 产物,转移的电子数为NA |
| D.标准状况下,11.2LCCl4含有的分子数为0.5 NA |
能在无色水溶液中大量共存的一组离子是
| A.H+、Fe3+、I-、Cl- | B.Al3+、Mg2+、NO3-、Cl- |
| C.K+、Ag+、Ca2+、SO42- | D.NH4+、Na+、AlO2-、MnO4- |
关于Na2CO3和NaHCO3比较中,下列说法不正确的是
| A.NaHCO3固体受热容易分解,而Na2CO3固体受热不容易分解 |
| B.等质量的Na2CO3和NaHCO3分别与足量的盐酸反应,前者消耗盐酸的物质的量比后者多 |
| C.等物质的量浓度的Na2CO3和NaHCO3溶液分别滴加2滴酚酞试液,前者颜色比后者深 |
| D.Na2CO3溶液和NaHCO3溶液分别与Ba(OH)2溶液反应的离子方程式相同 |
下列应用不涉及氧化还原反应的是
| A.Na2O2用作呼吸面具的供氧剂 |
| B.工业上电解熔融状态的Al2O3制备Al |
| C.工业上利用合成氨实现人工固氮 |
| D.实验室用NH4Cl和Ca(OH)2制备NH3 |
下列陈述中,Ⅰ、Ⅱ都正确且两者间具有因果关系的一组是
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
FeCl3溶液能腐蚀Cu |
Fe的金属性强于Cu |
| B |
Na2O2使酚酞溶液变红 |
Na2O2使品红溶液褪色 |
| C |
Cl2可部分与水反应 |
用排饱和食盐水法收集Cl2 |
| D |
浓H2SO4可干燥NO和SO2 |
NO和SO2还原性都弱 |
某小组设计电解饱和食盐水的装置如下图,通电后两极均有气泡产生,下列叙述正确的是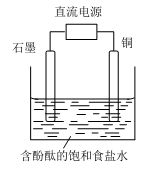
| A.铜电极附近观察到黄绿色气体 | B.石墨电极附近溶液先变红 |
| C.溶液中的Na+向石墨电极移动 | D.铜电极上发生还原反应 |
对于0.1mol•L-1Na2SO3 溶液,正确的是
| A.升高温度,溶液的pH降低 |
| B.加入少量NaOH固体,c(SO32- )与c(Na+ )均增大 |
C.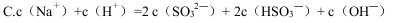 |
D. |
已知短周期元素R、W、X、Y、Z的原子序数依次增大,其氢化物中上述元素的化合价如下表,下列说法正确的是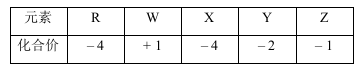
| A.离子还原性:Y2― < Z― | B.离子半径W+ > Z― |
| C.气态氢化物稳定性:RH4 < XH4 | D.酸性:H2YO4 < HZO4 |
莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是
| A.分子式为C7H6O5 |
| B.分子中只含有羟基和羧基两种官能团 |
| C.可发生加成和取代反应 |
| D.在水溶液中羟基和羧基均能电离出氢离子 |
黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)==K2S(s)+N2(g)+3CO2(g) ΔH=" x" kJ·mol-1
已知:碳的燃烧热 ΔH1=" a" kJ·mol-1①
S(s)+2K(s)==K2S(s) ΔH2=" b" kJ·mol ②
2K(s)+N2(g)+3O2(g)==2KNO3 (s) ΔH3=" c" kJ·mol-1③
则x为
| A.3a+b-c | B.c +3a-b | C.a+b-c | D.c+a-b |
在密闭容器中进行反应CH4(g)+H2O(g) CO(g)+3H2(g)ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断不正确的是
CO(g)+3H2(g)ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断不正确的是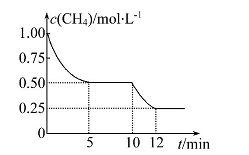
| A.10 min时,改变的外界条件可能是升高温度 |
| B.0~10 min内,v(H2)=0.15 mol·L-1·min-1 |
| C.恒温下,缩小容器体积,一段时间内v(逆)>v(正) |
| D.12 min时,反应达平衡的本质原因是气体总质量不再变化 |
下列有关实验装置的说法中正确的是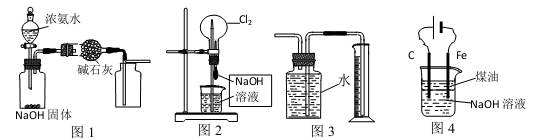
| A.图1装置可制取干燥纯净的NH3 |
| B.图2装置可以完成“喷泉”实验 |
| C.图3装置可测量Cu与浓硝酸反应产生气体的体积 |
| D.图4装置可用于实验室制备Fe(OH)2 |
已知:A为淡黄色固体,E、X常温下为气体,A、B、C、D含有相同的金属离子,其转化关系如下图(部分产物已略去)。
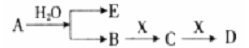
请回答下列问题:
(1)B中所含化学键的类型是___________。
(2)常温常压下,7.8g A与足量的水充分反应放出热量a kJ,写出该反应的热化学方程式 。
(3)①C也可转化为B,写出该转化的化学方程式____________。
②B与D反应的离子方程式为______________。
(4)将一定量的气体X通入2L B的溶液中,向所得溶液中边逐滴加入稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。
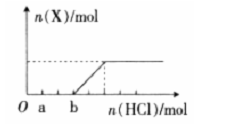
请回答:a 点溶液中所含溶质的化学式为_______,b 点溶液中各离子浓度由大到小的关系是______。
运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义。
(1)硫酸生产过程中2SO2(g)+O2(g) 2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图所示,根据图回答下列问题:
2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图所示,根据图回答下列问题:
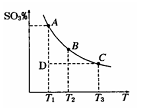
①2SO2(g)+O2(g) 2SO3(g)的△H________0(填“>”或“<”),
2SO3(g)的△H________0(填“>”或“<”),
②一定条件下,将SO2与O2以体积比2:1置于一体积不变的密闭容器中发生以上反应,能说明该反应已达到平衡的是________。
a.体系的密度不发生变化
b.SO2与SO3的体积比保持不变
c.体系中硫元素的质量百分含量不再变化
d.单位时间内转移4 mol 电子,同时消耗2 mol SO3
e.容器内的气体分子总数不再变化
(2)一定的条件下,合成氨反应为:N2(g)+3H2(g) 2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
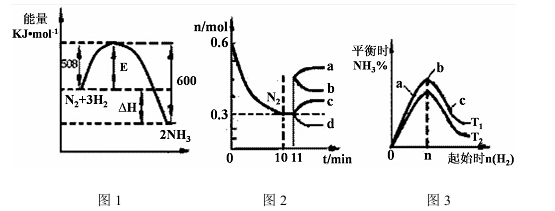
①该反应的平衡常数表达式为 ,升高温度,平衡常数 (填“增大”或“减小”或“不变”)。
②由图2信息,计算0~10min内该反应的平均速率v(H2)= ,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为 (填“a”或“b”或“c”或“d”)
③图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是 点,温度T1 T2(填“>”或“=”或“<”)
某化学兴趣小组利用废弃铝矿(含CuO、Al2O3及SiO2),模拟工业上提取铝的工艺,设计如下图所示的简单操作流程:

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:

回答下列问题:
(1)滤渣主要成分的化学式为_________。
(2)灼烧Al(OH)3时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有_______(填仪器名称)。
(3)溶液Y中要加入稍过量原料A,原料A的化学式是_______。
(4)操作流程中③的离子方程式为_____________。
(5)铝电池性能优越,Al—Ag2O电池可用作水下动力电源,其原理如图所示:
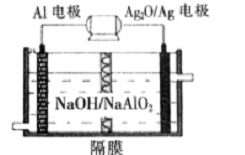
请写出该电池正极反应式 。
从樟科植物枝叶提取的精油中含有下列甲、乙两种成分:
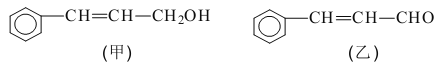
(1)乙中所含官能团的名称为 。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
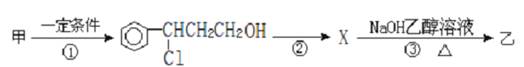
设计步骤①的目的是 ;指出①的反应类型 。
③反应的化学方程式为 (注明反应条件)。
(3)欲检验乙中的含氧官能团,选用下列的一种试剂是__________。
| A.溴水 | B.酸性高锰酸钾溶液 | C.溴的CCl4溶液 | D.银氨溶液 |
(4)乙经过氢化、氧化得到丙( 。丙的同分异构体中,既有苯环,又有羧基的共有 种。任意写出一种同时符合下列要求的丙的同分异构体结构简式_____________。
。丙的同分异构体中,既有苯环,又有羧基的共有 种。任意写出一种同时符合下列要求的丙的同分异构体结构简式_____________。
①能发生银镜反应;
②能与FeCl3溶液发生显色反应;
③核磁共振氢谱图上产生4个吸收峰。
在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3 + CO2 + NaCl + H2O ="=" NH4Cl + NaHCO3↓,依据此原理,欲制得碳酸钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
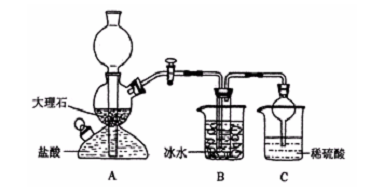
(1)A装置中所发生反应的离子方程式为: 。
C装置中稀硫酸的作用为: 。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
| |
0℃ |
10℃ |
20℃ |
30℃ |
40℃ |
50℃ |
| NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
| NaHCO3 |
6.9 |
8.1 |
9.6 |
11.1 |
12.7 |
14.5 |
| NH4Cl |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
参照表中数据,请分析B装置中使用冰水是因为 。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在 装置之间(填写字母)连接一个盛有 的洗气装置,其作用是 。
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号