北京市朝阳区高一下学期期末考试化学卷
下列关于海水资源的说法中,不正确的是
| A.海带中含有碘元素 |
| B.海水中含有大量氯元素 |
| C.蒸馏法是海水淡化的主要方法之一 |
| D.开发海水资源可以不考虑是否对环境有污染 |
下列原子序数所对应的元素组中,两者可形成离子键的是
| A.1和17 | B.12和9 | C.14和6 | D.15和8 |
下列物质中,能用于检验酒精中是否含有水的是
| A.CuSO4·5H2O | B.无水硫酸铜 | C.浓硫酸 | D.金属钠 |
某元素最高价氧化物的水化物的化学式为H2XO4,该元素的气态氢化物的化学式是
| A.HX | B.H2X | C.XH3 | D.XH4 |
下列物质在一定条件下可与甲烷发生反应的是
| A.氢氧化钠溶液 | B.稀硫酸 |
| C.氯气 | D.酸性高锰酸钾溶液 |
下列递变规律正确的是
| A.P、S、Cl元素的最高正价依次降低 |
| B.Na、Mg、Al的金属性依次减弱 |
| C.HCl、HBr、HI的稳定性依次增强 |
| D.HClO4、H2SO4、H3PO4的酸性依次增强 |
下列化学用语正确的是
A.CO2的电子式: |
B.乙烯分子的结构式: |
| C.乙酸的结构简式:C2H4O2 |
D.硫原子的原子结构示意图: |
不经过化学变化就能够从海水中获得的物质是
| A.食盐、淡水 | B.Ma、Mg、Al | C.烧碱、氢气 | D.Cl2、Br2、I2 |
由A、B两种金属和稀硫酸组成的原电池,A是正极,则下列推断正确的是
A.A的金属性强于B
B.A电极上发生的电极反应是还原反应
C.电子不断由A电极经外电路流向B电极
D.A在金属性活动顺序表中一定排在氢前面
在元素周期表中,同周期元素原子具有相同的
| A.电子层数 | B.核电荷数 |
| C.核外电子数 | D.最外层电子数 |
下列有关以碱金属元素的性质,从上到下递变规律正确的是
| A.金属性逐渐减弱 |
| B.化合价逐渐升高 |
| C.失电子能力逐渐增强 |
| D.最高价氧化物对应的水化物碱性逐渐减弱 |
工业上用H2和N2直接合成氨: ,下列措施肯定能使合成氨反应速率加快的是
,下列措施肯定能使合成氨反应速率加快的是
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④增大压强
| A.只有①②③ | B.只有①②④ | C.只有①③④ | D.①②③④ |
为了研究化学反应X+Y=Z的能量变化情况,某同学设计了下图所示装置。当向盛有X的试管中滚圆试剂Y时,看到U型管中甲处液面下降乙处液面上升,由此说明:
①反应为放热反应
②生成物的总能量比反应物的总能量高
③物质中的化学能通过化学反应转化成热能释放出来
④反应物化学键断裂吸收的能量高于生成物化学键形成放出的能量
| A.①② | B.①③ | C.①②③ | D.②③④ |
在①6Li ②14N ③7Li ④14C几种核素中:
(1)________和________(填序号,下同)互为同位素。
(2)________和________的质量数相等,但不能互称同位素。
在NaCl、NH4Cl、N2、CO2中,只含有离子键的是________(填化学式,下同),只含有极性键的是_________,只含有非极性键的是__________,既含有离子键又含有共价键的是__________。
下列几组物质:
| A.金属石和石墨 | B.C2H6和C5H12 | C.C2H4和C2H6 |
| D.CH3CH2CH2CH3 E.35Cl和37Cl |
(1)属于同分异构体的是___________(填序号,下同);(2)属于同素异形体的是____________;
(3)属于同素物的是___________; (4)属于同位素的是________________。
下图是元素周期表的一部分,针对表中的①—⑧八种元素,用元素符号或化学式回答相关问题:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为___________。
(2)地壳中含量最多的金属元素是___________。
(3)用电子式表示①与③形成化合物的过程:__________________________。
(4)这些元素的氧化物对应的水化物中,酸性最强的是________,碱性最强的是__________,显两性的是___________,该两性物质与②的最高价氧化物对应水化物的溶液反应的离子方程式为:
_______________________________ 。
(5)①②③④四种元素的简单离子核外电子排布相同,都有__________个电子,它们的离子半径由大到小的顺序是__________________(用“>”表示)。
(6)①⑤⑧三种元素的单质沸点由高到低的顺序是__________________(用“>”表示)。
在试管A中加入3ml乙醇,然后边振荡管边慢慢加入2ml浓硫酸和2ml乙酸,按下图所示连接好装置进行实验,以制取乙酸乙酯。
(1)试管B中盛放的试剂是____________(填名称)
(2)乙醇与乙酸反应的化学方程式是_________________________________。
(3)实验完成后,试管B的液面上有透明的不溶于水的油状液体产生。若要分离B中的液体混合物需要用到的玻璃仪器是____________________。
(4)用30g乙酸与46g乙醇反应,如果实验产率是理论产率的60%,则可等到的乙酸乙酯的质量是__________g(精确到0.1)
某有机物的结构简式为HOOC—CH=CH—CH2OH。
(1)该有机物分子中官能团的名称是:_________、_________、___________。
(2)验证该有机物中含有—COOH官能团常采用的试剂是______________(填名称),
现象是__________________________________________。
下图A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。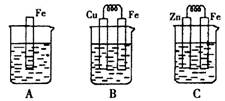
(1)A中反应的离子方程式是_______________________________________。
(2)B中Cu极的电极反应式是______________________________________。
(3)C中被腐蚀的金属是__________(填化学式),A、B、C中铁被腐蚀的速率,由快到慢的是顺序是_____________(用“>”表示)。
已知在溶液中IO3-可与I-发生反应:IO3-+5 I-+6H+====3I2+3H2O,根据此反应,可用试纸和一些生活中常见的物质进行检验,证明食盐中存在IO3-。可供选用的物质有:①自来水;②蓝色石蕊试纸;③碘化钾淀粉试纸;④淀粉;⑤食糖;⑥食醋;⑦白酒。进行上述检验时必须使用的物质是( )
| A.①②③ | B.②⑤ | C.③⑥ | D.①④⑦ |
糖类、油脂、蛋白质都是基本营养物质,有关它们的说法正确的是
| A.油脂在碱性条件下水解可制得甘油和肥皂 |
| B.三类物质都是高分子化合物,均可以发生水解反应 |
| C.蔗糖是一种双糖,1mol蔗糖水解可得2mol葡萄糖 |
| D.淀粉在稀酸下水解后,立即与新制氢氧化铜加热,能看到砖红色沉淀 |
下图为氢氧燃料电池构造示意图,其中A、B为气体进口,C1、C2均为石墨电极,电解质溶液为30%的氢氧化钾溶液,电极反应分别为:

下列有关该燃料电池的叙述正确的是
A.H2从B口进入电池
B.该燃料电池的能量转化率可达100%
C.每生成18g水,导线中电子转移2mol
D.使用该燃料电池时,H+向C1电极移动
关于下列各实验装置的叙述中,正确的是
| A.装置①常用于分离互不相溶的液体 |
| B.装置②可用于吸收NH3 |
| C.装置③可用于除去甲烷中混乱有的少量乙烯 |
| D.装置④可用于收集SO2、Cl2等气体 |
短周期非金属元素X和Y能形成XY2型化合物,下列有关说法正确的是
| A.XY2一定能与水反应 |
| B.XY2水溶液不可能呈碱性 |
| C.符合要求的XY2物质的两种 |
| D.X、Y一定不是同一主族的元素 |
一定条件下,在体积不变的密闭容器中,能表示反应 一定达到化学平衡状态的是
一定达到化学平衡状态的是
①X、Y、Z的物质的量之比为1:2:2 ②X的浓度不再变化
③容器中的压强不再变化 ④Z的物质的量不再变化
⑤气体的密度不再改变
| A.①②③ | B.②③④ | C.②④⑤ | D.①③⑤ |
已知白磷和红磷在一定条件下可以互相转化。25OC 101kPa时,将等质量的白磷和红磷分别完全燃烧,其中白磷放出的热量多,由此判断,下列说法正确的是
| A.由红磷转化为白磷是吸热反应,等质量的红磷能量比白磷高 |
| B.由红磷转化为白磷是放热反应,等质量的红磷能量比白磷低 |
| C.由红磷转化为白磷是放热反应,等质量的红磷能量比白磷高 |
| D.由红磷转化为白磷是吸热反应,等质量的红磷能量比白磷低 |
(3分)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,回答下列问题: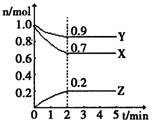
(1)该反应在______min时达到化学平衡状态。
(2)该反应的化学方程式是_______________________________。
(3)从开始到2 min ,Z的平均反应速率是_________________________。
I.有机玻璃是一种高分子化合物,在工业和生活中有着广泛用途,工业上可通过下列合成方法制得:
请回答:
(1)反应①的原子利用率是___________。
(2)反应②的化学方程式是____________________________________,
该反应的反应类型是_____________________ 。
(3)有机玻璃分子中的链节是____________________________。
II.甲基丙烯酸甲酯旧法合成的反应是:
①
②
(1)该方法的缺点是___________________________(填字母)
A.反应的原料利用率低 B.原料中有有毒物质
C.对设备腐蚀性较大 D.生产成本高
(2)甲基丙烯酸甲酯可进行的反应有______________(填字母)
A.加成反应 B.氧化反应 C.取代反应 D酯化反应.
(10分)海水中化学资源的综合开发利用已受到各国的高度重视。Br2和Mg等两种单质都可以从海水中提取,下图为提取它们的步骤:
请回答:
I.从海水中提取的溴占世界年产量的1/3,主要方法就是上述流程中的空气吹出法。
(1)制取Br2时,第一次通入Cl2发生反应的离子方程式是__________________。
(2)吸收塔中反应的离子方程式是________________________________________。
由(1)、(2)可知,SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是
__________________。( 用“”表示)
II.镁及其合金是用途很广泛的金属材料,而目前世界上60%的镁就是从海水中按上述流程提取的。
(1)上述流程中为了使MgSO4完全转化为Mg(OH)2,试剂①可以选用___________(写化学式)。
(2)加入试剂②后反应泊离子方程式是_________________________________。
(3)步骤①包括加热、蒸发、冷却、结晶、_________。
(4)通电时无水MgCl2在熔融状态下反应的化学方程式是
___________________________________________________。
III.上述流程在生产溴和镁的同时还可以制得其他化工物质,比如制备耐火材料氧化镁和盐酸。生产方法是:
①将氯化镁晶体(MgCl2·6H2O)加热到523OC以上,该晶体可以分解得到耐火材料氧化镁和两种气态化合物,其中一种气体常温下为无色液体。
②将两种气体冷却到室温,再根据需要,加入不同量的水,就可得到不同浓度的盐酸。
(1)MgCl2·6H2O在523OC以上分解的化学方程式是_____________________________。
(2)现用1mol MgCl2·6H2O分解所得的非固体产物来制取密度为1.19g/cm3的盐酸溶液168mL,需加水__________g(精确到0.1),该盐酸中溶质的物质的量浓度是____________mol/L(精确到0.1)。
R、Q、X、Y、Z均为短周期元素,且原子序数依次增大。已知Q元素在自然界中组成的化合物种类最多;Y原子最外层电子数与核外电子数之比为 3:4 ;R与Y、Z与Y均可组成原子个数比为1:1和2:1的两种化合物。据此回答:
(1)由R、X、Y三种元素可组成多种化合物,写出两种常见的不同类型的化合物的化学式
___________、______________。
(2)在Q和X组成化合物(QX)2中,Q、X原子均满足最外层8电子结构,则的电子式是(QX)2______。
(3)已知R与Q可组成化合物甲,R与Y可组成化合物乙,其中一个甲分子有10个电子,而一个乙分子有18个电子。
①甲的结构式是_____________。乙分子中共价键数是_____________。
②甲是一种重要的能源,通常状况下,1mol 甲在空气中完全燃烧生成二氧化碳和水,放出890kJ的热,若此时燃烧40g的甲,产生的热量是________kJ。
③在酸性条件下,向FeI2的淀粉溶液中加入乙,溶液变蓝。当1 mol Fe2+被氧化成Fe3+时,反应中电子转移为4 mol,该反应的离子方程式是_____________________________________________。
工业上根据污水中所含物质或离子的不同,有多种处理方法,比如:
请回答:
(1)在中和法中,若用CO2来处理污水,则离子方程式是___________________________。
(2)在沉淀法中,用硫化钠作沉淀剂,能有效地处理含Cu2+、Hg2+等重金属离子的污水。若某污水中能与硫化钠反应的阳离子只有Hg2+,且含量为400mg/L,则处理10L这样的污水至少需要加入硫化钠________g(精确到0.1)
我国规定的排放标准不能超过0.05mg/L,若1L污水经过沉淀法处理后含Hg2+为2×10-7 mol,则该污水是否达到了排放标准_____________(填“是”或“否”)
(3)在氧化还原法中,常用Cl2氧化污水中有毒的CN-,得到元素的CO2和N2,若参加反应的Cl2与CN-的物质的量之比为5:2,则该反应的离子方程式是__________________________________。
X、Y、Z为三种常见的单质,Z是绿色植物光合作用产物之一,A、B为常见化合物。它们在一定条件下可发生如图所示的反应(均在非溶液中进行)。
(1)当X为金属、Y为非金属时,A是________(填名称)。
(2)当X为非金属、Y为金属时,X可能是_________或________(均填化学式)。
(3)当X与Y均为金属时,X与A反应的化学方程式是______________________________。
(4)当X与Y均为非金属,且
X与Y同主族,X与A反应的化学方程式______________________________________。
X与Y不在同一主族,X与A反应的化学方程式________________________________。


 粤公网安备 44130202000953号
粤公网安备 44130202000953号