陕西岐山县高一下学期期末质量检测化学试卷
放射性同位素钬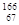 Ho的原子核内的中子数与核外电子数之差是
Ho的原子核内的中子数与核外电子数之差是
| A.32 | B.67 | C.99 | D.166 |
根据元素周期表和元素周期律分析下面的推断,其中错误的是
| A.铍(Be)的原子失电子能力比镁弱 |
| B.砹(At)的氢化物不稳定 |
| C.硒(Se)化氢比硫化氢稳定 |
| D.氢氧化锶[Sr(OH)2]比氢氧化钙的碱性强 |
下列说法中,错误的是
| A.化学反应必然伴随发生能量变化 |
| B.化学反应中的能量变化主要是由化学键变化引起的 |
| C.能量变化是化学反应的基本特征之一 |
| D.化学反应中能量变化的大小与反应物的质量多少无关 |
下列各组材料中,不能组成原电池的是
| |
A |
B |
C |
D |
| 两极材料 |
Zn片.石墨 |
Cu片.Ag片 |
Zn片.Cu片 |
Fe片.Cu片 |
| 插入溶液 |
H2SO4 |
AgNO3溶液 |
蔗糖溶液 |
稀盐酸 |
工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:
2SO2 + O2 2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是
2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是
| A.使用催化剂是为了加快反应速率,提高生产效率 |
| B.在上述条件下,SO2不可能100%地转化为SO3 |
| C.为了提高SO2的转化率,应适当提高O2的浓度 |
| D.达到平衡时,SO2的浓度与SO3的浓度相等 |
烃类分子中的碳原子与其他原子的结合方式是
| A.形成四对共用电子对 | B.通过非极性键 |
| C.通过两个共价键 | D.通过离子键和共价键 |
下列物质中,互为同分异构体的是
| A.淀粉和葡萄糖 | B.蔗糖和纤维素 |
| C.淀粉和纤维素 | D.果糖和葡萄糖 |
如图所示,把锌片和铜片用导线相连后插入装有稀硫酸溶液的烧杯中构成原电池。下列叙述正确的是
| A.Zn是负极,发生还原反应 |
| B.该装置将化学能转变为电能 |
| C.一段时间后,铜片质量减轻 |
| D.电流从锌片流向铜片 |
下列各对物质中互为同系物的是
| A.CH3-CH=CH2和CH3-CH2-CH=CH2 |
| B.CH3-CH3和CH3-CH=CH2 |
| C.CH3-CH2-CH3和CH3-CH=CH2 |
| D.CH3-CH2-CH2-CH3和CH3-CH2-CHCl2 |
下列金属冶炼的反应原理,错误的是
A.2NaCl(熔融) 2Na+Cl2 2Na+Cl2 |
B.MgO+H2 Mg+H2O Mg+H2O |
C.Fe3O4+4CO  3Fe+4CO2 3Fe+4CO2 |
D.2HgO  2Hg+O2 2Hg+O2 |
下列说法中正确的是
①化学性质相似的有机物是同系物 ②结构相似,分子组成相差一个或几个CH2原子团的有机物是同系物 ③若烃中碳、氢元素的质量分数相同,它们不一定是同系物 ④互为同分异构体的两种有机物的物理性质有差别,但化学性质可能相似,也可能不同
| A.①②③④ | B.只有②③④ | C.只有③④ | D.只有①②③ |
医院里检测糖尿病的方法是将病人尿液加入到CuSO4和NaOH的混合液中,加热后产生红色沉淀说明病人的尿液中含有
| A.脂肪 | B.乙酸 | C.葡萄糖 | D.蛋白质 |
实验室里可按下图所示的装置干燥储存气体R,多余的气体可用水吸收,则R是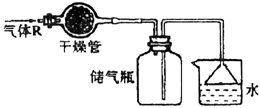
| A.NO2 | B.HCl |
| C.CH4 | D.NH3 |
1~20号元素(稀有气体元素除外)中:
(1)原子半径最小的是 ,原子半径最大的是 。
(2)与水反应最剧烈的金属单质是 ,非金属单质是 。
(3)既能与酸反应,又能与碱反应的金属单质是 。
(4)硬度最大的单质是 。
(5)气态氢化物的稳定性最强的是 。
(6)最高价氧化物对应的水化物碱性最强的是 (以上填元素符号或化学式)。
(7)铅是碳的同族元素,比碳多4个电子层,铅在周期表的位置为 周期、第 族。
如下图所示,烧杯中都盛有稀硫酸。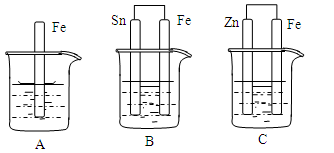
(1)A中反应的离子方程式为 ;
(2)B中的电极反应:Fe: .Sn: Sn极附近溶液的pH(填增大、减小或不变) ;
(3)C中被腐蚀的金属是 。其电极反应式为 。比较A、B、C中纯铁被腐蚀的速率由快到慢的顺序是 。
乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答:
(1)乙烯的电子式为 ,结构简式为________________。
(2)下列可以鉴别甲烷和乙烯的试剂为________(填选项字母)。
A.稀硫酸 B.溴的四氯化碳溶液
C.水 D.酸性高锰酸钾溶液
(3)下列物质中,不能通过乙烯加成反应得到的是________(填选项字母)。
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
(4)2CH3CHO + O2 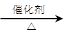 2CH3COOH 以乙烯为主要原料合成乙酸,合成线路如下图所示:
2CH3COOH 以乙烯为主要原料合成乙酸,合成线路如下图所示: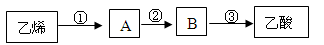
反应③的反应类型为 反应,反应②的化学方程式为 。
工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,该反应类型为 反应,其反应的化学方程式为 。
海藻中含有丰富的碘元素(以I-形式存在)。实验室中提取碘的流程如下:
(1)实验操作③的名称是__________,所用主要仪器名称为__________。
(2)提取碘的过程中,可供选择的有机试剂是__________(填序号)。
A.酒精(沸点78℃) B.四氯化碳(沸点77℃)
C.甘油(沸点290℃) D.苯(沸点80℃)
(3)在操作②中,溶液中生成少量ICl,为消除此杂质,使碘全部游离出来,应加入适量(填序号)_____溶液,反应的离子方程式为 。
A.KIO3 B.HClO C.KI D.Br2
(4)为使从含碘有机溶液中提取碘并回收溶剂顺利进行,采用水浴加热蒸馏(如图所示)。请指出图中实验装置中错误之处(有几处填几处,下列空白可不填满,也可补充)。
①_________________________,
②_________________________,
③_________________________,
④_________________________。
(5)实验中使用水浴的原因是 ,最后晶体碘聚集在__________(填仪器名称)中。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号