2010年全国统一高考理综试卷(湖南卷)化学部分
(Ⅰ)合金是生活中常用的材料,请回答下列问题:
(1)生铁和钢是含碳量不同的铁碳合金,含碳量在2%~4.3%的称为。不锈钢在空气中比较稳定,不易生锈,有强的抗腐蚀能力,其合金元素主要是;
(2)钢铁的腐蚀给社会造成的损失是巨大的,所以采取各种措施防止钢铁的腐蚀是十分必要的,请列举三种防止钢铁腐蚀的方法;
(3)青铜的主要合金元素为,黄铜的主要合金元素为:
(4)储氢合金是一类能够大量吸收氢气,并与氢气结合成金属氢化物的材料。如镧镍合金,它吸收氢气可结合成金属氢化物,其化学式可近似地表示为 (中各元素化合价均可看作是零),它跟可组成镍氢可充电电池:
该电池放电时,负极反应是。市面上出售的标称容量为2000的1节镍氢电池至少应含有镧镍合金(已知1法拉第电量为96500库仑或安培·秒)。
(Ⅱ)有机化合物与生活息息相关。请回答下列有关问题:
(1)棉花、蚕丝、小麦主要成分分别为、、,它们蕃都属于天然有机高分子化合物;
(2)味精是烹饪常用的调味品,其主要成分的化学名称为;
(3)解热镇痛药阿司匹林主要成分的结构简式为。
下列各项表达中正确的是
| A. |
的电子式为

|
| B. | 的乙醇和丙醇混合液完全燃烧生成的 为 (标准状况) |
| C. | 在氮原子中,质子数为7而中子数不一定为7 |
| D. |
的结构示意图为

|
分子式为的同分异构体共有(不考虑立体异构)
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
下列各组中的反应,属于同一反应类型的是
| A. | 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 |
| B. | 由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸 |
| C. |
由氯代环己烷消去制环己烯;由丙烯加溴制
 二溴丙烷 二溴丙烷
|
| D. | 由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇 |
把500 有和的混合溶液分成5等份,取一份加入含硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为
| A. | B. | ||
| C. | D. |
下表中评价合理的是
化学反应及其离子方程式 |
评价 |
|
A. |
与稀硝酸反应:↑ |
正确 |
B. |
向碳酸镁中加入稀盐酸:↑ |
错误,碳酸镁不应写成离子形式 |
C. |
向硫酸铵溶液中加入氢氧化钡溶液:↓ |
正确 |
D. |
溶液与等物质的量的反应: |
错误,与的化学计量数之比应为1:2 |
物质有下图所示转化关系(部分反应物、生成物没有列出)。其中为某金属矿的主要成分,经过一系列反应可得到和。单质可与的浓溶液发生反应,为砖红色沉淀。
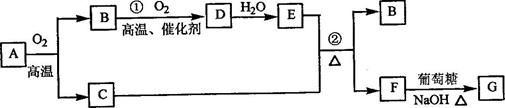
请回答下列问题:
(1)写出下列物质的化学式:
(2)利用电解可提纯物质,在该电解反应中阳极物质是
(3)反应②的化学方程式是
(4)将0.23和0.11氧气放入容积为1的密闭容器中,发生反应①,在一定温度下,反应达到平衡,得到0.12 ,则反应的平衡常数
某化学兴趣小组为探究的性质,按下图所示装置进行实验。
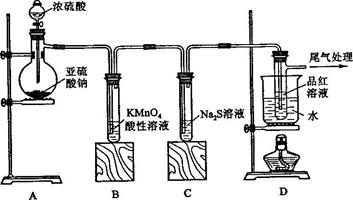
请到答F列问题:
(1)装置中盛放亚硫酸钠的仪器名称是,其中发生反应的化学方程式为;
(2)实验过程中,装置、中发生的现象分别是,这些现象分别说明具有的性质是 和;装置中发生反应的离子方程式为;
(3)装置的目的是探究与品红作用的可逆性,请写出实验操作及现象;
(4)尾气可采用溶液吸收。
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有
(2)硫酸铜溶液可以加快氢气生成速率的原因是
(3)实验室中现有、、、等4种溶液,可与实验中溶液起相似作用的是
(4)要加快上述实验中气体产生的速率,还可采取的措施有
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验 混合溶液 |
||||||
| 4 | 30 |
1 |
2 |
3 |
4 |
5 |
| 饱和溶液/ | 0 |
0.5 |
2.5 |
5 |
6 |
20 |
| 7 |
8 |
9 |
10 |
10 |
0 |
①请完成此实验设计,其中:1=
②反应一段时间后,实验中的金属呈
③该同学最后得出的结论为:当加入少量溶液时,生成氢气的速率会大大提高。但当加入的溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
是一种可降解的聚碳酸酯类高分子材料,由于其具有优良的耐冲击性和韧性,因而得到了广泛的应用。以下是某研究小组开发的生产的合成路线:

已知以下信息:
①可使溴的溶液褪色;
②中有五种不同化学环境的氢;
③可与溶液发生显色反应;
④不能使溴的褪色,其核磁共振氢谱为单峰。
请回答下列问题:
(1)的化学名称是;
(2)的结构简式为;
(3)与反应生成的化学方程式为;
(4)有多种同分异构体,其中能发生银镜反应的是 (写出结构简式);
(5)的同分异构体中含有苯环的还有种,其中在核磁共振氢谱中出现丙两组峰,且峰面积之比为3:1的是(写出结构简式)。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号