专题2:阿伏加德罗常数与化学计算
【2015新课标Ⅰ卷理综化学】NA为阿伏伽德罗常数的值。下列说法正确的是
| A.18gD2O和18gH2O中含有的质子数均为10NA |
| B.2L0.5mol/L亚硫酸溶液中含有的H+两种数为2NA |
| C.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA |
| D.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
【2015新课标Ⅱ卷理综化学】NA代表阿伏加德罗常数的值。下列叙述正确的是
| A.60g丙醇中存在的共价键总数为10NA |
| B.1L 0.1mol·L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA |
| C.钠在空气中燃烧可生成多种氧化物。23g钠充分燃烧时转移电子数为1NA |
D.235g核互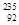 U发生裂变反应: U发生裂变反应: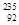 U+ U+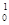 n n 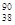 Sr+ Sr+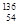 U+10 U+10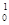 n,净产生的中子( n,净产生的中子(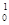 n)数为10NA n)数为10NA |
【2015四川理综化学】设NA为阿伏加德罗常数的值,下列说法正确的是
| A.2.0gH218O与D2O的混合物中所含中子数为NA |
| B.常温常压下,4.4g乙醛所含σ键数目为0.7NA |
| C.标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5 NA |
| D.50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
【2015广东理综化学】设nA为阿伏伽德罗常数的数值,下列说法正确的是
| A.23g Na 与足量H2O反应完全后可生成nA个H2分子 |
| B.1 molCu和足量热浓硫酸反应可生成nA个SO3分子 |
| C.标准状况下,22.4L N2和H2混合气中含nA个原子 |
| D.3mol单质Fe完全转变为Fe3O4,失去8nA个电子 |
【2015海南化学】下列指定微粒的数目相等的是
| A.等物质的量的水与重水含有的中子数 |
| B.等质量的乙烯和丙烯中含有的共用电子对数 |
| C.同温、同压同体积的CO和NO含有的质子数 |
| D.等物质的量的铁和铝分别于足量氯气完全反应时转移的电子数 |
【2015上海化学】将O2和NH3的混合气体448mL通过加热的三氧化二铬,充分反应后,再通过足量的水,最终收集到44.8mL气体。原混合气体中O2的体积可能是(假设氨全部被氧化;气体体积均已换算成标准状况)
| A.231.5mL | B.268.8mL | C.287.5mL | D.313.6mL |
【2015山东理综化学】(15分)利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法制备,钴氧化物可通过处理钴渣获得。
(1)利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B极区电解液为________溶液(填化学式),阳极电极反应式为_________,电解过程中Li+向_____电极迁移(填“A”或“B”)。
(2)利用钴渣[含Co(OH)3、Fe(OH)3等]制备钴氧化物的工艺流程如下: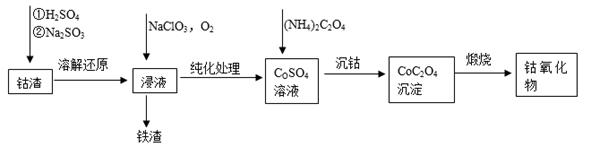
Co(OH)3溶解还原反应的离子方程式为___________,铁渣中铁元素的化合价为___________,在空气中煅烧CoC2O4生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则钴氧化物的化学式为__________。
【2015江苏化学】(12分)软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的水悬浊液与烟气中SO2反应可制备MnSO4·H2O ,反应的化学方程式为:MnO2+SO2=MnSO4
(1)质量为17.40g纯净MnO2最多能氧化_____L(标准状况)SO2。
(2)已知:Ksp[Al(OH)3]=1×10-33,Ksp[Fe(OH)3]=3×10-39,pH=7.1时Mn(OH)2开始沉淀。室温下,除去MnSO4溶液中的Fe3+、Al3+(使其浓度小于1×10-6mol·L-1),需调节溶液pH范围为________。
(3)下图可以看出,从MnSO4和MgSO4混合溶液中结晶MnSO4·H2O晶体,需控制结晶温度范围为_______。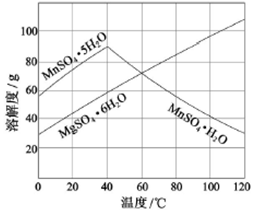
(4)准确称取0.1710gMnSO4·H2O样品置于锥形瓶中,加入适量H2PO4和NH4NO3溶液,加热使Mn2+全部氧化成Mn3+,用c(Fe2+)=0.0500mol·L-1的标准溶液滴定至终点(滴定过程中Mn3+被还原为Mn2+),消耗Fe2+溶液20.00mL。计算MnSO4·H2O样品的纯度(请给出计算过程)。
【2015上海化学】(本题共12分)甲醛是深受关注的有机化合物。甲醛含量的测定有多种方法,例如:在调至中性的亚硫酸钠溶液中加入甲醛水溶液,经充分反应后,产生的氢氧化钠的物质的量与甲醛的物质的量相等,然后用已知浓度的硫酸滴定氢氧化钠。
完成下列填空:
(1)将4.00 mL甲醛水溶液加入到经调至中性的亚硫酸钠溶液中,充分反应后,用浓度为1.100 mol/L的硫酸滴定,至终点时耗用硫酸20.00 mL。
甲醛水溶液的浓度为 mol/L。
(2)上述滴定中,若滴定管规格为50mL,甲醛水溶液取样不能超过 mL。
(3)工业甲醛含量测定的另一种方法:在甲醛水溶液中加入过氧化氢,将甲醛氧化为甲酸,然后用已知浓度的氢氧化钠溶液滴定。
HCHO + H2O2 → HCOOH + H2O
NaOH + HCOOH → HCOONa + H2O
已知H2O2能氧化甲酸生成二氧化碳和水。
如果H2O2用量不足,会导致甲醛含量的测定结果 (选填“偏高”、“偏低”或“不受影响”),因为 ;如果H2O2过量,会导致甲醛含量的测定结果 (选填“偏高”、“偏低”或“不受影响”),因为 。
(4)甲醛和新制氢氧化铜的反应显示了甲醛的还原性,发生反应的化学方程式通常表示如下:
HCHO + 2Cu(OH)2 HCOOH + Cu2O↓ + 2H2O
HCOOH + Cu2O↓ + 2H2O
若向足量新制氢氧化铜中加入少量甲醛,充分反应,甲醛的氧化产物不是甲酸或甲酸盐,设计一个简单实验验证这一判断。
①主要仪器:试管 酒精灯
②可供选用的试剂:硫酸铜溶液、甲醛、甲酸、氢氧化钠溶液
【2015上海化学】(本题共14分)氨碱法制纯碱包括石灰石分解、粗盐水精制、氨盐水碳酸化等基本步骤。
完成下列计算:
(1)CaCO3质量分数为0.90的石灰石100 kg完成分解产生CO2 L(标准状况)。
石灰窑中,该石灰石100 kg与焦炭混合焙烧,产生CO2 29120 L(标准状况),
如果石灰石中碳酸钙完全分解,且焦炭完全燃烧,不产生CO,则焦炭的物质的量为 mol。
(2)已知粗盐水含MgCl2 6.80 mol/m3,含CaCl2 3.00mol/m3。
向粗盐水中加入Ca(OH)2除镁离子:MgCl2 + Ca(OH)2 → Mg(OH)2↓ + CaCl2
然后加入Na2CO3除钙离子。
处理上述粗盐水10 m3,至少需要加Na2CO3 g。
如果用碳酸化尾气(含NH3体积分数为0.100、CO2体积分数0.040)代替碳酸钠,发生如下反应:
Ca2+ + 2NH3 + CO2 + H2O → CaCO3↓ + 2NH4+
处理上述10 m3粗盐水至少需要通入多少L(标准状况)碳酸化尾气?列式计算。
(3)某氨盐水含氯化钠1521 kg,通入二氧化碳后析出碳酸氢钠晶体,过滤后溶液中含氯化铵1070 kg。列式计算:
①过滤后溶液中氯化钠的质量。
②析出的碳酸氢钠晶体的质量。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号