新课标高一化学第一节 无机非金属材料的主角—硅练习
下列说法正确的是( )
| A.SiO2溶于水显酸性 |
| B.CO2通入水玻璃可得硅酸 |
| C.SiO2是酸性氧化物,它不溶于任何酸 |
| D.SiO2晶体中不存在单个SiO2分子 |
下列说法正确的是( )
| A.SiO2溶于水显酸性 |
| B.CO2通入水玻璃中可得到原硅酸 |
| C.SiO2是酸性氧化物,它不溶于任何酸 |
| D.因高温时SiO2与Na2CO3反应放出CO2,所以硅酸的酸性比碳酸强 |
10g含有杂质的CaCO3和足量的盐酸反应,产生CO20.1mol,则此样品中可能含有的杂质是( )
| A.KHCO3和MgCO3 | B.MgCO3和SiO2 |
| C.K2CO3和SiO2 | D.无法确定 |
下列关于二氧化硅的说法中,错误的是( )
| A.二氧化硅也叫硅酐 |
| B.二氧化硅分子由一个硅原子和两个氧原子构成 |
| C.不能用二氧化硅跟水直接作用制取硅酸 |
| D.二氧化硅既能与氢氟酸反应,又能与烧碱反应,所以它是两性氧化物 |
下面关于硅的叙述中,正确的是( )
| A.硅的非金属性比碳强,只有在高温下才能跟氢气起化合反应 |
| B.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位 |
| C.硅的化学性质不活泼,在自然界中可以以游离态存在 |
| D.硅在电子工业中,是重要的半导体材料 |
证明生石灰中既混有石英,又混有石灰石的正确方法是( )
| A.加入过量的盐酸,观察是否有气泡冒出 |
| B.加入过量的烧碱溶液,观察是否有固体溶解 |
| C.加热至高温,观察是否有气泡冒出,是否有硅酸钙生成 |
| D.先加过量的盐酸搅拌,观察是否有不溶物剩余及气泡出现;若有不溶物则滤出,投入到氢氧化钠溶液中看其是否溶解 |
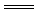 H2SiO3↓+Na2CO3
H2SiO3↓+Na2CO3 Na2SiO3+CO2↑
Na2SiO3+CO2↑ 粤公网安备 44130202000953号
粤公网安备 44130202000953号