辽宁省沈阳郊联体高一下期中化学理试卷
化学为人类基本的生存需要、进而追求生活乃至生命质量的提升提供了重要的保障。但某些人的贪得无厌和对化学原理的滥用败坏了化学学科声誉,我们每个人都应该避免成为这样的人。下列科学史上的重要发现与发明,从原理上看与化学学科没有直接相关性的是
| A.1774年舍勒最早制得氯气,1820年前后漂白粉用于饮用水消毒 |
| B.1869年门捷列夫发现元素周期律,使元素的性质更有规律可循 |
| C.1902年哈伯开始对合成氨反应进行研究,工业化后提高了粮食产量 |
| D.1942年费米进行了235U原子核裂变试验,从而开创原子能利用时代 |
近期我国合成多种元素的新同位素,其中一种是 (铪),它的中子数和电子数之差是
(铪),它的中子数和电子数之差是
| A.41 | B.72 | C.113 | D.185 |
浓硫酸在与含有水分的蔗糖作用过程中没有显示的性质是
| A.强氧化性 | B.脱水性 | C.酸性 | D.吸水性 |
运用元素周期律分析下面的推断,其中错误的是
| A.锂(Li)的密度比钠小,锂的熔沸点也比钠低 |
| B.砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 |
| C.在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 |
| D.HBrO4的酸性比HIO4的酸性强 |
往100 mL氢离子浓度为1mol·L-1的硫酸和硝酸混合液中投入3.84 g铜粉,微热使反应充分完成后,生成NO气体448 mL(标准状况)。则反应前的混合液中含硫酸的物质的量为
| A.0.01mol | B.0.02 mol | C.0.03 mol | D.0.04 mol |
我国明代宋应星所著《天工开物》中有关于“升炼倭铅”的记载:“炉甘石(碳酸锌)十斤,装载入一泥罐内,封裹泥固,······,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,·····,冷定毁罐取出,······,即倭铅也,······,以其似铅而性猛,故名之曰倭”,下列对于这段话中描述的理解错误的是
| A.我国历史上铅的使用早于锌 |
| B.锌和铅有相似性但锌更活泼 |
| C.所得产品中混有煤炭 |
| D.属于热还原法冶炼金属 |
海带中碘元素的检验可经过以下四个步骤完成,各步骤中选用的实验用品不能都用到的是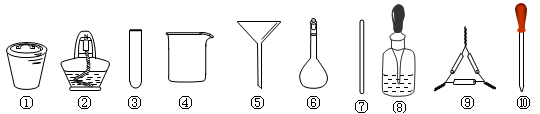
| A.将干海带剪碎后灼烧灰化,选用①、②和⑨ |
| B.将海带灰加入蒸馏水搅拌煮沸,选用④、⑥和⑦ |
| C.过滤得到的滤液,选用④、⑤和⑦ |
| D.检验滤液中的I-,选用③、⑧和⑩ |
X、Y、Z均为短周期元索,X、Y处于同一周期,X、Z的最低价离子分别为x2-和Z-,Y+ 和Z-具有相同的电子层结构。下列说法正确的是
| A.原子最外层电子数:X>Y>Z | B.单质活泼性: X>Y>Z |
| C.原子序数: X>Y>Z | D.离子半径: X2—>Y+>Z— |
工业废气中氮氧化物是主要污染物,为了治理污染,常通入NH3,发生反应NOx+NH3―→N2+H2O来治理污染.现有NO、NO2的混合气体3 L,用同温同压下3.5 LNH3使其恰好完全转化为N2,则混合气体中NO、NO2的物质的量之比为
| A.1∶1 | B.1∶3 | C.2∶1 | D.1∶4 |
化学史上很多重要物质的发现背后都有科学家们的兴趣、坚持、创新与传承。例如氨的发现史,阅读下文并填空。
1727年,英国牧师、化学家哈尔斯用氯化铵与熟石灰的混合物在以水封闭的曲颈瓶中加热,只见水被吸入瓶中而不见气体放出;
(1)哈尔斯制氨气发生的反应方程式为 ,水吸入曲颈瓶的原理与 实验相同。氨的电子式为 ;
1774年英国化学家普利斯特里重作这个实验,采用汞代替水来密闭曲颈瓶,即排汞取气法,制得了碱空气(氨)。他还研究了氨的性质,他发现 ;
(2)氨可以在纯氧中燃烧,已知该反应为一个置换反应,反应方程式为 ,预期该反应在生产上 (填有或无)实际用途。
(3)在氨气中通以电火花时,气体体积在相同条件下增加很多,该反应的化学方程式是 ,据此证实了氨是氮和氢的化合物。其后戴维等化学家继续研究,进一步证实了氨的组成。
短周期A、B、C、D 4种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上电子数之和。
(1)A的原子结构示意图是___________ E的电子式为___________;
(2)D在周期表中的位置是 ______。它的下一周期同族元素最高价氧化物对应的水化物的分子式为___________;
(3)C与水反应的化学方程式是_________________________________,写出所得溶液中含有10个电子的微粒符号___________。
焦炭是工业生产中的重要还原剂和燃料,活性炭用于生活和实验室中通过吸附作用除去有害气体或有毒物质。它们的化学成分都可以看成是碳单质。
(1)红热的焦炭投入浓硝酸中,写出反应的化学方程式 ;
(2)将一定条件下的高锰酸钾溶液与活性炭混合,可发生如下反应(未配平)
MnO4-+ C+ H2O—— MnO2+ ① +CO32-
则 ① 处应该填入的微粒化学式为 ;
(3)PbO俗称密陀僧或铅黄,将黄色粉末状PbO和足量活性炭充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水,按图连接仪器。实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却。此时,管中的熔融物凝固成银白色金属。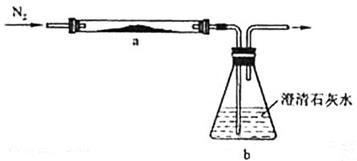
写出反应管a中发生的所有反应的化学方程式 。
甲~辛等元素在周期表中的相对位置如下表。甲与戊的原子序数相差4,戊的单质是空气中含量最多的成分,丁与辛属同周期元素,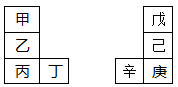
(1)用元素符号表示甲、乙、丁的金属性从强到弱的顺序 ;
(2)用元素符号表示辛、己、戊的原子半径从大到小的顺序 ;
(3)丙与庚的原子核外电子数相差 ;
(4)戊单质电子式为 ,写出一种含戊、己两种元素的离子化合物的化学式 。
工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生成过程。
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若 ,则整个装置气密性良好。装置D的作用是 。装置E中为 溶液。
(2)装置A中反应的化学方程式为 。
烧瓶C中发生反应如下:
Na2S+H2O+SO2=Na2SO3+H2S (I)
2H2S+SO2=3S+2H2O (II)
S+Na2SO3 Na2S2O3 (III)
Na2S2O3 (III)
为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号