河北省石家庄市高三下学期二模考试理综化学试卷
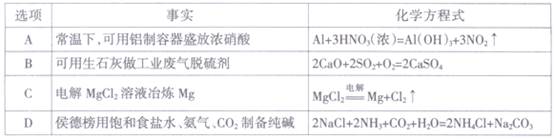
下列说法正确的是
| A.CH3CH2CH3分子中的3个碳原子不可能在同一直线上 |
| B.油脂在酸性条件下的水解反应称为皂化反应 |
| C.聚氯乙烯、麦芽糖和蛋白质均属于有机高分子化合物 |
D.CH3CH2OH与CH3CO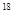 OH发生酯化反应所得混合液中, OH发生酯化反应所得混合液中,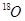 原子只存在于水分子中 原子只存在于水分子中 |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.2 mL 0.5 mol/L硅酸钠溶液中滴入盐酸所制得的硅酸胶体中,含胶粒数目为0.001 NA |
| B.8.4 g NaHCO3固体中含有的离子总数为0.3 NA |
| C.25℃时,1 L pH=l的CH3COOH溶液中含有氢离子数目为0.l NA |
| D.7.8 g 过氧化钠固体中含有的共用电子对数目为0.2NA |
下列与金属腐蚀有关的说法正确的是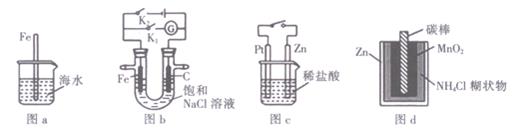
| A.图a中,插人海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,闭合K2,铁电极的腐蚀速率比闭合K1时慢 |
| C.图c中,接通开关时,Zn的腐蚀速率增大,Zn上放出气体的速率也增大 |
| D.图d中,锌锰电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
短周期元素X、Y、Z、W的原子序数逐渐增大,其中X原子的电子数与电子层数相等,Z为短周期中金属性最强的元素,Y与X、Y与Z均能形成原子个数比为1:1和1:2的两种化合物,Y和W同主族。下列说法正确的是
| A.Y与Z形成的两种化合物中所含化学键类型完全相同 |
| B.化合物X2W比化合物X2Y稳定 |
| C.Y、Z、W三种元素形成的化合物的水溶液一定呈中性 |
| D.原子半径:r(Z)>r(W)>r(Y)>r(X) |
已知热化学方程式:
①CO(g)+1/2O2(g)=CO2(g) △H= -283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(g) △H= -241.8kJ/mol
据此判断下列说法正确的是
| A.H2(g)+1/2O2(g)=H2O(l) △H>-241.8kJ/mol |
| B.H2(g)的燃烧热△H ="-241.8" kJ/mol |
| C.H2(g)转变成H2O(g)的化学反应一定放出能量 |
| D.CO(g)+ H2O(g)= CO2(g)+ H2(g)的△H =-41.2kJ/mol |
某浅绿色晶体X[x(NH4)2SO4·yFeSO4·zH2O]在分析化学上常用作还原剂。为确定其组成,某小组同学进行如下实验。
I.NH4+的测定
采用蒸馏法,蒸馏装置如图所示,实验步骤如下: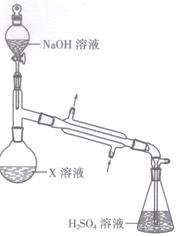
①准确称取19.60 g晶体X,加水溶解,注入圆底烧瓶中;
②准确量取50.00 mL l.0100 mol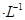 H2SO4溶液于锥形瓶中;
H2SO4溶液于锥形瓶中;
③向圆底烧瓶中加入足量NaOH溶液,加热蒸馏;
④用0.0400 mol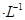 NaOH标准溶液滴定锥形瓶中过剩的酸,到终点时消耗NaOH标准溶液25.00 mL。
NaOH标准溶液滴定锥形瓶中过剩的酸,到终点时消耗NaOH标准溶液25.00 mL。
(1)步骤②中,准确量取H2SO4溶液所用的玻璃仪器为________.
(2)步骤③中,加热蒸馏时间需长达30分钟,其目的为________.
(3)步骤④中,若滴定前滴定管尖嘴有气泡,滴定后气泡消失,则所测n(NH4+)的值将________(填“偏大”、“偏小”或“不变”)。
Ⅱ.SO42-的测定
采用重量分析法,实验步骤如下:
①另准确称取19.60 g晶体X于烧杯中,加水溶解,边搅拌边加入过量的 BaCl2溶液;
②用无灰滤纸(灰分质量很小,可忽略)过滤,洗涤沉淀3~4次;
③用滤纸包裹好沉淀取出,灼烧滤纸包至滤纸完全灰化;
④继续灼烧沉淀至恒重.得沉淀质量23.30 g。
(4)步骤①中,判断 BaCl2溶液已过量的实验操作和现象是________。
(5)步骤②中,所用洗涤剂最合适的是________(填选项字母)。
A.冷水 B.稀硫酸 C.滤液
(6)步骤③灼烧操作中,除三脚架外,还需要用到下列仪器中的____(填选项字母)。
A.烧杯
B.坩埚
C.表面皿
D.泥三角
E.蒸发皿
F.酒精灯
(7)综合实验I、Ⅱ,通过计算得出晶体X的化学式为________。
稀土是一种不可再生的战略性资源,被广泛应用于电子信息、国防军工等多个领域。一种从废弃阴极射线管(CRT)荧光粉中提取稀土元素钇(Y)的工艺流程如下: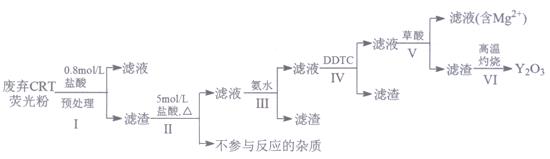
已知:①废弃CRT荧光粉的化学组成(某些不参与反应的杂质未列出)如下表所示;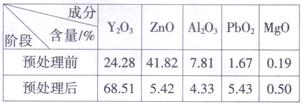
②不同离子沉淀的pH如图一所示。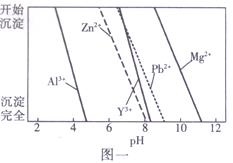
(1)步骤I中进行原料预处理的目的为________________。
(2)步骤Ⅱ中有黄绿色气体产生,该反应的化学方程式为________________。
(3)步骤Ⅲ中发生的主要反应的离子方程式为________________。
(4)步骤Ⅳ中除杂试剂DDTC除去的杂质离子有____________,其不能通过直接加碱的方法除去,原因为________。
(5)步骤V中Y3+沉淀完全时,需保证滴加草酸后的溶液中c(C2O42-)不低于________mol/L。
(已知:当离子浓度小于10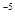 mol/L时,沉淀就达完全;Ksp[Y2(C2O4)3]= 8.0×10-28)
mol/L时,沉淀就达完全;Ksp[Y2(C2O4)3]= 8.0×10-28)
(6)步骤Ⅵ中草酸钇隔绝空气加热可以得到Y2O3,该反应的化学方程式为____________。
汽车尾气中含有NO、CO和碳颗粒等有害物质,已成为某些大城市空气的主要污染源。
(1)汽车燃料中一般不含氮元素,汽缸中生成NO的原因为(用化学方程式表示为可逆反应)________;汽车启动后,汽缸内温度越高,单位时间内NO排放量越大,试分析其原因________。
(2)治理汽车尾气中NO和CO污染的一种方法是将其转化为无害的和,反应原理为: 2CO(g)+2NO (g) 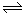 CO2(g)+N2 (g) △H<0,某研究小组在三个容积均为5L的恒容密闭容器中,分别充入0.4 mol NO和0.4 molCO,在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示:
CO2(g)+N2 (g) △H<0,某研究小组在三个容积均为5L的恒容密闭容器中,分别充入0.4 mol NO和0.4 molCO,在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示: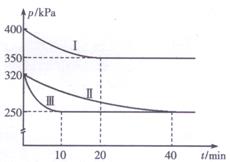
①计算实验Ⅱ从开始至达到平衡时的反应速率v(N0)=________。
②图中三组实验从开始至达到平衡时的反应速率v( NO)由大到小的顺序为__________(填实验序号)。
③与实验Ⅱ相比,实验I和实验Ⅲ分别仅改变一种反应条件,所改变的条件和判断的理由为:
实验I__________________________________________;
实验Ⅲ________________________________________。
④三组实验中CO的平衡转化率α1(CO)、αII(CO)和αIII(CO)的大小关系为____________。
⑤计算实验Ⅲ的平衡常数K=____________。
[化学一选修2:化学与技术]海洋是一个丰富的资源宝库,通过海水的综合利用可获得许多物质供人类使用。
(1)海水中盐的开发利用:
①海水制盐目前以盐田法为主,建盐田必须选在远离江河人海口,多风少雨,潮汐落差大且又平坦空旷的海滩。所建盐田分为贮水池、蒸发池和________池。
②目前工业上采用比较先进的离子交换膜电解槽法进行氯碱工业生产,在电解槽中阳离子交换膜 只允许阳离子通过,阻止阴离子和气体通过,请说明氯碱生产中阳离子交换膜的作用_______(写一点即可)。
(2)电渗析法是近年来发展起来的一种较好的海水淡化技术,其原理如图所示。其中具有选择性的阴离子交换膜和阳离子交换膜相间排列。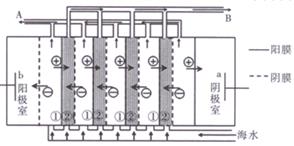
①海水不能直接通入到阴极室中,理由是______________.
②A口排出的是_______(填“淡水”或“浓水”)。
(3)用苦卤(含 Na+、K+、Mg2+、Cl-、Br-等离子)可提取溴,其生产流程如下: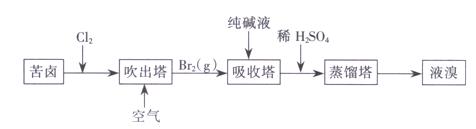
①若吸收塔中的溶液含BrO3-,则吸收塔中反应的离子方程式为___________。
②通过苦卤中通入Cl2已获得含溴的溶液,为何还需经过吹出、吸收、酸化来重新获得含Br2的溶液________。
③向蒸馏塔中通入水蒸气加热,控制温度在90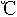 左右进行蒸馏的原因是___________。
左右进行蒸馏的原因是___________。
[化学一选修3:物质结构与性质]第四周期的过渡元素在工业、农业、科学技术以及人类生活等方面有重要作用。其中Ni-Cr-Fe合金是常用的电热元件材料。请回答:
(1)基态Ni原子核外电子排布式为_______;第二周期中基态原子未成对电子数与Ni相同且电负性大的元素为________。金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)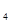 ,该分子呈正四面体构型。试推测Ni(CO)
,该分子呈正四面体构型。试推测Ni(CO)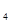 的晶体类型为________,Ni(CO)
的晶体类型为________,Ni(CO)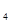 易溶于下列_______(填选项字母)中。
易溶于下列_______(填选项字母)中。
| A.水 | B.四氯化碳 | C.苯 | D.硫酸镍溶液 |
(2)FeO、NiO晶体中r(Ni2+)和r(Fe2+)分别为69 pm和78 pm,则熔点NiO_________FeO(填“>”或“<”),原因为_____________;黄血盐是一种配合物,其化学式为K4[Fe(CN)6] ·3H2O,该配合物中配体的化学式为_________,黄血盐溶液与稀硫酸加热时发生非氧化还原反应,生成硫酸盐和一种与该配体互为等电子体的气态化合物,该反应的化学方程式为_______________。
(3)酸性高锰酸钾溶液能氧化硝基苯酚,邻硝基苯酚和对硝基苯酚在20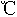 水中的溶解度之比为0.39,其原因为_________。
水中的溶解度之比为0.39,其原因为_________。
(4)在铬的硅酸盐中,SiO44-四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大结构型式。图(b)为一种链状结构的多硅酸根,其中Si原子的杂化形式为________,其化学式为_________。
[化学一选修5:有机化学基础]某有机反应中间体(M)的一种合成路线如图所示。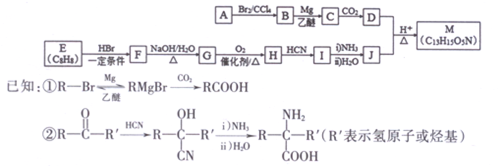
③标准状况下,气态烃A的密度是H2的14倍
④芳香族化合物H能发生银镜反应
请回答:
(1)B的名称(系统命名)为________ ;H→I的反应类型为___________。
(2)E中官能团的结构简式为_________,
(3)F到G的化学方程式为________。
(4)D+J→M的化学方程式为_________。
(5)写出符合下列条件的J的所有同分异构体的结构简式________(不考虑立体异构)。
①苯环上连有-NO2
②核磁共振氢谱有3个峰
(6)结合已有知识和相关信息,写出以CH3CHO和E为原料,经三步制备
合成路线流程图示例为:
 粤公网安备 44130202000953号
粤公网安备 44130202000953号