天津市和平区九年级下学期第一次质量调查化学试卷
偏钛酸钡(BaTiO3)因其显著的“压电效应”而广泛应用于超声波发生装置中。已知偏钛酸钡中钡元素的化合价为+2价,则其偏钛酸钡中钛元素的化合价是
| A.+1 | B.+2 | C.+3 | D.+4 |
厕所用清洁剂中含有盐酸,如果不慎洒到大理石地面上,会发出嘶嘶声,并有气体产生。这种气体是
| A.氢气 | B.二氧化硫 | C.氧气 | D.二氧化碳 |
下列实验现象的描述中,错误的是
| A.细铁丝在氧气中燃烧,火星四射,生成黑色固体 |
| B.红磷在空气中燃烧产生大量的白色烟雾 |
| C.硫在氧气中燃烧产生蓝紫色火焰、放热、生成有刺激性气味的气体 |
| D.打开盛有浓盐酸试剂瓶的瓶塞,在瓶口上方出现大量白雾 |
下列说法正确的是
| A.人体缺乏维生素A会引起坏血病 |
| B.棉花、羊毛、塑料均属于合成有机高分子材料 |
| C.可以用NaNO2代替NaCl |
| D.香烟烟气中的一氧化碳是一种极易与血液中的血红蛋白结合的有毒气体 |
有关水的认识正确的是
| A.电解水得到H2和O2,可知水是由氢原子和氧原子组成的 |
| B.水和过氧化氢的组成元素一样,所以化学性质也一样 |
| C.液态水变成水蒸气,分子间间隔增大 |
| D.KMnO4、NaCl、汽油加入一定量水中都能形成溶液 |
下列说法正确的是
A.喝了汽水会打嗝,说明压强减小气体的溶解度增大
B.金刚石和石墨物理性质存在着明显差异,是因为构成它们的碳原子的排列方式不同
C.二氧化锰可以加快过氧化氢分解速率,所以二氧化锰可以做任何化学反应的催化剂
D.C、H2、CO都具有还原性,在一定条件下它们都能跟氧化铁发生置换反应
下表列出了部分元素的原予结构示意图。下列叙述不正确的是
| A.硫原子在化学反应中易得到电子 |
| B.O2-的核外电子总数为10 |
| C.由镁元素和硫元素组成化合物的化学式为Mg2S |
| D.氧元素和硫元素化学性质具有相似性的原因是它们的原子最外层的电子数相同 |
地质考察人员发现一种带螺纹的矿石,研究时发现该矿石能在氧气中燃烧,主要反应是4X+11O2 2Fe2O3+8SO2。下列有关说法中不正确的是
2Fe2O3+8SO2。下列有关说法中不正确的是
| A.X的化学式是FeS2 |
| B.FeS2是由铁元素和硫元素组成 |
| C.反应前后氧元素的化合价发生改变 |
| D.SO2中的硫、氧元素的个数比为1:2 |
下列事实的结论或解释中不正确的是
| A.铝制品有抗腐蚀性能——实质是表面生成了致密氧化膜起保护作用 |
| B.公园的桂花开放时满园飘香——说明分子在不断运动 |
| C.酸碱中和反应都能生成水—一实质是H+与OH-结合生成了H2O |
| D.化肥硫酸铵不能和熟石灰混放或混用——硫酸铵和熟石灰发生中和反应 |
鉴别下列各组物质,所用两组试剂均正确的是
| |
待鉴别的物质 |
鉴别试剂1 |
鉴别试剂2 |
| A |
稀盐酸和稀硫酸 |
氯化钡溶液 |
碳酸钠溶液 |
| B |
硝酸铵固体和氢氧化钠固体 |
熟石灰 |
水 |
| C |
氯化铵和氯化钾 |
硝酸银溶液 |
熟石灰 |
| D |
氧气、二氧化碳 |
燃着的木条 |
澄清石灰水 |
除去下列物质中少量的杂质,正确的是
| 选项 |
溶液 |
杂质 |
试剂 |
| A |
NaNO3溶液 |
Na2CO3溶液 |
过量Ba (NO3)2溶液 |
| B |
CaCl2溶液 |
稀盐酸 |
足量CaCO3固体 |
| C |
氢气 |
氯化氢 |
先通过过量NaOH溶液,再通过过量浓硫酸 |
| D |
Fe2(SO4)3溶液 |
Na2SO4溶液 |
适量NaOH溶液 |
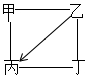
下表中“—”表示相连的物质间能发生反应,“→”表示这种物质可转化为另一种物质。甲、乙、丙、丁四种物质不符合对应“转化关系”的是
| 选项 |
A |
B |
C |
D |
|
| 转化关系 |
 |
 |
 |
 |
|
| 物质 |
甲 |
C |
Na2CO3 |
Ca(OH)2 |
Fe |
| 乙 |
O2 |
Ca(OH)2 |
HCl |
HCl |
|
| 丙 |
CuO |
NaCl |
CO2 |
CuCl2 |
|
| 丁 |
CO |
H2SO4 |
NaOH |
NaOH |
有一包白色粉末,可能由氯化钠、硫酸钠、硫酸铜、碳酸钠、碳酸钙中的一种或几种组成,为确定其组成,进行如下实验:
①称取一定质量的该白色粉末加足量水溶解,得无色溶液A.
②在无色溶液A中加入过量氯化钡溶液,充分反应后过滤,分别得无色溶液B和白色沉淀C;将白色沉淀C洗涤,烘干后称得质量为20g.
③在20g白色沉淀C中加入足量的稀硝酸,沉淀部分消失,并有气泡冒出.
④在无色溶液B中滴加硝酸银溶液和稀硝酸,产生白色沉淀.
由上述实验得出的下列判断中,不正确的是
A.白色粉末中一定含有氯化钠
B.无色溶液B中一定含有两种溶质
C.白色粉末中不含碳酸钙、硫酸钠、硫酸铜
D.步骤③生成的气体质量可能是4.4g
化学与生活息息相关。现有水、氮气、甲烷、干冰、碳酸钙等五种物质,对应物质的化学式填空:
(1)钟乳石的主要成分是 .
(2)天然气的主要成分是 .
(3)可用于人工降雨的是 .
(4)充入食品包装袋内用于防腐的是 .
(5)生命的孕育和维系需要的氧化物是 .
(7)化学是在原子、分子水平上研究物质和创造物质。
(1)甲和乙在一定条件下反应生成丙和丁,结合微观示意图分析:
上述物质中属于氧化物的是 (填序号);发生反应的甲和乙的质量比为 。
(2)在氨气,镁和氯化钠三种物质中,由离子构成的物质是 (填化学式);保持氨气化学性质的最小粒子是 (填化学式)。工业制镁的一种原理是氧化镁和硅和氧化钙在真空环境下加热至1600℃反应生成镁单质和硅酸钙(Ca2SiO4)。写出此反应的化学方程式: ,抽走容器中的空气对反应有促进作用,且能防止空气中的物质与Mg反应使产品混有 (填化学式).
如图是甲、乙、丙三种固体物质的溶解度曲线,请回答: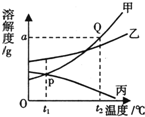
(1)t2℃时,甲、乙、丙三种物质的溶解度由小到大的顺序是 .
(2)若将甲物质的不饱和溶液变为饱和溶液,下列说法不正确的是 (填写字母)。
A.溶剂的质量一定变小
B.溶质的质量可能不变
C.溶质的质量分数一定变大
D.溶液的质量一定变大
E.该饱和溶液还可以溶解其他物质
(3)将t2 ℃时,甲、乙、丙三种物质的饱和溶液,都降温至tl℃时,所得溶液的溶质质量分数由大到小的顺序是
(4)若甲物质溶液中混有少量的乙物质,提纯甲物质可采取的方法是
(5)对(4)析出的晶体和剩余溶液描述不正确的是 (填写字母)
A.剩余溶液一定是甲饱和溶液 B.剩余溶液一定不含有乙
C.剩余的溶液一定是纯净物 D.析出的晶体中只含有甲
写出下列反应的化学方程式:
(1)磷在空气中燃烧: 。
(2)高锰酸钾受热分解: 。
(3)碳酸氢钠和稀盐酸混合 。
实验室有两瓶失去标签的稀盐酸和氢氧化钠溶液(记作A、B),小强用下列方法鉴别,回答下列问题.
(1)他取适量的A、B两种溶液于试管中,分别加入适量氯化铁溶液,观察到A中产生红褐色沉淀,则A是 ,(填化学式)发生反应的化学方程式为 。
(2)他另取适量的A、B两种溶液于试管中,分别加入适量碳酸钠溶液,观察到B中的现象为 ,发生反应的化学方程式为 。
(3)他通过测定溶液的酸碱度来鉴别:若pH 7,则溶液为 (填名称)
(4)他还利用了下列试剂进行鉴别,其中能鉴别的试剂是 .(填字母)
A.锌 B.硫酸铜溶液 C.硝酸钠溶液 D.酚酞试液
金属与我们生活息息相关.
(1)铁锅用来做饭是利用了铁的 性.
(2)已知金属锰在金属活动性顺序中位于铝和锌之间。下列化学反应能发生的是 (填字母)
| A.Mn+2HCl=MnCl2+H2↑ | B.Mg+MnSO4=MgSO4+Mn |
| C.Fe+MnSO4= FeSO4+Mn | D.Mn+CuSO4 =MnSO4+Cu |
(3)某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,则:
①溶液甲中一定含有Al (NO3)3和Zn (NO3)2
②固体乙中一定含有Ag,可能含有Cu和Zn
③若溶液甲是蓝色,则溶液甲一定含有Al(NO3)3、Zn(NO3)2和Cu(NO3)2
④向固体乙上滴加盐酸有气泡产生,则溶液甲中一定没有AgNO3和Cu (NO3)2
上述四种说法正确的 (填序号)。
(4)为探究工业废水的综合利用,某化学小组在实验室中完成了以下实验。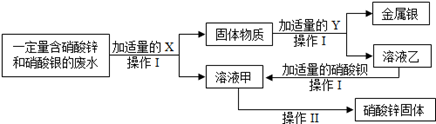
①x为 ;乙与硝酸钡反应的化学方程式为 。
②操作I和操作II中都要用到一种玻璃仪器。该仪器在操作II中的作用是 。
根据下列装置图回答问题.
(1)实验室制取较纯净的氧气时,可选择图中的 装置(填字母)。进行此实验,加试剂前,连接装置并检查装置的 。
(2)写出实验室用锌与稀硫酸制取氢气的化学方程式 。点燃氢气前 。
(3)实验室制取二氧化碳气体时,可选择图中的 装置(填字母)。为了确定反应后的溶液里含有CaCl2,张林同学向溶液中滴加少许Na2CO3溶液,结果没有观察到白色沉淀,你推测是 (填物质名称)的干扰。
(4)如果氧气不足,乙醇燃烧还可能生成CO。若乙醇燃烧产物中的CO和CO2的总质量为25.2g,其中碳元素和氧元素的质量比是2:5,则参加反应的乙醇的质量是 g。
农业生产上常需要用质量分数为12%的氯化钠溶液选种。下图是小军实验操作过程示意图:
(1)图中一处明显错误的操作是 (填序号),改正操作后,用上述图示的序号表示配制溶液的正确操作顺序 。
(2)现配制100kg这种溶液,需氯化钠 kg;
(3)现用质量分数为12%的氯化钠溶液(密度约为l.09g/cm3),配制50g质曼分数为6%的氯化钠溶液。需要质量分数12%的氯化钠溶液 mL(计算结果精确到0.l),需要水 mL(水的密度为1g/cm3)。
(4)20℃时,向50g水中加入20g氯化钠,充分溶解后,得到溶液的质量为68g,则20℃时,氯化钠的溶解度为 g.
A~F是初中化学常见的六种物质,它们之间的关系如下图所示。“→”表示物质间的转化关系,“——”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出)。A可以与酸、碱、盐三类物质发生反应,D是食盐的主要成分,C和F都是无色气体,反应①和②都有白色沉淀生成。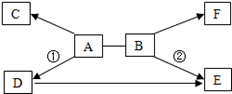
(1)F的化学式为 ,C的化学式 ;
(2)写出B→E反应的化学方程式 ;
(3)写出A与一种碱反应的化学方程式 。
二氧化碳是一种宝贵的碳氧资源。以CO2和NH3合成尿素CO(NH2)2是固定和利用CO2的成功范例,该反应的化学方程式为CO2+2NH3=CO(NH2)2+H2O。
请计算:
(1)尿素中C、O、N、H四种元素的质量比 ;
(2)尿素中含氮元素的质量分数为 ;
(3)若按上述方法生产150 t纯度为80%尿素,可固定的CO2的质量为 。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号