高考原创化学预测卷 08(广东卷)
下列说法正确的是
A.乙酸的结构简式为 分子中含有两种官能团 分子中含有两种官能团 |
| B.油脂是食物组成中的重要部分,也是产生能量最高的营养物质 |
| C.三大营养物质糖类、油脂、蛋白质均能发生水解反应 |
| D.95%的酒精常用于医用消毒剂 |
下列体系中,离子或分子能大量共存的是
| A.甲基橙呈红色的溶液中:MnO4-、Al3+、C2H5OH、SO42- |
| B.FeCl3溶液中:K+、C6H5OH、NO3-、Br- |
| C.0.1 mol·L-1NaAlO2溶液:K+、Na+、CO32-、OH- |
| D.加入镁粉产生氢气的溶液:Na+、NH4+、NO3-、Cl- |
下列叙述I和II均正确且具有因果关系的是
| 编号 |
叙述I |
叙述II |
| A |
碘易溶在有机溶剂中 |
可以用酒精萃取碘水中的碘 |
| B |
纯净的硅单质具有导电性 |
高纯度的硅可以用光导纤维 |
| C |
碳酸、氨水能够导电 |
液氨、二氧化碳是电解质 |
| D |
铝具有强还原性 |
通过铝热反应冶炼某些高熔点金属 |
设NA为阿伏伽德罗常数的数值。下列说法正确的是
| A.在含Fe3+总数为NA的FeCl3溶液中,Cl-总数为3NA |
| B.标准状况下,2.24L异丁烷分子中含有共价键的数目为1.3NA |
| C.6.4g铜与硫分反应,电子转移总数为0.2 NA |
| D.常温下,0.1L pH=1的H2SO4溶液中含有H+的数目为0.02NA |
一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示。以下说法不正确的是
| A.左侧是阴离子交换膜 |
| B.X气体为O2 |
| C.右侧电极反应式为2NO3-+12H++10e-=N2↑+6H2O |
| D.若有机物用C6H10O5表示,则电路中每通过4mol电子,产生标准状况下X的体积为22.4L |
下列溶液中粒子的物质的量浓度关系正确的是
| A.0.l mol·L-1的KHCO3溶液中:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| B.已知在相同条件下酸性HF > CH3COOH,则物质的量浓度相等的NaF与CH3COOK溶液中:c(Na+)-c(F-) >c(K+)-c(CH3COO-) |
| C.某溶液中存在的离子有S2—、HS—、OH—、Na+、H+,则离子浓度的大小关系一定是:c(Na+)>c(S2—)>c(OH—)>c(HS—)>c(H+) |
| D.CH3COONa溶液和盐酸混合呈中性的溶液中:c(Na+)>c(Cl-)=c(CH3COOH) |
X、Y、Z、W、M五种元素的原子序数依次增大。已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素。下列说法错误的是
| A.Z、W、M三种元素的离子半径从大到小的顺序是:Z>W>M |
| B.Y能分别与X、W元素形成相对分子质量相等的化合物 |
| C.Z与W形成的化合物只有5种 |
| D.用M单质作阳极,石墨作阴极电解NaHCO3溶液,电解一段时间后,在阴极区会出现白色沉淀 |
下列实验操作能达到其对应目的的是
| 序号 |
实验内容 |
实验目的 |
| A |
向盛有10滴0.1mol/LAgNO3溶液的试管中滴加0.1mol/LNaCl溶液,至不再有沉淀生成,再向其中滴加0.1mol/LNa2S溶液 |
证明AgCl沉淀能转化为溶解度更小的Ag2S沉淀 |
| B |
将少量某物质的溶液滴加到新制的氢氧化铜悬浊液中,加热后产生红色沉淀 |
证明该物质一定属于醛类 |
| C |
向Na2SiO3溶液中通入SO2 |
证明硫元素的非金属性强于硅 |
| D |
在淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入几滴碘水 |
验证淀粉已完全水解 |
5-氯-2,3-二氢-1-茚酮是是一种重要的医药中间体。
已知:
以化合物A(分子式为C7H7Cl)为原料合成5-氯-2,3-二氢-1-茚酮(化合物F)工艺流程如下:

(1)写出A结构简式 ,反应E→F的反应类型 。
(2)化合物B中加入足量的氢氧化钠水溶液,在高温高压的条件并加合适的催化剂(所有卤素原子参与水解)反应的方程式 。
(3)某化合物是D的同分异构体,能使FeCl3溶液显紫色,且分子中只有3种不同化学环境的氢。写出该化合物的结构简式: (任写一种)。
(4)E→F的转化中,会产生一种与F互为同分异构体的副产物,其结构简式为 。
(5)根据已有知识并结合相关信息,写出以化合物F和CH2(COOC2H5)2为有机反应原料制备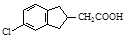 的合成路线流程图(注明反应条件)。合成路线流程图示例如下:
的合成路线流程图(注明反应条件)。合成路线流程图示例如下:

能源、环境与人类生活和社会发展密切相关,研究它们的综合利用有重要意义。
Ⅰ、煤可以通过气化和液化转变为清洁能源并提高燃烧效率。
煤气化的主要反应是:C(g)+ H2O(g) CO(g)+H2(g)。
CO(g)+H2(g)。
气化得到的CO和H2可以进一步液化合成甲醇,反应方程式为:
CO(g)+2H2(g) CH3OH(g) ∆H
CH3OH(g) ∆H
(1)若相同温度下CO、H2、CH3OH(g)的燃烧热(∆H)分别为a、b、c,则上述反应的∆H= 。
(2)将1molCO和2molH2通入1L密闭容器中,分别恒温在3000C和5000C反应,每隔一定时间测得容器中甲醇的浓度如下:
| |
10min |
20min |
30min |
40min |
50min |
60min |
| 3000C |
0.40 |
0.60 |
0.75 |
0.84 |
0.90 |
0.90 |
| 5000C |
0.60 |
0.75 |
0.78 |
0.80 |
0.80 |
0.80 |
①在3000C反应开始10分钟内,H2的平均反应速率_____________。
②5000C平衡常数K=___________。
③在另一体积不变的容器中,充入1.2molCO和2.0molH2,一定条件下达到平衡,测得容器内压强为起始的一半。计算该条件下H2转化率为 。
(3)煤燃烧的主要产物CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其KSP=2.8×10-9mol2/L2。现将2×10-4mol/L的Na2CO3溶液与一定浓度的CaC12溶液等体积混合生成沉淀,计算应加入CaC12溶液的最小浓度为 。
Ⅱ、超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO十2CO 2CO2+ N2 △H
2CO2+ N2 △H
某温度下用气体传感器测得不同的时间的NO和CO浓度如下表:
| 时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
| c(NO)(×10-4mol/L) |
10.0 |
4.50 |
2.50 |
1.50 |
1.00 |
1.00 |
| c(CO)( ×10-3mol/L) |
3.60 |
3.05 |
2.85 |
2.75 |
2.70 |
2.70 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H 0(填写“>”、“<”、“=”);
(2)某同学设计了三组实验,分别验证温度、催化剂比表面积对化学反应速率的影响规律,部分实验条件如下表:
| 实验编号 |
T/℃ |
NO初始浓度/mol·L-1 |
CO初始浓度/mol·L-1 |
催化剂的比表面积/m2·g—1 |
| I |
280 |
1.2×10—3 |
5.8×10—3 |
82 |
| Ⅱ |
280 |
1.2×10—3 |
5.8×10—3 |
124 |
| Ⅲ |
350 |
1.2×10—3 |
5.8×10—3 |
124 |
该同学画出了表中三个实验条件下,混合气体中NO浓度随时间变化的趋势曲线图,请在图上标明各条曲线的实验编号。

工业上以锂辉石(Li2O·Al2O3·4SiO2,含少量Ca,Mg元素)为原料生产碳酸锂。其部分工业流程如下: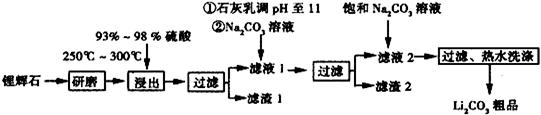
已知:①Li2O·Al2O3·4SiO2 + H2SO4(浓) Li2SO4 + Al2O3·4SiO2·H2O
Li2SO4 + Al2O3·4SiO2·H2O
②某些物质的溶解度(S)如下表所示。
| T/℃ |
20 |
40 |
60 |
80 |
| S(Li2CO3)/g |
1.33 |
1.17 |
1.01 |
0.85 |
| S(Li2SO4)/g |
34.2 |
32.8 |
31.9 |
30.7 |
(1)从滤渣1中分离出Al2O3部分的流程如下图所示,括号表示加入的试剂,方框表示所得的物质。则步骤Ⅱ中反应的离子方程式是______________________________。
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3。向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)_____________________________。
(3)最后一个步骤中,用“热水洗涤”的目的是______________________________。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下:
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液做阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入少量NH4HCO3溶液并共热,过滤、烘干得高纯Li2CO3。
①a中,阳极的电极反应式是_________________________。
②电解后,LiOH溶液浓度增大的原因_____,b中,生成Li2CO3反应的化学方程式是_______。
(5)磷酸亚铁锂电池总反应为:FePO4+Li LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:__________________。若用该电池电解饱和食盐水(电解池电极均为惰性电极)当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为__________________。
LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:__________________。若用该电池电解饱和食盐水(电解池电极均为惰性电极)当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为__________________。
某化学探究小组拟用废铜屑制取Cu(NO3)2,并探究其化学性质。
I.如图,用浓HNO3,和过量的废铜屑充分反应制硝酸铜溶液。

(1)写出铜与浓硝酸反应的离子方程式 。
(2)①装置中NaOH溶液的作用是 。
②欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤是蒸发浓缩、 、过滤。
③你认为此装置是否合理,并说明原因 。
如果不合理,同时在原装置上改进;如果合理,只需说明原因。
Ⅱ.为了探究Cu(NO3)2的热稳定性,探究小组按下图装置进行实验。(图中铁架台、铁夹和加热仪器均略去)
【实验装置】

【实验操作及现象】往试管中放入研细的无水Cu(NO3)2晶体并加热,观察到试管中有红棕色气体生成,最终残留黑色粉末;用U型管除去红棕色气体,在集气瓶中收集到无色气体。
【解释与结论】
(3)①红棕色气体是 。
②根据现象判断Cu(NO3)2在加热条件下可以分解,其化学反应方程式为 。
Ⅲ.利用Cu(NO3)2制备浅绿色的碱式碳酸铜[CuCO3·Cu(OH)2]。
向大试管中加入一定量的碳酸钠溶液和硝酸铜溶液,水浴加热,用0.4mol/L的NaOH溶液调节pH至8.5,振荡、静置、过滤、洗涤、干燥,得到样品。
【实验数据】反应温度对样品的影响
| 实验序号 |
1 |
2 |
3 |
4 |
| 温度/℃ |
35 |
50 |
70 |
95 |
| 样品颜色 |
深蓝色 |
深蓝色 |
浅绿色 |
暗蓝色 |
| 样品中碱式碳酸铜 的质量分数/% |
90.9 |
92.7 |
x |
92.0 |
(4)滤液中可能含有CO32—,写出检验CO32—的方法 。
(5)95℃时,样品颜色发暗的原因:____ 。
(6)70C时,实验得到2.38 g样品,取此样品加热至分解完全(杂质不分解),得到1.76 g固体,此样品中碱式碳酸铜的质量分数是 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号