浙江省台州市高三3月调研考试理综化学试卷
下列说法不正确的是
A.合成氨反应在低温下能够自发进行,是因为反应物键能之和大于生成物键能之和
B.元素分析仪可以确定物质中是否含有C、H、O、N、S、Cl、Br等元素,原子吸收光谱可以确定物质中含有哪些金属元素
C.人们利用元素周期律在过渡元素中寻找各种性能优良的催化剂,以降低化学反应的活化能,从而起到很好的节能效果
D.超高分辨率荧光显微镜能够观察到纳米尺度的物质,用它可以获得蛋白质溶液中的分子图像
下列说法不正确的是
| A.在粗盐提纯中,当加热到蒸发皿中有较多固体析出,残留少量液体时,停止加热,用余热将液体蒸干 |
| B.当振荡分液漏斗中的混合溶液时,须用一只手压住分液漏斗的玻璃塞,另一只手握住旋塞,将分液漏斗倒转过来,用力振荡 |
| C.从加碘盐中获取碘单质的操作步骤为:溶解—萃取—分液—蒸馏 |
| D.实验过程中若皮肤不慎沾上少量碱液,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗 |
短周期元素X、Y、Z、W、M的原子序数依次增大,X、Z同主族,Z、W、M同周期,其中X与Y能形成两种物质,且常温下均为液体。W的氧化物既能溶于强碱溶液,又能溶于X、M形成的水溶液。已知W与M形成的物质在178°C时升华。下列说法不正确的是
| A.Z、W、M的原子半径由大到小的顺序为Z>W>M |
| B.M分别与Z、W所形成的物质的晶体类型相同 |
| C.X2Y2易溶于X2Y中,是由于X2Y2与X2Y能形成分子间氢键 |
| D.将Z2Y在空气中加热可得到Z2Y2 |
下列说法正确的是
A.按系统命名法,化合物 的名称为2-甲基-3-乙基丁烷 的名称为2-甲基-3-乙基丁烷 |
| B.甲醇、乙醇、甘油互为同系物 |
C.等物质的量的乙炔、乙醛、 完全燃烧时耗氧量不相等 完全燃烧时耗氧量不相等 |
| D.以乙烯为原料制备乙酸乙酯的合成路线可以为: |

化学镀铜废液中含有一定量的CuSO4,任意排放会污染环境,利用电化学原理可对废液进行回收处理,装置如图,其中质子交换膜只允许H+通过。已知:①Cu2++ HCHO + 3OH-=Cu + HCOO-+ 2H2O;②还原性:HCHO > M(—种金属)> Cu。
下列说法正确的是
| A.反应之前,应将含OH-的HCHO溶液加人到装置的左侧 |
| B.右侧发生的电极反应式:HCHO-2e-+H2O=HCOO-+3H+ |
| C.若将质子交换膜换成阴离子交换膜,放电过程中,大量的OH-将向左侧迁移 |
| D.放电一段时间后打开开关,移去质子交换膜,装置中可能会有红色固体、蓝色絮状物出现 |
在25°C时,向10mL0.0lmol·L-1NaCN溶液中逐滴加人0.0lmol·L-1的盐酸,滴定曲线如图1所示,CN—、HCN浓度所占分数(α)随pH变化的关系如图2所示,下列表述正确的是 
| A.b点时,溶液中微粒浓度大小的关系:c(CN-)>c(Cl-)>c(HCN)>c<(OH-)>c(H+) |
| B.d点溶液存在的关系:c(Na+)+c(H+)=c(HCN)+c(OH-)+2c(CN-) |
| C.图2中的e点对应图1中的c点 |
| D.在滴定过程中选用酚酞试剂比选用甲基橙试剂作指示剂误差更小 |
某溶液中可能含有Na+、K+、AlO2-、CO32-、SO32-、Cl-中的若干种离子。某同学设计并完成了如下实验:
已知:AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-
根据以上的实验操作与现象,该同学得出的结论不正确的是
| A.沉淀2放置在空气中,若质量增加,试样中肯定存在SO32- |
| B.试样溶液中加人稍过量的NH4C1溶液能得到与沉淀1成分相同的物质 |
| C.上述流程步骤(1)(2)(3)的顺序改为(3)(2)(1),可能会获得相同的实验现象 |
| D.试样溶液中肯定存在AlO2-、Cl-,其中Na+、K+至少存在1种 |
(10分)以苯为原料合成高分子化合物I的路线如下:
已知有机物的化学性质主要由官能团决定。请回答下列问题:
(1)含有的官能团名称为______;I的结构简式为____。
(2)写出A→B反应的化学方程式:___________;E+F→G的反应类型为____。
(3)写出H与NaOH溶液在加热条件下反应的化学方程式____。
(18分)
Ⅰ.浓硝酸与浓盐酸混合过程中会产生少量的气体单质X、化合物M和无色液体,化合物M中所有原子均达到8电子的稳定结构。2molM加热分解生成lmol X和2mol无色气体Y,Y遇到空气呈现红棕色。
(1)镁与气体X反应产物的电子式为________。
(2)浓硝酸和浓盐酸反应的化学方程式为________。
(3)化合物M水解生成两种酸,为非氧化还原反应,该反应的化学方程式为________。
Ⅱ.石油铁储罐久置未清洗易引发火灾,经分析研究,事故由罐体内壁附着的氧化物甲与溶于石油中的气态氢化物乙按1:3反应生成的黑色物质丙自燃引起。某研究小组将一定量的丙粉末投人足量的浓盐酸中发生反应,得到4.8g淡黄色沉淀和气体乙,乙在标准状况下的密度为1.5179g/L,过滤后向滤液(假设乙全部逸出)中加人足量的NaOH溶液,先出现白色沉淀,最终转变为红褐色沉淀,过滤、洗涤、灼烧后的固体质量为24g,已知气体乙可溶于水。请回答下列问题:
(1)甲的化学式为________。
(2)写出丙中非金属元素的离子结构示意图________。
(3)丙在盐酸中反应的化学方程式:________。(离子方程式表示)
(4)请设计合理的实验方案验证不同温度对丙与盐酸反应速率的影响
(5)为消除火灾隐患,下列措施可行的是________。
| A.石油入罐前脱硫 |
| B.定期用酸清洗罐体 |
| C.罐体内壁涂刷油漆 |
| D.罐体中充入氮气 |
(15分)二氧化碳的过度排放会引发气候问题,而进行有效利用则会造福人类,如以CO2和NH3 为原料合成尿素。经研究发现该反应过程为:
①CO2(g)+2NH3(g) NH2COONH4(s) △H1
NH2COONH4(s) △H1
②NH2COONH4(s) CO(NH2)2(s)+H2O(g) △H2>0
CO(NH2)2(s)+H2O(g) △H2>0
请回答下列问题:
(1)研究反应①的平衡常数(K)与温度(T)的关系,如图1所示,则△H1____0。(选填“>”、“<”或“=”)。
(2)有体积可变(活塞与容器之间的摩擦力忽略不计)的密闭容器如图2所示,现将3molNH3和2molCO2放入容器中,移动活塞至体积V为3L,用铆钉固定在A、B点,发生合成尿素的总反应如下:
CO2(g)+2NH3(g) CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)
测定不同条件、不同时间段内的CO2的转化率,得到如下数据:
| CO2的转化率T(℃) |
10min |
20min |
30min |
40min |
| T1 |
30% |
65% |
75% |
75% |
| T2 |
45% |
50% |
a1 |
a2 |
①T1℃下,l0min内NH3的平均反应速率为__________。
②根据上表数据,请比较T1_________T2(选填“>”、“<”或“=”);T2℃下,第30min时,a1=________,该温度下的化学平衡常数为_________。
③T2℃下,第40min时,拔去铆钉(容器密封性良好)后,活塞没有发生移动,再向容器中通人3molCO2,此时v(正)_____v(逆)(选填“>”、“<”或“=”),判断的理由是______。
(3)请在下图中补画出合成氨总反应2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)过程中能量变化图,并标明中间产物〔NH2COONH4(s)〕、 生成物CO(NH2)2(s)+H2O(g)〕。
CO(NH2)2(s)+H2O(g)过程中能量变化图,并标明中间产物〔NH2COONH4(s)〕、 生成物CO(NH2)2(s)+H2O(g)〕。
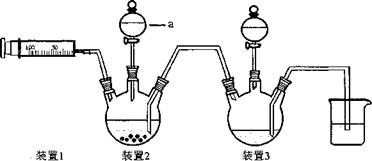
(15分)二氯化一氯五氨合钴([Co(NH3)5C1]C12,M=250.5g·mol-1,紫红色固体)因在离子鉴定、电镀、医学方面的广泛应用受到人们的关注,它不溶于乙醇,难溶于水。实验室制备二氯化一氯五氨合钴的流程及装置如下: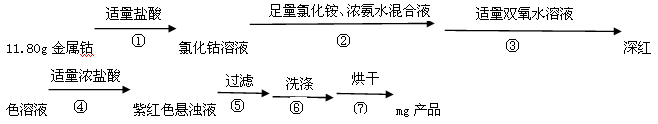
相关信息:
Co+2HCl=CoCl2+H2↑ [Co(NH3)5C1]2++H2O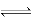 [Co(NH3)5H2O]3++Cl-
[Co(NH3)5H2O]3++Cl-
(深红色)
请回答下列问题:
(1)写出仪器a的名称_____;向装置2中加入适量盐酸后,关闭活塞进行第①步反应,如何通过装置1判断该反应已经完全_____;在不添加其他试剂的前提下,如何操作能够实现第②步反应_____。
(2)第③步加入双氧水的作用是_____;第④步加入适量浓盐酸的作用是_____。
(3)第⑥步洗涤操作为:先用冷水洗涤,再用乙醇洗涤。其中乙醇洗涤的目的是_____。
(4)第⑦步烘干操作的温度应控制在100-160℃,温度不能过低也不能过高的可能原因是_____。
(5)将产品分为10等份,取其中一份于强碱溶液中,加热煮沸,蒸出所有氨气后,向溶液中加酸中和,然后加人0.5000mol·L-1的KI溶液0.04000L(过量),滴加指示剂,用0.l000mol·L-1Na2S2O3溶液滴定,达到终点消耗0.1200LNa2S2O3标准溶液,则该实验的产率为_____。(2Co3++2I-=2Co2++I2;2S2O32-+I2=S4O62-+2I-)
 粤公网安备 44130202000953号
粤公网安备 44130202000953号