河北省唐山市高三上学期期末理综化学试卷
下列说法或表达正确的是
| A.乙醇、糖类和蛋白质都是人体必需的营养物质 |
B.NH4I的电子式: |
| C.石油是混合物,其分馏产品汽油也是混合物 |
| D.陶瓷、水晶、水泥、玻璃都属于硅酸盐 |
用下列实验装置和方法进行相应实验,能达到实验目的的是
| A.用甲装置制干燥的氨气 |
| B.用乙装置收集并测量Cu与浓硝酸反应产生的气体及体积 |
| C.用丙装置除去CO2中含有的少量HC1 |
| D.用丁装置吸收NH3,并防止倒吸 |
有机物C4H8Cl2的结构中只含有一个甲基的同分异构体有几种(不考虑立体异构)
| A.3 | B.4 | C.7 | D.8 |
设NA为阿伏加德罗常数,下列叙述中正确的是
| A.足量铁在氯气中反应,l mol铁失去的电子数为2 NA |
| B.标准状况下22.4 L H2中含中子数为2 NA |
| C.1 L Imol/L的盐酸溶液中,所含氯化氢分子数为NA |
| D.常温下46 g NO2和N2O4混合气体中含有原子数为3NA |
短周期四种元素离子W2+、X-、Y2-、Z+的电子层结构相同。下列说法正确的是
| A.原子序数:W>Z>X>Y |
| B.离子半径:r(W2+)>r(X一)>r(Y2-)>r(Z+) |
| C.Y的气态氢化物比X的气态氢化物稳定 |
| D.氢氧化物碱性强弱:W(OH)2>ZOH |
镁是海水中含量较多的金属,镁合金及其镁的化合物用途非常广泛。
(1)Mg2Ni是一种储氢合金,已知:
Mg(s)+H2(g)=MgH2(S) △H1="-" 74.5kJ·mol-1
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) △H2="-" 64.4kJ·mol-l
则:Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s)的△H3= .
(2)某科研小组用水氯镁石(主要成分为MgCl2·6H2O)制备金属镁工艺的关键流程如下: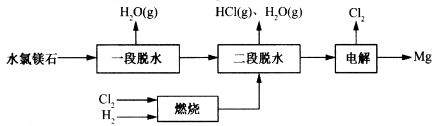
科研小组将MgCl2·6H2O在氩气气氛中进行热重分析,结果如下图(TG表示残留固体质量占原样品总质量的百分数)。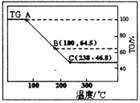
①图中AB线段为“一段脱水”,试确定B点对应固体物质的化学式____ ;图中BC线段为“二段脱水”,在实验中通入H2和Cl2燃烧产物的目的是 。
②该工艺中,可以循环使用的物质有___ 。
(3)CH3MgCl是一种重要的有机合成剂,其中镁的化合价是 ,该化合物水解时生成甲烷、氯化镁和氢氧化镁,请写出该反应的化学方程式 。
(4)储氢材料Mg(AIH4)2在110~200℃的反应为:Mg(AIH4)2=MgH2+2Al+3H2↑;每转移3 mol电子生成Al的质量为____ 。
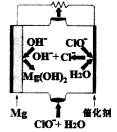
(5)“镁一次氯酸盐”燃料电池的装置如右图所示,该电池的正极反应式为 。
节能减排是当下环境保护的重点。
(1)将CO和气态水通入一个体积固定的密闭容器中,在一定条件下发生如下可逆反应:
CO(g)+H2O(g) CO2(g)+H2(g),△H<0
CO2(g)+H2(g),△H<0
800℃,在2L恒容密闭容器中,起始时按照下表数据进行投料,达到平衡状态,K=1.0。
①从起始经过5 min达到化学平衡时,用生成物CO2表示该反应的反应速率v(CO2)= ;平衡时,容器中CO的转化率为 。
②下图表示上述反应在tl时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况。则t2时刻发生改变的条件可能是 。(写出一条)
(2)汽车尾气中的一氧化碳是大气污染物,可通过反应:
CO(g)+l/2O2(g) CO2(g)降低其浓度。
CO2(g)降低其浓度。
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示。请在表中的空格处填写“>"“<”或“="。
②相同温度下,某汽车尾气中CO、CO2的浓度分别为l.0×10-5mol/L和1.0×l0-4mol/L。若在汽车的排气管上增加一个补燃器,不断补充O2并使其浓度保持为1.0×l0-4mol/L,则最终尾气中CO的浓度为 mol/L(请保留两位有效数字)。
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其KSp=2.8×l0-9。现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×l0-4mol/L,则生成CaCO3沉淀所需CaCl2溶液的最小浓度为 mol/L。
对叔丁基苯酚 工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚。实验步骤如下:反应物和产物的相关数据列表如下:
工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等。实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚。实验步骤如下:反应物和产物的相关数据列表如下:
步骤l:组装仪器,用量筒量取2.2 mL叔丁基氯(过量),称取1.6 g苯酚,搅拌使苯酚完全溶解,并装入滴液漏斗。
步骤2:向X中加入少量无水AlCl3固体作催化剂,打开滴液漏斗旋塞,迅速有气体放出。
步骤3:反应缓和后,向X中加入8 mL水和1 mL浓盐酸,即有白色固体析出。
步骤4:抽滤得到白色固体,洗涤,得到粗产物,用石油醚重结晶,得对叔丁基苯酚1.8 g。
(1)仪器X的名称为 。
(2)步骤2中发生主要反应的化学方程式为 。该反应过于激烈,放出大量热,常使实验的产率降低,可能的原因是 。
(3)图中倒扣漏斗的作用是 。苯酚有腐蚀性,能使蛋白质变性,若其溶液沾到皮肤上可用 洗涤。
(4)在取用苯酚时发现苯酚冻结在试剂瓶中,可采取的措施为____ 。
(5)下列仪器在使用前必须检查是否漏液的是 (填选项字母)。
| A.量筒 |
| B.容量瓶 |
| C.滴定管 |
| D.分液漏斗 |
E.长颈漏斗
(6)本实验中,对叔丁基苯酚的产率为 。(请保留三位有效数字)
【化学——选修2化学与技术】
红矾钠(重铬酸钠:Na2Cr2O7·2H2O)是重要的基本化工原料,应用领域十分广泛。
(1)实验室中红矾钠可用铬铁矿(主要成分:FeO·Cr2O3)利用以下过程来制取。
①步骤I中反应的化学方程式为:4FeO·Cr2O3(s)+8Na2CO3(s)+7O2= 8Na2CrO4(s)+2Fe2O3(s)+8CO2
该反应的化学平衡常数的表达式为 。在常温下该反应速度极慢,下列措施中能使反应速率增大的是 。
| A.升高温度 | B.通入过量的空气 |
| C.将原料粉碎 | D.增加纯碱的用量 |
②步骤II中所得溶液显碱性,其中除含有Na2C rO4外还含有铝、硅元素的化合物,它们的化学式可能是 。
③步骤III需将溶液的pH调至7~8并煮沸,其目的是 。
④步骤Ⅳ中发生反应的离子方程式为:____。
(2)将红矾钠与KC1固体1:2(物质的量比)混合溶于水后经适当操作可得到K2Cr2O7晶体,反应方程式为:Na2CrO4 +2KCl= K2Cr2O7 +2NaCl(已知NaCl的溶解度受温度影响小,K2Cr2O7的溶解度受温度影响大),基本实验步骤为:①溶解;② ;③____ 。
④冷却、结晶,过滤,得到K2Cr2O7晶体。
【化学——选修3物质结构与性质】已知A、B、C、D、E、F为前四周期的六种元素,原子序数依次增大,其中A位于周期表的s的区,其原子中电子层数和未成对电子数相同;B原子价电子排布式为nsnnpn,B和E同主族,D原子的最外层电子数是其内层的3倍;F元素位于元素周期表的第四行、第十一列。试回答下列问题:
(1)基态F原子的核外电子排布式为 。
(2)关于B2A2的下列说法中正确的是____ (填选项序号)。
①B2A2中的所有原子都满足8电子稳定结构
②每个B2A2分子中 键和
键和 键数目比为1:1
键数目比为1:1
③B2A2是由极性键和非极性键构形成的非极性分子
④B2A2中心原子的杂化类型为sp杂化
(3)B、C、D三种元素第一电离能按由大到小的顺序排列为 (用元素符号表示)。
(4)C的气态氢化物与C的最高价氧化物对应的水化物反应生成一种盐H,H晶体中存在的化学键类型
有____(填选项序号)。
①离子键 ②共价键 ③氢键 ④配位键 ⑤金属键
(5)基态E原子的最高能层具有的原子轨道数为____ ;B和E分别与氧元素形成的最高价氧化物中,熔沸点较高的是 (写化学式);
(6)F单质的晶体堆积方式为面心立方,其配位数为 ;若F的相对分子质量为M,它的晶胞棱长为a(cm),则F晶体的密度为 g·cm-3。(阿伏伽德罗常数为NA)
【化学——选修5有机化学基础】
乙苯是一种重要的化工原料。以乙苯为原料通过以下转化可得多种化工产品。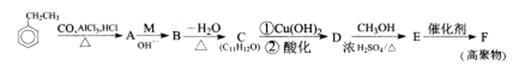
己知:
I.
II.
III.A中苯环上的一氯代物只有2种
(1)写出物质A的分子式 ,M的结构简式: 。
(2)C中苯环侧链所含官能团的名称是 。
(3)E→F的反应类型是 。
(4)关于B的说法正确的是 。(填选项字母)
a.能发生银镜反应
b.能发生消去反应
c.遇FeCl3溶液发生显色反应
d.能与H2发生加成反应
(5)写出D→E反应的化学方程式: 。
(6)符合下列条件的A的同分异构体有____ 种(不考虑立体异构),写出任意一种同分异构体的结构简式: 。
①苯环上有3个取代基
②遇FeCl3溶液发生显色反应
③能与溴水发生加成反应


 粤公网安备 44130202000953号
粤公网安备 44130202000953号