上海市嘉定区高三一模化学试卷
下列说法正确的是
| A.宏观上的物质对外不显电性,是因为组成它们的微观粒子都是电中性的原子和分子 |
| B.某物质经科学测定只含有一种元素,则可以断定该物质是一种纯净物 |
| C.利用化学方法,我们可以制造出新的分子,但不能制造出新原子 |
| D.由两种元素组成的电解质分子中,显正价的是阳离子,显负价的是阴离子 |
下列有关电子云和原子轨道的说法正确的是
| A.原子核外的电子象云雾一样笼罩在原子核周围,故称电子云 |
| B.s亚层的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动 |
| C.p亚层的原子轨道呈纺锤形,随着电子层数的增加,p亚层原子轨道也在增多 |
| D.s、p电子原子轨道的平均半径随电子层的增大而增大 |
根据原子结构及元素周期律的知识,下列推断正确的是
| A.同主族元素含氧酸的酸性随核电荷数的增加而减弱 |
| B.核外电子排布相同的微粒化学性质相同 |
| C.Cl-、S2-、Ca2+、K+半径逐渐减小 |
| D.还原性强弱: F-< Cl-< I- |
在已经处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明平衡已经发生移动的是
| A.反应混合物的浓度 | B.反应物的转化率 |
| C.正、逆反应速率 | D.反应混合物的压强 |
下列各图中,纵坐标表示能量,横坐标表示反应过程,均从反应物开始。则表示在催化剂作用下,正反应是吸热反应的,比较合理的图象是
石墨作电极电解氯化铜溶液,(下图),下列分析正确的是
| A.a端是直流电源的负极 |
| B.通电使氯化铜发生电离 |
| C.阳极上发生的反应:Cu2++2e→Cu |
| D.通电一段时间,在阴极附近观察到有黄绿色气体产生 |
常温下,在含有H+ 、SO42- 、Fe 2+ 的溶液中,加入含有下列离子的溶液后,溶液中的各种离子仍能大量共存的是
| A.MnO4- | B.CH3COO- | C.S2O32- | D.Br- |
少量 通入“84消毒液”中,其离子反应方程式最合理的是:
通入“84消毒液”中,其离子反应方程式最合理的是:
| A.H2SO3+ClO-→2 H++ SO42― +Cl― |
| B.SO2+ClO-+H2O→2 H++SO42―+Cl― |
| C.SO2+ClO-+H2O→SO32―+HClO |
| D.SO2+ClO―+2OH―→SO42―+Cl― +H2O |
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是
| 选项 |
a中的物质 |
b中的物质 |
C中收集的气体 |
d中的物质 |
| A |
浓氨水 |
CaO |
NH3 |
H2O |
| B |
稀硝酸 |
Cu |
NO2 |
H2O |
| C |
稀硫酸 |
FeS |
H2S |
NaOH溶液 |
| D |
浓盐酸 |
MnO2 |
Cl2 |
NaOH溶液 |
下列有关实验的叙述正确的是
| A.检验溶液中SO42—的方法是:先加入BaCl2溶液,再加盐酸 |
| B.从溴水中提纯单质溴的方法是:先用CCl4萃取,分液后再蒸馏 |
| C.证明气体分子中含有“C=C”的方法是:将该气体通入KMnO4酸性溶液 |
| D.除去CO2中少量HCl的方法是:将混合气体通过盛有饱和NaHSO3溶液的洗气瓶 |
下列实验误差分析错误的是
| A.用湿润的pH试纸测稀碱溶液的pH,测定值偏小 |
| B.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 |
| C.滴定前滴定管尖嘴内有气泡,终点读数时尖嘴内无气泡,所测体积偏大 |
| D.测定1mol气体体积时,未冷却至室温就读数,所测体积偏大 |
在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:
3SnCl2+12Cl—+2H3AsO3+6H+→2As+3SnCl62-+6M
关于该反应的说法中正确的组合是
① 氧化剂是H3AsO3;② 还原性:Cl->As;③ 每生成7.5gAs,还原剂失去的电子为0.3mol;
④M为OH-;⑤SnCl62-是氧化产物。
| A.①③⑤ | B.①②④⑤ |
| C.①②③④ | D.只有①③ |
羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得。
(羟基扁桃酸)
下列有关说法正确的是
| A.苯酚和羟基扁桃酸互为同系物 |
| B.标准状况下,22.4L羟基扁桃酸中共用电子对的数目为24 NA |
| C.乙醛酸只存在一种不同环境的氢原子 |
| D.羟基扁桃酸分子中至少有12个原子共平面 |
将一镁铝合金(含0.1 molMg,0.2 molAl)完全溶于由0.2 molNH4Cl和1 molHCl组成的混合溶液中,在反应后的溶液中慢慢加入Na2O2粉末,加热排出气体,则加入Na2O2的量和生成气体及沉淀的量的关系正确的是
| |
A |
B |
C |
D |
| Na2O2(mol) |
0.2 |
0.4 |
0.6 |
0.7 |
| 沉淀(mol) |
0 |
0.2 |
0.3 |
0.1 |
| 气体(mol) |
0.3 |
0.4 |
0.5 |
0.6 |
浓硫酸在加热条件下能溶解金属银,反应的化学方程式为2Ag +2H2SO4(浓) Ag2SO4 +SO2↑+2H2O,下列反应中浓硫酸的作用与该反应相同的是
Ag2SO4 +SO2↑+2H2O,下列反应中浓硫酸的作用与该反应相同的是
A.Cu + 2H2SO4 (浓)  CuSO4 + SO2 ↑+ 2H2O CuSO4 + SO2 ↑+ 2H2O |
B.C +2H2SO4 (浓) CO2 ↑ + 2SO2↑+ 2H2O CO2 ↑ + 2SO2↑+ 2H2O |
| C.2FeO+ 4H2SO4 → Fe2(SO4)3+SO2↑+ 4H20 |
D.C2H5OH +2H2SO4 (浓) 2C + 2SO2↑+ 5H2O 2C + 2SO2↑+ 5H2O |
天然碱的化学式表示为2Na2CO3·NaHCO3·2H2O,取少量该物质溶于水得到稀溶液,在溶液中逐滴加入稀盐酸。下列离子方程式与事实不相符的是
A.HCO3-+ CO32- + 3H+ 2H2O + 2CO2↑ 2H2O + 2CO2↑ |
B.2HCO3-+ CO32- + 4H+ 3H2O +3CO2↑ 3H2O +3CO2↑ |
C.CO32- + H+ HCO3- HCO3- |
D.HCO3-+ 3CO32- + 7H+ 4H2O + 4CO2↑ 4H2O + 4CO2↑ |
室温下,将一元酸HA溶液和NaOH溶液等体积混合(忽略体积变化),实验数据如下表
| 实验编号 |
起始浓度(mol/L) |
反应后溶液的pH |
|
| C(HA) |
C(NaOH) |
||
| ① |
0.1 |
0.1 |
9 |
| ② |
x |
0.2 |
7 |
下列判断正确的是
A.实验①反应后的溶液中C(Na+)>C(A-)>C(OH-)>C(H+)
B.实验①反应后的溶液中C(OH-)=C(Na+)-C(A-)= mol/L
mol/L
C.实验②反应后的溶液中C(A-)+ C(HA)=0.1 mol/L
D.实验②反应后的溶液中C(Na+)=C(A-)>C(OH-)=C(H+)
固体混合物,可能含有FeCl2、NaNO2、Ba(OH)2、AlCl3、Na2SO3中的若干种。取适量该混合物加适量水充分搅拌,得到白色沉淀A与无色溶液B.
①取适量A加入稀硝酸至过量,白色沉淀部分溶解
②取少量B逐滴加入稀硫酸至过量,不断生成白色沉淀后沉淀部分溶解
③取少量B滴加酸性高锰酸钾溶液,振荡,最终得无色溶液
根据上述实验现象,以下推测正确的是
A.无法判断固体中FeCl2是否存在
B.③中使高锰酸钾溶液褪色的是亚硝酸根离子
C.B的pH>7
D.固体由Ba(OH)2、AlCl3、Na2SO3组成
将氢氧化钠、氯化钡和硫酸铝三种固体组成的混合物溶于足量的水中,充分溶解,用1mol·L-1稀硫酸滴定,加入稀硫酸的体积与生成沉淀的质量关系如图所示
下列有关判断正确的是:
| A.A点所表示的沉淀是:Al(OH)3、BaSO4 |
| B.B-C段所发生反应的离子方程式是:H++ OH- →H2O |
| C.A-B段发生反应的离子方程式:Ba2+ + SO42- →BaSO4↓ |
| D.拐点E的横坐标为70mL |
探究外界条件对化学反应速率的影响常用到该反应
已知:Na2S2O3+H2SO4→Na2SO4+S↓+SO2+H2O
针对上述反应涉及到的元素或物质及性质回答有关问题:
23.硫元素的化合价由高到低顺序为:______________________________
涉及元素的简单离子半径由小到大顺序为:______________________________;
24.氧原子的最外层电子排布轨道表示式:______________________________;
列举2个能说明氧、硫两种元素非金属性强弱事实:______________________________;
25.预测镁在二氧化硫中燃烧的现象:________________________________________
产物除氧化镁、硫磺外还可能有 生成。
26.下面是某同学是根据该反应实验数据绘制的图表
该同学得出的结论是:
_________________________________________________________________________________。
27.将SO2通入BaCl2溶液至饱和,未见沉淀生成,继续滴加一定量的氨水后,生成BaSO3沉淀,用电离平衡原理解释上述现象。
_________________________________________________________________________________。
若继续通入另两种气体如Cl2 和H2S也会产生沉淀,请用化学方程式表示生成沉淀的原理。
_________________________________________________________________________________。
常温下有五种溶液:①NaHCO3 ;②KNO3;③NH4HCO3;④KOH;⑤HCl
28.上述五种溶液中既能跟盐酸反应又能跟NaOH溶液反应的是 (填序号)。
上述①的水溶液呈碱性的原因是(用离子方程式表示) 。
29.取10mL 0.5mol/L⑤的溶液加水稀释到500mL,则该溶液中由水电离出的c(H+)= mol/L.  ③跟足量的NaOH浓溶液在加热条件下反应的离子方程式是
③跟足量的NaOH浓溶液在加热条件下反应的离子方程式是
30.②和④混合后撒入铝粉,有气体产生,该气体能使湿润的红色石蕊试纸变蓝。
写出该反应化学方程式:_______________________________________________________。
31.最新“人工固氮”的研究报道:常温常压、光照条件下,N2在催化剂表面与水发生反应:
2N2 (g)+6H2O(l) 4NH3 (g)+3O2 (g) - Q ,如果反应的平衡常数K值变小,该反应 (选填编号)。A.一定向正反应方向移动
4NH3 (g)+3O2 (g) - Q ,如果反应的平衡常数K值变小,该反应 (选填编号)。A.一定向正反应方向移动
B.在平衡移动时正反应速率先增大后减小
C.一定向逆反应方向移动
D.在平衡移动时逆反应速率先减小后增大
32.如果上述反应在体积不变的密闭容器中进行,当反应达到平衡后,下列判断错误的是
A.容器中气体的平均分子量不随时间而变化
B.通入大量稀有气体能提高反应的速率
C. (N2)/
(N2)/  (O2)=2:3
(O2)=2:3
D.容器中气体的密度不随时间而变化
33.若反应的容器容积为2.0L,反应时间4.0 min,容器内气体的密度增大了0.18 g/L,在这段时间内O2的平均反应速率为 。
坐落在沿海地区的某纯碱厂是我国重点大型企业,其生产工艺流程可简要表示如图所示:
34.上述生产纯碱的方法称________________;副产品的一种用途为_______________。
35.使原料氯化钠的利用率从70%提高到90%以上,主要是设计了__________(填上述流程中的编号)的循环。从沉淀池中取出沉淀的操作所需玻璃仪器有烧杯、_______________________等。
36.母液中含有NaCl、NH4Cl、_____________________(以化学式表示)。向母液中通入氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有___________
硫酸铜晶体(CuSO4·xH2O),采用加热法测定该晶体中结晶水x的值,实验数据记录如下:
| 坩埚质量 |
坩埚与晶体总质量 |
加热后坩埚与固体总质量 |
||
| 第一次称量 |
第二次称量 |
|||
| 11.710g |
22.700g |
18.621g |
a |
|
37.若无需再进行第三次称量,则a的数值范围应为 。
38.若加热后坩埚与固体总质量为18.620g,计算x 的实测值 (保留二位小数),相对误差 。
昆石属于稀有的石种,其成分主要是二氧化硅以及铁、钠、钙元素的氧化物,根据图示流程回答有关问题。
39.操作1和操作4的名称分别是________和_________。
40.写出加CaO时发生反应的离子方程式:________。
41.在沉淀2后,依次进行了洗涤、干燥、灼烧操作,证明沉淀已经洗涤干净的操作是
________________________________________________________________________
42.证明滤液3含有钠元素的方法是________________________________________
43.写出能证明红棕色固体中含有金属元素的操作过程、现象、结论。
________________________________________________________________________________________
咖啡酸苯乙酯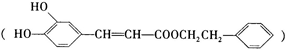 是一种天然抗癌药物,在一定条件下能发生如下转化:
是一种天然抗癌药物,在一定条件下能发生如下转化: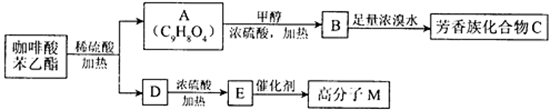
请填写下列空白。
44.D分子中的官能团是__________;高分子M的结构简式是_____________。
45.写出A→B反应的化学方程式:_______________________。
46.B→C发生的反应类型有______________________。
47.A的同分异构体很多种,其中,同时符合下列条件的同分异构体有____种。
①苯环上只有两个取代基;②能发生银镜反应;③能与碳酸氢钠溶液反应;
④能与氯化铁溶液发生显色反应。
48.以下对A具有的性质描述正确的是__
a.1molA可消耗2molNaOH
b.一定条件下1molA最多能与1mol氢气加成
c.能发生银镜反应
d.能发生取代反应
某芳香族化合物H(C11H12O4)是有机合成工业的一种重要的中间产物,其合成路线如下。已知2molC分子可缩合生成1mol六元环化合物分子。F常温下是气体,水溶液具有很好的防腐杀菌效果,且能与新制氢氧化铜反应。请回答下列问题:
49.F的电子式为 , A的结构简式
B转化为C的条件是
| A.水解、酸化、氧化、还原 | B.氧化、水解、酸化、还原 |
| C.水解、酸化、还原、氧化 | D.氧化、酸化、水解、还原 |
50.以C为原料可合成可降解塑料,试写出其化学方程式
51.H与氢氧化钠溶液反应的化学方程式
52.H的同分异构体有多种,请写出符合下列条件的同分异构体的结构简式
。(写两种即可)
①苯环上只有两个取代基,苯环上的一氯取代物只有两种
②1mol的H与足量的NaHCO3溶液反应,生成2molCO2
计算题
53.某同学查得Ba(OH)2•8H2O晶体在20℃时的溶解度为3.9 g/100g水,则20℃时,Ba(OH)2饱和溶液的质量分数为______________________ (答案保留2位小数) 。
54.过氧化钡(BaO2)是一种常用的氧化剂。工业上制取过氧化钡的方法之一是2BaO+O2
2BaO2。现有16.0吨的氧化钡在足量的氧气中加热反应后,固体的质量变为17.6吨。那么实际参加反应的氧化钡的质量为______________吨。
取不同质量由Ba(OH)2•nH2O和BaCO3组成的样品,加水溶解后加入80 mL 1.0 mol/L的盐酸,并不断地搅拌,所得CO2气体的体积(已换算为标准状况)与加入样品的质量关系通过描点得到下图(在此过程中不考虑Ba(HCO3)2的生成和CO2的溶解)。请计算:
55.在11.58 g样品中BaCO3的质量为多少g?(写出计算过程)
56.化学式Ba(OH)2•nH2O中n的值为多少?(写出计算过程)

 粤公网安备 44130202000953号
粤公网安备 44130202000953号