河南省新野县第三高中高三上学期第四次月考化学试卷
化学已渗透人类生活的各个方面,下列说法不正确的是
| A.高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
| B.“光化学烟雾”、“臭氧空洞”的形成都与氮氧化合物有关 |
| C.低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,减少温室气体的排放 |
| D.高铁酸钾(K2FeO4)是新型高效多功能水处理剂,既能消毒杀菌又能净水 |
已知25℃、101kPa时,1g甲醇(CH3OH)完全燃烧生成CO2和液态H2O,同时发出22.68kJ热量。则下列表示该反应的热化学方程式正确的是
| A.CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(g) △H=-725.8kJ•mol-1 |
| B.2 CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1451.6kJ |
| C.2 CH3OH+3O2=2CO2+4H2O △H=-22.68kJ•mol-1 |
| D.CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)△H=-725.8kJ•mol-1 |
据报导,2012年俄罗斯科学家再次合成117号元素。本次实验生成了6个新原子,其中5个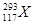 ,1个
,1个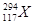 。下列关于
。下列关于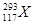 和
和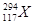 的说法,不正确的是
的说法,不正确的是
| A.是两种核素 | B.互为同位素 |
| C.中子数分别为176和177 | D.电子数相差1 |
我国的砷化镓太阳能电池研究方面处于国际领先。砷(As)和镓(Ga)都是第四周期元素,分别属于ⅤA和ⅢA族.下列说法中,不正确的是
| A.原子半径:Ga>As>P |
| B.热稳定性:NH3>PH3>AsH3 |
| C.酸性:H3AsO4>H2SO4>H3PO4 |
| D.Ga(OH)3可能是两性氢氧化物 |
下列各组离子一定能大量共存的是
| A.在含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- |
| B.在含有Al3+、Cl-的溶液中:HCO3-、I-、NH4+、Mg2+ |
| C.在c(H+)=1×10-13mol/L的溶液中:Na+、S2-、SO32-、NO3- |
| D.在溶质为KNO3和NaHSO4的溶液中:Fe2+、Ca2+、Al3+、Cl- |
下列实验中,颜色的变化与氧化还原反应有关的是
| A.往紫色石蕊试液中加入盐酸,溶液变红 |
| B.饱和FeCl3溶液在沸水中变成红褐色胶体 |
| C.向FeSO4溶液中滴加NaOH溶液,生成的沉淀由白色变成灰绿色,最后变成红褐色 |
| D.SO2使有酚酞的NaOH溶液褪色 |
下图实验为研究金属腐蚀的实验,下列相关说法正确的是
| A.食盐水中有气泡逸出 |
| B.铁表面的反应为Fe-3e=Fe3+ |
| C.红色首先在食盐水滴的中心出现 |
| D.该实验研究的是金属的吸氧腐蚀 |
设NA为阿伏伽德罗常数的值。下列叙述正确的是
| A.20mL10mol/L的浓硝酸与足量铜加热反应转移电子数为0.2NA |
| B.标准状况下,11.2L氦气中含有NA原子 |
| C.在精炼铜或电镀铜的过程中,当阳极消耗铜32g时,转移电子数均为NA |
| D.标准状况下,2.24LCl2通入足量NaOH溶液中发生反应转移电子数为0.1NA |
密闭容器中,有可逆反应Z(g)+W(g) X(?)+2Y(?)发生,Z的转化率随温度和压强变化关系如图所示,有关该平衡体系的说法不正确的是
X(?)+2Y(?)发生,Z的转化率随温度和压强变化关系如图所示,有关该平衡体系的说法不正确的是
A.T1℃温度下发生反应的平衡常数表达式为K= |
| B.T1℃温度下混合气体的平均相对分子质量保存不变时,反应达到平衡 |
| C.升高温度至T2℃,平衡常数K减小 |
| D.增加X的量,平衡一定逆向移动 |
下列离子方程式正确的是
| A.NaHSO3溶液与NaOH溶液反应:H++OH-=H2O |
| B.少量二氧化碳通入足量的NaOH溶液中:CO2+OH-=HCO3- |
| C.Fe与盐酸反应产生氢气:2Fe+6H+=2Fe3++3H2↑ |
| D.氨水与醋酸溶液混合:NH3·H2O+CH3COOH=NH4++CH3COO-+H2O |
分析如图所示的能量变化,下列热化学方程式正确的是
| A.S(s,单斜)+O2(g)=SO2(g) △H=+297.16kJ/mol |
| B.S(s,单斜)+O2(g)=SO2(g) △H=-296.83kJ/mol |
| C.S(s,正交)+O2(g)=SO2(g)△H=-296.83kJ/mol |
| D.单斜硫的稳定性大于正交硫的稳定性 |
实现反应:Cu+2H+=Cu2++H2↑,可以通过以下措施
| A.将Cu投入稀硫酸中 |
| B.让Cu在潮湿的环境发生电化学腐蚀 |
| C.将Cu投入浓硫酸中并加热 |
| D.用Cu作电极、稀硫酸作电解质溶液电解 |
在一定温度下,向2L体积固定的密闭容器中加入1molHI,2HI(g) H2(g)+I2(g)△H>0,H2的物质的量随时间的变化如图示,下列说法正确的是
H2(g)+I2(g)△H>0,H2的物质的量随时间的变化如图示,下列说法正确的是
| A.该温度下,反应的平衡常数是1/8 |
| B.0~2min内的HI的平均反应速率为0.05mol•L-1•min-1 |
| C.恒压下向该体系中加入N2,平衡不移动,反应速率不变 |
| D.升高温度,平衡向正反应方向移动,只有正反应速率加快 |
锂离子电池已经成为应用最广泛的可充电电池。某种锂离子电池的结构示意图如下图,其中两极区间的隔膜只允许Li+通过。电池充电时的总反应化学方程式为:LiC002=Li1-xC002+xLi。关于该电池的推论错误的是
A.放电时,Li+主要从负极区通过隔膜移向正极区
B.放电时,负极反应xLi-xe-=xLi+
C.充电时,有电能转化为化学能
D.充电时,负极(C)上锂元素被氧化
已知H2(g)、C2H4(g)和C2H5OH(l)的燃烧热分别是-285.8kJ/mol、-1411.0kJ/mol和-1366.8kJ/mol,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为
| A.-44.2kJ/mol | B.+44.2kJ/mol |
| C.-330kJ/mol | D.+330kJ/mol |
为探究铁质材料与热浓硝酸的反应,某学习小组进行了以下实验:
[探究一]
(1)铁钉放在浓硫酸中浸泡后,再用蒸馏水冲洗,然后放入硫酸铜溶液中,铁钉表面无明显变化,其原因是_____________________。
(2)另称取铁钉6.0g放入15.0ml浓硝酸中,加热,充分应后得到溶液M并收集到气体N。为了探究溶液M中铁元素的价态,甲同学设计了如下实验:
有药品:
| A.稀盐酸溶液 |
| B.稀硫酸溶液 |
| C.淀粉KI溶液 |
| D.KMnO4溶液 |
E.NaOH溶液
F.H2O2溶液
G.KSCN溶液
仪器:试管和滴管
步骤1.取试样,滴加少量的______(填试剂字母),溶液的颜色变____色,则试样中含有Fe3+,发生反应的离子方程式为________________。
步骤2.再去适量的试样滴加少量的______(填试剂字母),若溶液_______,则试样中含有Fe2+。
[探究二]
乙同学设计以下装置探究气体N的成分。
(3)A装置的作用:______________________。
(4)B装置收集满气体后,通过气泡鼓入空气后,有红棕色气体生成,能否确定气体N中含NO____(填“能”或“不能”)?理由是________________。
已知A、B、C、D四种短周期元素原子序数依次增大,A与D的原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,B、C、D三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且X、Y、Z可两两相互反应生成盐和水,试推断并用相应的化学用语回答下列问题:
(1)D元素原子的结构示意图为_________________;
(2)X与C元素的最高价氧化物可以发生反应,该反应的离子方程式为___________________;
(3)A、B、C三种元素的原子半径由小到大的顺序为__________________________;
(4)A与D两元素的气态氢化物之间可以反应生成一种盐,该盐的水溶液呈___(填“酸”、“碱”或“中”)性,该水溶液中各离子浓度由小到大的顺序为_____________________。
工业上金属的冶炼过程复杂。
(1)炼铁涉及的2个热化学方程式:
Fe2O2(s)+1/3CO(g)=2/3Fe3O4(s)+1/3CO2(g) △H=-15.73kJ•mol-1
Fe3O4+CO(g)=3FeO(s)+CO2(g) △H=+640.4kJ•mol-1
则反应Fe2O3(s)+CO(g)=2FeO(s)+CO2(g)的△H=__________;
(2)工业上电解硫酸锌溶液可实现湿法炼锌(控制条件,使H+难放电、阳极电极不溶解).写出电解总反应离子方程式____________________;
(3)将干净的铁片浸于熔融的液态锌水中可制得镀锌钢板,这种钢板具有很强的耐腐蚀能力。镀锌钢板的镀层一旦被破坏后,锌将作为原电池的___极发生___反应。(填“氧化”或“还原”)
(4)实验室用镀锌钢板与稀硫酸制取标准状况下的氢气4.48L,则该反应转移的电子数为______,消耗硫酸的物质的量是_____________。
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) △H>0。
2Fe(s)+3CO2(g) △H>0。
①该反应的平衡常数表达式为K=________________;
②该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。则10min内CO的平均反应速率为_____________________;
(2)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是__________;
(3)三价铁盐和铝盐在性质上有很多相似的地方,如遇碱都生成难溶的胶状沉淀,可用于净水;也有不同之处,如Fe3+既有氧化性又有还原性,Al3+只有氧化性.但Fe3+只有在碱性介质中才能被氧化为FeO42-,请完成下列化学方程式:
_____Fe(OH)3+___ClO-+____ =____FeO42-+___Cl-+____
=____FeO42-+___Cl-+____ ;
;
(4)若将ag Fe和Al的混合物溶于2mol/L足量的硫酸中,再往溶液中加入足量的6mol/L的NaOH溶液,充分反应,过滤、洗涤、干燥灼烧,称量所得固体的质量仍为ag,则原混合物中Al的质量分数为_____________。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号