广东省汕头市潮师高中高二上学期期中化学(理)试卷
下列变化属于吸热反应的是
①液态水汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释
④氯酸钾分解制氧气 ⑤生石灰与水反应生成熟石灰
| A.①②④ | B.②③⑤ | C.①④⑤ | D.②④ |
关于冰融化为水的过程判断正确的是
| A.ΔH>0,ΔS>0 | B.ΔH<0,ΔS>0 |
| C.ΔH>0,ΔS<0 | D.ΔH<0,ΔS<0 |
一定温度下,反应N2+O2 2NO在密闭容器中进行,下列措施不改变化学反应速率的是
2NO在密闭容器中进行,下列措施不改变化学反应速率的是
| A.缩小体积使压强增大 | B.恒容,充入N2 |
| C.恒压,充入He | D.恒容,充入氩气 |
下列有关热化学方程式的叙述正确的是
| A.已知2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1,则氢气的燃烧热为285.8 kJ·mol-1 |
| B.已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
| C.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) ΔH=-57.4 kJ·mol-1 |
| D.已知2C(s)+2O2(g)=2CO2(g) ΔH1; 2C(s)+O2(g)==="2CO(g)" ΔH2,则ΔH1>ΔH2 |
在一定条件下,反应2HI(g) H2(g)+ I2(g)(紫红色) ΔH>0,达到平衡时,要使混合气体的颜色加深,可采取的措施是
H2(g)+ I2(g)(紫红色) ΔH>0,达到平衡时,要使混合气体的颜色加深,可采取的措施是
①增大氢气的浓度 ②升高温度 ③降低温度 ④缩小体积 ⑤增大HI的浓度 ⑥减小压强
| A.①③⑥ | B.②④⑤ | C.③⑤⑥ | D.①③⑤ |
对化学反应3X(g)+Y(g) 2Z(g)+2Q(s)达到平衡后,增大压强,下列关于对该化学反应产生的影响的说法正确的是
2Z(g)+2Q(s)达到平衡后,增大压强,下列关于对该化学反应产生的影响的说法正确的是
| A.正反应速率增大,逆反应速率减小,平衡向正反应方向移动 |
| B.正反应速率减小,逆反应速率增大,平衡向逆反应方向移动 |
| C.正、逆反应速率都增大,平衡向正反应方向移动 |
| D.正、逆反应速率都没有变化,平衡不发生移动 |
在一恒容密闭烧瓶中,25℃时存在平衡:2NO2(g)  N2O4(g) △H<0。将烧瓶置于100℃的水中,则下列物理量中不会改变的是
N2O4(g) △H<0。将烧瓶置于100℃的水中,则下列物理量中不会改变的是
| A.颜色 | B.密度 | C.N2O4的浓度 | D.压强 |
下列说法中不正确的是
| A.在相同条件下,反应可向正方向进行,又可向逆方向进行的反应就是可逆反应 |
| B.在其他条件不变时,升高温度可以使化学平衡向吸热反应的方向移动 |
| C.有气体的可逆反应,在其他条件不变时,增大压强可使化学平衡向气体体积缩小的方向移动 |
| D.在其他条件不变时,使用催化剂既可以加快化学反应速率,又可以使化学平衡状态移动 |
下列说法正确的是
| A.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
| C.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 |
| D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率 |
恒温下,反应aX(g) bY(g) +cZ(g)达到平衡后, 把容器体积压缩到原来的一半且达到新平衡时,X的物质的量浓度由0.1mol/L增大到0.19mol/L,下列判断正确的是:
bY(g) +cZ(g)达到平衡后, 把容器体积压缩到原来的一半且达到新平衡时,X的物质的量浓度由0.1mol/L增大到0.19mol/L,下列判断正确的是:
| A.a>b+c | B.a<b+c | C.a=b+c | D.a=b="c" |
灰锡(以粉末状存在)和白锡(韧性很好)是锡的两种同素异形体。已知:
①Sn(s、白)+2HCl(aq)=SnCl2(aq)+H2(g) △H1
②Sn(s、灰)+2HCl(aq)=SnCl2(aq)+H2(g) △H2
③Sn(s、灰)  Sn(s、白) △H3=+2.1kJ·mol-1
Sn(s、白) △H3=+2.1kJ·mol-1
下列说法正确的是
| A.△H1>△H2 |
| B.锡的两种同素异形体在常温下可以相互转化,是可逆反应 |
| C.灰锡转化为白锡的反应是吸热反应 |
| D.锡制器皿应置于高于13.2℃的环境中,否则会自行毁坏 |
可逆反应mA(s)+ nB(g) eC(g)+fD(g)反应过程中,当其他条件不变时,C的体积分数φ(C)在不同温度(T)和不同压强(p)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是
eC(g)+fD(g)反应过程中,当其他条件不变时,C的体积分数φ(C)在不同温度(T)和不同压强(p)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是
A.达到平衡后,若使用催化剂,C的体积分数将增大
B.达到平衡后,增加A的质量,化学平衡向不移动
C.化学方程式中,n>e+f
D.达到平衡后,若温度升高,化学平衡向逆反应方向移动
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图,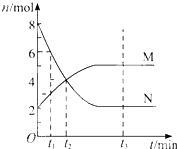
下列表述中正确的是
A.反应的化学方程式为:2 N  M M |
| B.t2时,正逆反应速率相等,达到平衡 |
| C.t3时,正反应速率大于逆反应速率 |
| D.t1时,N的浓度是M浓度的2倍 |
2 mol A与2 mol B混合于2 L的密闭容器中,发生如下反应:2A(g)+3B(g) 2C(g)+zD(g),若2s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是
2C(g)+zD(g),若2s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是
A、v(C)=v(D)=0.25 mol·L-1·s-1
B、z=3
C、B的转化率为25%
D、C的体积分数为28.6%
下图中曲线表示一定条件下可逆反应X(g)+Y(g) 2Z(g)+W(s);ΔH<0的反应过程。若使a曲线变为b曲线,可采取的措施是
2Z(g)+W(s);ΔH<0的反应过程。若使a曲线变为b曲线,可采取的措施是
| A.加入催化剂 | B.增大Y的浓度 |
| C.降低温度 | D.增大体系压强 |
(12分)(1)已知C(s、金刚石)+O2==CO2(g) ΔH=-395.4kJ/mol,
C(s、石墨)+O2==CO2(g) ΔH=-393.5kJ/mol。
①石墨和金刚石相比,石墨的稳定性 金刚石的稳定性。
②石墨中C-C键键能______金刚石中C-C键键能。(均填“大于”、“小于”或“等于”)。
(2)肼(N2H4)和NO2是一种双组分火箭推进剂。两物质混合发生反应生成N2和H2O(g),已知8g气体肼在上述反应中放出142kJ热量,其热化学方程式为: 。
(3)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学反应方程式为: ;
又知H2O(l) H2O(g),△H=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时,放出的热量是 kJ。
H2O(g),△H=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时,放出的热量是 kJ。
(8分)能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质。一定条件下,在体积为2 L的密闭容器中,1mol一氧化碳与2mol氢气反应生成甲醇(催化剂为Cu2O/ZnO):
CO(g)+2H2(g) CH3OH(g) △H<0
CH3OH(g) △H<0
根据题意完成下列各题:
反应达到平衡时,平衡常数表达式K= ,升高温度,K值 (填“增大”、“减小”或“不变”)。
(2)在500℃,10min反应达平衡,此时甲醇的物质的量浓度为0.3mol/L,从反应开始到平衡,氢气的平均反应速率v(H2)= 。
(3)在其它条件不变的情况下,把反应处于平衡体系的容器的体积压缩为1 L,下列有关该体系的说法正确的是 。
| A.平衡向正反应方向移动 | B.正反应速率加快,逆反应速率减慢 |
| C.甲醇的物质的量增加 | D.重新平衡时c(CO)/c(CH3OH)不变 |
(1)已知下列各反应的焓变
①Ca(s)+C(s,石墨)+3/2O2(g)=CaCO3(s) △H1 = -1206.8 kJ/mol
②Ca(s)+1/2O2(g)=CaO(s) △H2= -635.1 kJ/mol
③C(s,石墨)+O2(g)=CO2(g) △H3 = -393.5 kJ/mol
试求: ④CaCO3(s)=CaO(s)+CO2(g) △H=________。
(2)已知下列各反应的焓变
①CO(g)+1/2O2(g)=CO2(g) ΔH1= -283.0 kJ/mol
②H2(g)+1/2O2(g)=H2O(l) ΔH2= -285.8 kJ/mol
③C2H5OH(l)+ 3O2(g)=2CO2(g)+3H2O(l) ΔH3=-1370 kJ/mol
试求: ④2CO(g)+4H2(g)=H2O(l)+C2H5OH(l) ΔH=________。
(10分)汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g) 2NO(g),ΔH>0,已知该反应在2 404℃,平衡常数K=64×10-4。请回答:
2NO(g),ΔH>0,已知该反应在2 404℃,平衡常数K=64×10-4。请回答:
(1)某温度下,向2 L的密闭容器中充入N2和O2各1 mol,5分钟后O2的物质的量为0.5 mol,则N2的反应速率为_____________________。
(2)为了减少汽车尾气中有害气体的排放,在现实生活中你认为可以采取的措施有 。
| A.采用耐高温的陶瓷发动机,以提高内燃机的工作温度 |
| B.为了避免上述反应,不使用空气,改用纯氧气 |
| C.在排气管中安装高效催化剂,将有害气体转化为无害气体 |
| D.将燃油车改换成电动车 |
(3)将一定量的N2、O2的混合气体充入恒容密闭容器中,下图变化趋势正确的是____________(填字母序号)。
(4)将一定量的N2、O2的混合气体充入恒温密闭容器中,分别在不同的压强P1、P2(P1>P2)下达到平衡,请画出N2的转化率在不同压强下随时间变化的曲线图。(不同压强下的曲线要有相应的标识)
 2C (g) + xD (g) ,经过5min达到化学平衡,此时生成C为2mol,测得D的反应速率为0.1mol/(L·min),计算:①、x的值;②、平衡时B的转化率;③、A的平衡浓度;④求平衡常数K。(用三段式的方法写出必要的计算过程,结果精确到小数点后两位)
2C (g) + xD (g) ,经过5min达到化学平衡,此时生成C为2mol,测得D的反应速率为0.1mol/(L·min),计算:①、x的值;②、平衡时B的转化率;③、A的平衡浓度;④求平衡常数K。(用三段式的方法写出必要的计算过程,结果精确到小数点后两位) 粤公网安备 44130202000953号
粤公网安备 44130202000953号