在标准状况下,进行甲、乙、丙三组实验。三组实验各取30 ml.同浓度的盐酸,加入同
一种镁、铝混合物粉末,产生气体,有关数据列表如下:

(1)甲、乙两组实验中,哪一组盐酸是不足量的? (填“甲”或“乙”)。理由是
(2)计算盐酸的物质的量浓度;(写出计算过程)
(3)求混合粉末中Mg、Al的物质的量之比?(写出计算过程)
实验室欲配制0.5 mol.L-l的NaOH溶液500 mL有以下仪器:①烧杯②分液漏斗③1 000 mL容量瓶④500 mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)
(1)配制时,必须使用的仪器有(填代号) ,还缺少的仪器是__________。
(2)需称量________g烧碱固体,固体应放在 中称量。
(3)使用容量瓶前必须进行的一步操作是 。
(4)在配制过程中,其他操作都正确,下列操作会引起误差偏高的是 。
①未洗涤烧杯、玻璃棒
②未等NaOH溶液冷却至室温就转移到容量瓶中
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤定容时仰视刻度线
⑥NaOH用纸盛装进行称量
⑦超过刻度线,吸出一部分水
⑧摇匀后液面下降,补充水
下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
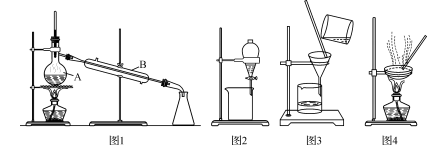
(1)装置图l中A的名称是 ,B的名称是 。
A中一般要加入碎瓷片,其作用是 。装置图4中盛溶液的仪器名称是 。
(2)为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

i灼烧海带时,除需要三脚架外,还需要用到的实验仪器是 (从下列仪器中选出所需仪器,将标号字母填写在空白处);
A 烧杯 B 坩埚 C 表面皿 D 泥三角 E 酒精灯
ii步骤③的实验选择上述装置图 (填图的序号);
iii步骤⑤的实验操作名称是_____________;
iV步骤⑥的目的是从含碘苯溶液中分离出单质碘,同时回收苯,该步骤的实验操作名称是 _,选择上述装置图 (填图的序号)。
已知X是某金属单质,X、A、B、C含同一种元素,可发生如下转化:
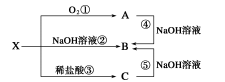
(1)写出下列物质的化学式:X ,A ,B C ;
(2)写出以下反应的离子方程式:
②
④
铝、铁的混合物溶于足量的盐酸中,再加入过量的NaOH溶液,在空气中静置,当红褐色沉淀不再增加时,将沉淀滤出并充分灼烧,得到的固体残留物恰好跟原混合物的质量相等,则此合金中铝的质量分数为
| A.22.2% | B.75.7% | C.30.0% | D.80.6% |
若在加入铝粉能放出H2的溶液中分别加入下列各组离子,肯定不能大量共存的是
| A.Fe3+、SO42-、C1-、Na+ |
| B.Ba2+、Mg2+、CO32-、C1- |
| C.N03-、Na+、K+、CO32- |
| D.N03-、K+、CO32-,OH- |
下列实验问题的处理方法中,正确的是
| A.用铂丝做焰色反应实验,每次做完后都需要用盐酸洗涤,再用自来水洗净后使用 |
| B.在气体发生装置上直接点燃H2气体前,必须先检验氢气的纯度 |
| C.实验结束后,应及时将废液倒人下水道,清洗仪器并摆放整齐 |
| D.在制取NH3的实验中,将多余的NH3直接用玻璃导管导入水中(注:NH3极易溶于水),以 |
免污染空气
深秋及寒冬的清晨,常出现有雾的天气,雾中小液滴直径范围是
| A.小于1 nm | B.在1~100 nm之间 |
| C.大于100 nm | D.无法确定 |
常温下,将四种不同的一元酸(用 HA 代表)分别和 NaOH 溶液等体积混合。 两种溶液的物质的量浓度和混合溶液的 pH 如下表所示:
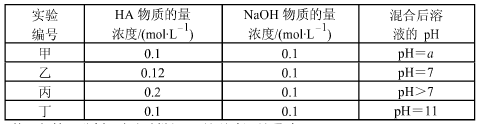
(1)从甲组情况分析,如何判断 HA 是强酸还是弱酸?________________。
(2)乙组混合溶液中粒子浓度 c(A-)和 c(Na+)的大小关系_____________。
A.前者大 B.后者大 C.两者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是:___________
(4)分析丁组实验数据,写出混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=_______mol·L-1。
(5) 某二元酸(化学式用 H2B 表示)在水中的电离方程式是:
H2B===H++HB- HB- H++B2-
H++B2-
回答下列问题:
在 0.1 mol·L-1的 Na2B 溶液中,下列粒子浓度关系式正确的是________。
A.c(B2-)+c(HB-)=0.1 mol·L-1
B.c(B2-)+c(HB-)+c(H2B)=0.1 mol·L-1
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(H+)=c(OH-)+c(HB-)
(1)4g CO 在氧气中燃烧生成 CO2,放出 9.6kJ 热量,写出 CO 燃烧的热化学方程式;
(2)已知拆开 1mol H﹣H 键、1mol N﹣H 键、1mol N≡N 键分别需要的能量是 436kJ、391kJ、946kJ,则 N2与 H2反应生成 NH3的热化学方程式为 。
(3)已知碳的燃烧热△H1="a" kJ•mol﹣1
2K(s)+N2(g)+3O2(g)═2KNO3(s)△H2="b" kJ•mol﹣1
S(s)+2K(s)═K2S(s)△H3="c" kJ•mol﹣1
则 S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g)△H= 。
II.稀土元素是宝贵的战略资源,赣州的稀土蕴藏量居世界首位,是名符其实的稀土王国。
(4)铈(Ce)是地壳中含量最高的稀土元素。在加热条件下 CeCl3易发生水解,无水 CeCl3可用加热 CeCl3·6H2O 和 NH4Cl 固体混合物的方法来制备。其中 NH4Cl 的作用是
(5)在某强酸性混合稀土溶液中加入 H2O2,调节 pH≈3,Ce3+通过下列反应形成 Ce(OH)4沉淀得以分离。完成反应的离子方程式:□Ce3++□H2O2+□H2O ===□Ce(OH)4↓+□_________
将 0.1 L 含有 0.02mol CuSO4和 0.01molNaCl 的水溶液用惰性电极电解。电解一段时间后,一个电极上得到 0.01 mol Cu,另一电极析出的气体( )
| A.只有Cl2 | B.既有Cl2又有O2 | C.只有O2 | D.只有H2 |
已知热化学方程式:2SO2(g)+O2(g) 2SO3(g); H=-Q kJ·mol-1(Q>0)。下列说法 正确的是( )
2SO3(g); H=-Q kJ·mol-1(Q>0)。下列说法 正确的是( )
| A.相同条件下,2 mol SO2(g)和 1 mol O2(g)所具有的能量小于 2 mol SO3(g)所具有的能量 |
| B.将 2 mol SO2(g)和 1 mol O2(g)置于一密闭容器中充分反应后,放出热量为 Q kJ |
| C.增大压强或升高温度,该平衡都向逆反应方向移动 |
| D.如将一定量 SO2(g)和 O2(g)置于某密闭容器中充分反应放热 Q kJ,则此过程中有 2 mol SO2(g)被氧化 |
下列各组实验中溶液最先变浑浊的是( )
| A.0.1mol/LNa2S2O3和 H2SO4 各 5mL,加水 5mL,反应温度10℃ |
| B.0.1mol/LNa2S2O3 和 H2SO4各 5mL,加水 10mL,反应温度 10℃ |
| C.0.1mol/L Na2S2O3和H2SO4各 5mL,加水 5mL,反应温度 30℃ |
| D.0.2mol/L Na2S2O3和H2SO4各 5mL,加水 10mL,反应温度 30℃ |
运用相关化学知识进行判断,下列结论错误的是
| A.某吸热反应能自发进行,因此该反应是熵增反应 |
| B.NH4F 水溶液中含有 HF,因此 NH4F 溶液不能存放于玻璃试剂瓶中 |
| C.可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 |
| D.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成 H2 的速率 |
吸热反应N2(g)+O2(g) 2NO(g),在2000℃时K=6.2×10-4。2000℃时,向10L密闭容器中放入3×10-3molNO、2.50×10-1molN2和4.00×10-2molO2。
2NO(g),在2000℃时K=6.2×10-4。2000℃时,向10L密闭容器中放入3×10-3molNO、2.50×10-1molN2和4.00×10-2molO2。
通过计算回答:
(1)此反应的初始状态是否为化学平衡状态?
(2)若非化学平衡状态,反应将向哪个方向进行以达到化学平衡状态?