【2015年江苏省扬州市】含锌废渣和各种锌矿(如菱锌矿)都有着重要的用途
Ⅰ.以含锌废渣(主要成分为ZnO,杂质为FeO﹑CuO)为原料制备七水硫酸锌(ZnSO4·7H2O)的流程如下。
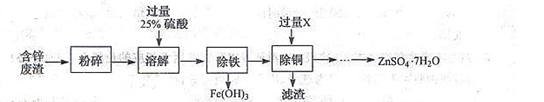
(1)粉碎的目的是 。
(2)若实验室用质量分数为98%的硫酸配制200g25%的硫酸,需要的玻璃仪器有胶头滴管﹑玻璃棒﹑ 和 ,此处玻璃棒的作用是 。
(3)物质X是 ,滤渣中含有的金属单质有 ,除铜时发生的反应属于 反应(填基本反应类型)
(4)流程中获得七水硫酸锌前省略的操作是 ﹑冷却结晶﹑ 洗涤和低温烘干。
(5)某温度下,Fe(OH)3分解得到一种铁﹑氧质量比21:8的氧化物,该氧化物的化学式 。
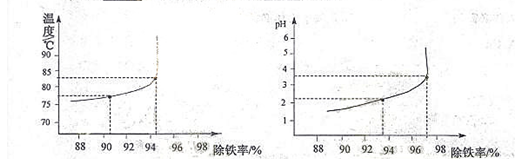
(6)除铁过程中,温度pH对除铁效果的影响分别对如图所示。由图可知,除铁时温度应控制在 ℃为宜,pH应控制在 为宜。
Ⅱ.以某菱锌矿(ZnCO3含量为62.5%)为原料制备锌的原理如下(假设杂质不参加反应):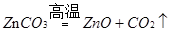
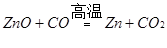 则100吨这样的菱锌矿理论上最多制得锌多少吨?(写出计算过程)
则100吨这样的菱锌矿理论上最多制得锌多少吨?(写出计算过程)
【2015年山东省济南市】1926年,我国著名化学家侯德榜先生创立了侯氏制碱法,促进了我国民族工业的发展和世界制碱技术的进步,其生产过程中有下列反应: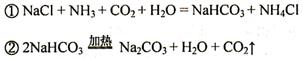
(1)侯氏制碱法所制的“碱”是指_______________。
(2)工业生产过程中,氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,在常温下,两者首先从溶液中结晶析出的是_________ 晶体(填物质名称)。
(3)现有Na2CO3和NaCl的混合物样品22.3g,将其放入干净的烧杯中,加一定质量的水使其完全溶解。向所得溶液中逐滴加入溶质质量分数为7.3%的稀盐酸,烧杯中溶液的质量与滴入稀盐酸的质量关系曲线如图所示。试回答下列问题: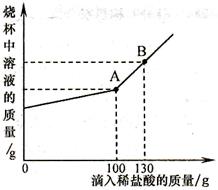
①当滴入上述稀盐酸至图中B点时,烧杯中溶液里的溶质为_______________(写化学式)。
②在Na2CO3和NaCl的混合物样鼎中,含Na2CO3的质量为_______________g。
③当滴入上述稀盐酸至图中A点时,试通过计算,求此温度时所得不饱和溶液中溶质的质量(计算结果精确至0.1g)。
【2015年四川省泸州市】过氧化钙晶体﹝CaO2·8H2O﹞较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒。以贝壳为原料制备CaO2流程如下:
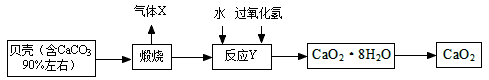
(1)气体X是CO2,其名称是 ;将过氧化钙晶体与溶液分离的方法是 。
(2)反应Y需控制温度在0~5℃,可将反应容器放在 中,该反应是化合反应,反应产物是CaO2·8H2O,请写出化学方程式 。获得的过氧化钙晶体中常含有Ca(OH)2杂质,原因是 。
(3)CaO2的相对分子质量为 ,过氧化钙晶体﹝CaO2·8H2O﹞中H、O元素的质量比为 。
(4)为测定制得的过氧化钙晶体中CaO2·8H2O的质量分数,设计的实验如下:称取晶体样品50g,加热到220℃充分反应(方程式为2CaO2·8H2O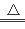 2CaO+O2↑+16H2O↑,杂质不发生变化),测得生成氧气的质量为3.2g,请计算样品中CaO2·8H2O的质量分数(CaO2·8H2O相对分子质量为216),写出必要的计算过程。
2CaO+O2↑+16H2O↑,杂质不发生变化),测得生成氧气的质量为3.2g,请计算样品中CaO2·8H2O的质量分数(CaO2·8H2O相对分子质量为216),写出必要的计算过程。
【2015年山东省德州市】2015年4月13日,西昌市动物疫病预防控制中心堆放在仓库中浓度为21%的过氧乙酸消毒液发生泄漏。经查阅资料可知:过氧乙酸(化学式为C2H4O3)是无色液体,有强烈刺激性气味,易溶于水、乙醇等,易挥发,与其他酸有相似的化学性质,温度稍高即分解为乙酸、氧气。请回答下列问题:2-1-c-n-j-y
(1)过氧乙酸的物理性质有: (写出两条即可)。
(2)过氧乙酸溶液中存在的阳离子是 (填离子符号)。
(3)过氧乙酸中碳、氢、氧元素的质量比为:
(4)乙酸和过氧乙酸都是无色液体,具有强烈剌激性气味,要把两种液体区别开来,可采用的方法是:________________________________________________________________
【2015年四川省宜宾市】元素X、Y、Z、M是初中常见的四种元素。有关信息如下表:
| 元素 |
有关信息 |
| X |
可形成相对分子质量最小的气体单质 |
| Y |
形成的一种单质是天然存在的最硬的物质 |
| Z |
期单质约占空气总体积的1/5 |
| M |
人体内含量最高的金属元素 |
(1)M元素的名称是 。
(2)Y形成的天然存在的最硬的物质是 ,此物质不属于 (填“有机物”或“无机物”)
(3)由X、Y两种元素组成的最简单的有机物是 (填化学式),该有机物中X元素的质量分数为 。
(4)由Y、Z两种元素组成的能用于人工降雨的固体物质是 。
(5)由Z、M 两种元素按原子个数比1︰1组成的化合物,俗称 ,写出它与水反应的化学方程式 。
【2015年广东省】某化肥说明书的一部分如题图。

(1)此包化肥中含氮的质量为 kg。
(2)该化肥的化学性质为:
与碱性物质混用会因放出 气而损失肥效;
‚ ,
(3)该化肥的物理性质为 。
【2015年湖南省株洲市】请用所学的知识回答下列问题:
(1)pH<5.6的降雨称为酸雨。为什么把标准定为5.6?
(2)华雪同学用锌粒与稀硫酸在如图所示的装置中制取氢气,一段时间后不再有气泡产生。在解释“不再有气泡产生”的原因时,华雪同学认为可能是锌粒与稀硫酸脱离了接触,你认为还可能有什么原因?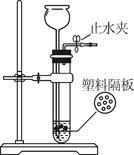
【2015年浙江省衡州市】兴趣小组的同学探究一瓶敞口放置的NaOH溶液(原质量分数为10%)是否变质,进行了下述实验:
| 同学 |
小柯 |
小江 |
小龙 |
| 操作 |
各取一支相同规格的试管,在试管中加入一定量的待测溶液 |
||
| 滴入无色酚酞 |
加入足量的 ? |
加入足量的BaCl2溶液 |
|
| 现象 |
变红 |
产生气泡 |
产生白色沉淀 |
| 结论 |
没变质 |
变质 |
变质 |
(1)小江加入的“?”是 。
(2)小江认为小柯的实验和结论不正确,理由是 。
(3)小龙将沉淀过滤、洗涤、干燥,称量质量为1.97g。已知小龙所取的待测溶液质量为10g,请根据化学方程式计算,该待测溶液中变质生成物的质量分数。
自然界的水都是含有多种物质的混合物,生产、生活中需要的纯净水可以通过蒸馏得到。
(1)将刚刚蒸馏出来的蒸馏水盛放在敞口的干净容器里,一段时间后,蒸馏水的pH将发生怎样的变化?
请你分析说明引起蒸馏水pH改变的原因。
(2)在电解水的实验中,为了增加水的导电性,常在水中加入一定量的稀硫酸。某次实验时,在一定量的蒸馏水中加入50克16%的稀硫酸进行电解,结束后测得剩余溶液的质量为100克,则剩余溶液中溶质的质量分数为多少?
【2015年江苏省苏州市】二氧化硫是一种无色具有刺激性气味的气体,它进入大气后可形成硫酸型酸雨。
(1)煤、石油、木柴中都含有硫元素,点燃后均会产生二氧化硫气体,可用 溶液检验该气体的存在。
(2)为减少大气污染,火力发电厂采用以下两种方法吸收废气中的二氧化硫。
①用氨水吸收废气中的二氧化硫,其反应原理可用化学方程式表示为 。已知:亚硫酸盐不稳定,易被空气中的氧气氧化成硫酸盐。
②用石灰石浆吸收废气中的二氧化硫,其反应原理是:
2CaCO3+O2+2SO2 2CaSO4+2CO2 。若1000kg废气中含有1.6kg的二氧化硫,则至少需要含90%碳酸钙的石灰石多少千克才能将其完全吸收(写出解题过程,计算结果保留一位小数)?
2CaSO4+2CO2 。若1000kg废气中含有1.6kg的二氧化硫,则至少需要含90%碳酸钙的石灰石多少千克才能将其完全吸收(写出解题过程,计算结果保留一位小数)?
【2015年江苏省扬州市】在人类生活﹑生产活动中处处离不开溶液和能源。
(1)下列物质加入水中,能形成溶液的是 。(填序号)
a.泥土 b.食用油 c.碳酸钠
(2)下列物质溶于水,能使溶液温度降低的是 。(填序号)
a.硝酸铵 b.氢氧化钠 c.浓硫酸
(3)人误食重金属中毒后,为了减轻毒性,最好服用下列物质中的 。(填序号)
a.蛋清 b.乙酸铅溶液 c.水
(4)电解水时加入少量NaOH 能增强导电性,是因为其溶于水能自由移动的
和 (填离子符号),与电源电极相连的电极上产生的气体是 。
(5)0.9%的生理盐水中质量分数最大的元素是 。
(6)工业生产中要大量消耗大量的煤﹑石油和 等化石燃料,其中煤是成分复杂的固态混合物,含有的主要元素是 。
【2015年山东省济南市】构建安全体系,建设小康社会,关系国计民生。近期,媒体报道的某些环境问题、卫生问题和安全问题引发了人们的关注:
(1)据报道:“济南俩月查处了13家‘铝包子’铺”,所谓‘铝包子’是指所用面粉中非法加入了含有硫酸铝铵[NH4Al(SO4)2.12H2O]成分的泡打粉,食物中铝元素超标,危害身体健康。在硫酸铝铵中,所含非金属元索共有__________种。
(2)露天烧烤不仅污染环境、导致周边空气中PM2.5指数严重超标,在烧烤的肉类食物中还含有强致癌物质一一苯并 (a) 芘(化学式为C2OH12),在苯并 (a) 芘中,氢元素与碳元素的原子个数之比为_________(填最筒整数比)。
(3)据报道:2015年5月6日在104国道某段,一辆载有20多吨浓硫酸的罐车不慎侧翻,造成大量硫酸泄漏。有关部门调来大量熟石灰粉[主要成分为Ca(OH)2]和沙土用于清除泄漏的硫酸。试写出硫酸和熟石灰反应的化学方程式:______________________________。
(4)世界卫生组织将5月3 1日定为“世界无烟日”,我国采取了公共场所禁止吸烟等控烟措施。吸烟有害健康,我国遭受二手烟危害的非吸烟人口就多达7.4亿。烟雾中主要含有一氧化碳、尼古丁(C10H14N2)和焦油,这三种物质被称为香烟的三大杀手。下列有关说法中,正确的是_________(填写序号A、B、C、D之一)
①生活中应拒绝毒品 ②焦油能诱发细胞病变 ③吸烟对他人无害
④“煤气”中毒是由一氧化碳引起的 ⑤在尼古丁中氮元素的含量最高
A.①④⑤ B.①②③ C.①②④ D.②③⑤
某地规定工业排放的废气中S0 2的含量不得超过0.4mg/L。某兴趣小组利用以下反应:S0 2+I 2+2H 20=H 2S0 4+2HI,测定某工业废气中S0 2的含量,测试装置如图所示。

测试步骤:
①碘溶液的配制:准确称取l.27g碘单质,加入少量碘化钾,先溶解在100mL水中,继续加水配制成l000mL溶液。
②取5mL上述溶液,加入试管中,滴入2~3滴淀粉试液。
③把l00mL注射器的活塞推到底后,插入试管的橡皮塞中,如图所示。
然后缓缓向外拉,使吸入试管内的废气与淀粉碘溶液充分接触。每次抽取的气体为l00mL,重复抽取n次,直到溶液的颜色变为无色(废气中的其它成分不与淀粉碘溶液反应)。
(1)排放到空气中的S0 2气体主要来自于 燃烧。
(2)步骤②中,5mL溶液中溶有碘单质 mg,滴入淀粉试液后,溶液变为 色。
(3)按步骤测试某工业废气,抽取次数为80次后,溶液刚好变为无色。试计算该废气中S0 2含量,并判断是否符合排放标准。
根据下列装置图,回答有关问题:
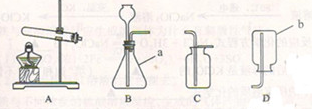
(1)写出装置图中标号仪器的名称:a____________;b____________。
(2)写出实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式:__________________________。可选用的收集装置是________(填字母)。
(3)写出实验室用石灰石和稀盐酸反应制取二氧化碳的化学方程式_________________________。可选用的发生装置是________(填字母)。
(4)实验室将A装置加以改动,在高温下使碳酸钙分解生成氧化钙和二氧化碳。按此反应,试计算工业上要制取5.6t氧化钙,理论上需要含碳酸钙80%的石灰石的质量是多少?(写出计算过程)
【2015年重庆市B】(学习化学后,我们学会了从微观角度认识物质。
(1)已知碳原子和氧原子的结构示意图分别为: 两种原子中相等的是 (填序号)。
两种原子中相等的是 (填序号)。
| A.质子数 | B.电子数 | C.第一层电子数 | D.第二层电子数 |
(2)保持一氧化碳化学性质的粒子名称是 。
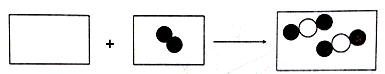
(3)下图是一氧化碳与氧气反应的微观模型图,请在下图方框中以图示的方式完成该化学反应的微观过程(图中 表示氧原子,Ο表示碳原子)。
表示氧原子,Ο表示碳原子)。