某化学小组初步探究"氢氧化钠溶液与盐酸发生中和反应时溶液温度的变化情况".
实验用品:37%的浓盐酸(密度为
)、10%的氢氧化钠溶液、蒸馏水、量筒、温度计
实验一:配制100
10%的盐酸(密度为
)
实验步骤
(1)计算:需要37%的浓盐酸的体积为
(精确到0.01
,下同);需要蒸馏水的体积为
(水的密度为
)
(2)量取浓盐酸和蒸馏水。
(3)混合配制。
实验二:在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸(室温下),反应中溶液温度的变化如下:

(1)表中
的值为.
(2)试绘出溶液温度变化与加入盐酸体积之间的关系图.
(3)根据所绘曲线分析,加入盐酸的体积在0~10
时,溶液温度变化的趋势及其原因是。
(4)其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线的分析,大胆猜想新曲线最高点的位置(不考虑溶液密度和比热容的变化及热量散失等影响因素)。
横坐标及猜想理由:;
纵坐标及猜想理由:。

某化学小组初步设计了"收集不同体积比例的二氧化碳和一氧化碳混合气体"的实验方案。
方案一:如图1所示
(1)请写出硬质玻璃管中发生反应的化学方程式:。
(2)该实验能获得二氧化碳和一氧化碳混合气体,其原因是。
方案二:如图2所示
请写出该气体与炭粉发生反应的化学方程式:.
方案三:如图3所示

(提示:饱和
溶液的作用是除去
气体,部分夹持装置及导管已略去)
请回答下列问题:
(1)写出装置A中发生反应的化学方程式:。
(2)
气体应由(填"a"或"b")通入。
(3)写出装置C中浓硫酸的两点主要作用:
① ;
②。
如图是实验室制取气体的常用装置,请回答下列问题:

(1)写出图中标号仪器的名称:①;②.
(2)实验室可加热
和
的固体混合物制取氧气,请写出该反应的化学方程式:,应选择的气体发生装置是(填字母,下同).若用向上排空气法收集氧气,验满的方法是:将放在集气瓶口,若复燃,则证明氧气已满.
(3)实验室可用
粒和稀硫酸制取氢气,请写出该反应的化学方程式:,应选择的气体发生装置是.
(4)常温下,乙烯(
)是一种无色气体,密度与空气相近,难溶于水,不与空气和水发生反应.实验室收集乙烯时,应选择的装置是.
下图是两种物质的溶解度曲线,下列说法正确的是( )

| A. | 甲的溶解度大于乙的溶解度 |
| B. | ℃时等质量甲、乙两种物质的饱和溶液中溶质质量相等 |
| C. | ℃时等质量的甲、乙两物质的饱和溶液降温至 ℃时,两溶液中溶质质量分数相等 |
| D. | 氧气的溶解度随温度变化的规律与图中乙相似 |
实验室有一瓶无色溶液,老师告诉同学们该溶液可能是
溶液、
溶液、
溶液中的一种,请你和同学们一起来参与探究,并回答问题:
(1)取少量该溶液于试管中,滴加酚酞试液,溶液变红色,则原溶液不可能是溶液;
(2)另取少量该溶液于试管中,滴加
溶液,产生(填实验现象),则该溶液为
溶液,其反应的化学方程式为。
某白色固体由
、
、
、
中的三种组成,取样后加入足量的水,充分搅拌后,有白色沉淀生成,则原固体混合物的组成可能有(填序号)
①
、
、
②
、
、
③
、
、
④
、
、
如图是
、
、
三种固体物质的溶解度曲线图,请回答:

(1)
、
、
三种物质的溶解度受温度影响最大的是;
(2)t1℃时
的溶解度(填">"、"<"或"=")
的溶解度;
(3)在t2℃时,将15g
物质加入到50g水中,充分搅拌后,所得溶液中溶质的质量分数为。
化学物质王国中举行节日游戏活动,游戏规则如图所示(图中"→"表示一步反应生成),以形成物质间相互转化的循环接龙.
请你将下列八位队员:①
②
③
④
⑤
⑥
⑦
⑧
平均分成红、蓝两队。游戏规定,物质⑤任红队的队长,物质⑦任蓝队的队长,且红、蓝两队的队长均处于甲的位置,两队分别形成循环接龙。
请回答:

(1)红队乙的化学式.
(2)红队中丙→丁的化学方程式为.
(3)蓝队队员依甲乙丙丁的顺序排列是⑦(填序号)
柠檬酸亚铁(
)是一种易吸收的高效铁制剂,可由硫酸亚铁通过下列反应制取。

请回答下列问题:
(1)柠檬酸亚铁中铁元素的化合价为 ;
(2)写出反应②的化学方程式;
小明测得石灰石与一定量的稀盐酸反应后的溶液PH为2,也适量该溶液向其中逐滴加入碳酸钠溶液,并测得溶液PH随加入碳酸钠溶液体积的变化曲线如下图所示。
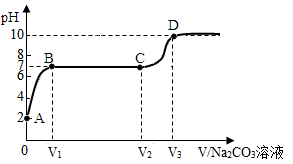
请回答下列问题:
(1)A点处溶液中的两种溶质是(写化学式);
(2)AB段可观察到的实验现象是 ;
(3)BC段发生反应的化学方程式是 ;
(4)CD段PH上升的原因是;
如图,初中化学中,我们学习了酸和碱发生中和反应的实质是
。像这种实际参加反应的离子符号来表示反应的式子叫离子方程式.离子方程式的书写一般按以下步骤:(以
与
反应为例)

①写出反应的化学方程式:
②把易溶于水、易电解的物质写出离子形式,把难溶的物质、气体和水等仍用化学式表示.上述方程式可改写成:
③删去方程式两边不参加反应的离子:
④检查方程式两边各元素的原子个数和电荷总数是否相等.
请回答:
(1)下列各组中的离子,能在溶液中大量共存的是()
| A. | B. | ||
| C. | D. |
(2)写出稀盐酸滴在石灰石上所发生反应的离子方程式。
(3)写出一个与离子方程式
相对应的化学方程式。
(4)酸、碱、盐在水溶液中发生的复分解反应实质上就是两种化合物在溶液中相互交换离子的反应,只要具备生成物中有气体或沉淀或生成,反应就能发生。
如图是实验室制取气体的常用装置,请回答下列问题:

(1)写出带有标号的仪器名称①②。
(2)写出一个实验室制取氧气的化学方程式,用该方法制取氧气所选择的发生装置是。若用排水法收集氧气,判断气瓶内氧气已收集满的依据是。
(3)实验室制取二氧化碳,可选择发生装置为.若要收集一瓶纯净、干燥的二氧化碳气体,请按照气流从左到右的方向,用仪器接口字母表示连接顺序.发生装置端口→
(4)检验二氧化碳气体的方法是。(用化学方程式表示)
某化学兴趣小组同学利用图中所示装置模拟炼铁:

(1)为了避免玻璃管
在加热时可能发生爆炸,加热前应。
(2)
管中氧化铁发生反应的化学方程式为。
(3)
装置可用来吸收二氧化碳气体,写出该反应的化学方程式;
装置(填"能"或"不能")用来收集
。
(4)若
管中氧化铁全部还原成铁,冷却后称量铁的质量比反应前氧化铁的质量减少了2.4
,则加入
管中氧化铁的质量是
。
如图是氯化钠和硫酸钠的溶解度曲线,看图后回答问题:

(1)的溶解度收温度影响变化不大。
(2)温度不变时,若将氯化钠的不饱和溶液变为饱和溶液可采取的方法是。(填一种即可)
(3)40℃时,将30
硫酸钠固体加入到50
水中充分溶解,所得溶液的质量是。
(4)用降温结晶的方法提纯含少量杂质氯化钠的硫酸钠,最佳的温度范围是℃以下,理由是。
化学实验题
(1)仪器B的名称是 。
(2)写出用KClO3与MnO2的混合固体制取O2的化学方程式 ,需用到的仪器是 (写字母,可多选),那么除此之外还需要用到的仪器是 。
(3)实验室制取CO2的化学方程式是 。
(3)实验室常用块状固体电石(主要成分是CaC2)与水反应制取乙炔,该反应剧烈,速度较快,为了节约化学药品,则应选择的发生装置是 (填字母),通常情况下乙炔(C2H2)是一种无色、无味、密度比空气略小,难溶于水的气体,若要收集较纯净的乙炔气体,则应将气体从 (填a、b、c、或d)通入.
(5)将CO2和O2通入图L进行分离,最终得到的气体是
| A.CO2、O2 | B.CO2 | C.O2 | D.O2、H2O |
甲、乙两种固体物质的溶解度曲线如图所示.

(1)
时甲物质的溶解度是
;乙物质的溶解度随着温度的升高而(填"增大"或"减小");
(2)
时甲物质的饱和溶液中溶质的质量分数为;将
时甲、乙两种物质的饱和溶液分别降温至
,溶液中溶质质量分数大小关系是:甲(填"<"、"="或">")乙.