金属材料广泛应用于生产、生活中。
(1)下列物品所用的主要材料中,属于金属材料的是 。
A.塑料水杯
B.汽车轮胎
C.青铜古剑
D.医用口罩
(2)用盐酸可除去铁表面的铁锈,反应的化学方程式是 。
(3)不法分子常用铜锌合金制成假金币行骗。能有效鉴别“金币”真假的一种方法是:将“金币”浸入稀硫酸中,产生气泡的是假金币。原理是 (用化学方程式表示)。
通过近一年的学习,同学们一定深刻感受到化学就在身边,人类的衣、食、住、行都离不开化学,它使我们的生活变得更加绚丽多彩。请回答下列问题:
(1)你身上的衣服牢固耐穿、易洗快干、抗皱性好,是因为衣料大多都由 (填“合成纤维”或“天然纤维”)制成。
(2)自2018年以来,宁夏多地区启动深度净化黄河水替换地下水源供水,保障城乡居民饮水安全。黄河水自取水站经过沉淀、过滤、吸附、杀菌消毒,达到国家生活饮用水标准后,输送至千家万户。小刚通过 ,判断自来水仍然是硬水。饮用前,可 将其软化。
(3)你住的房屋建造时所用的各种材料也和化学有关。例如,用石灰浆粉刷过的墙壁,一段时间后,变得既白又坚固,其原理是 (用化学方程式表示)。
(4)“共享电动车”方便市民绿色出行,有效缓解了城市交通压力,减少了大气污染,成为现代城市的又一道靓丽“风景”。为防止电动车钢制车架与空气中的 等接触而生锈,通常在车架表面进行喷漆处理。
化学实验是进行科学探究的重要方式。
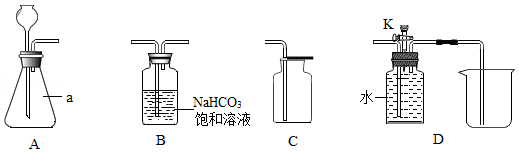
(说明:NaHCO 3饱和溶液的作用是吸收氯化氢气体;装置气密性良好;其他连接装置略)
实验一 氧气的实验室制取
(1)写出图中标号a仪器的名称: 。
(2)用A、C装置制取氧气,所需药品是 。
实验二:制取较纯净的CO 2并探究其性质
[药品准备]将30g质量分数为36%的浓盐酸稀释为9%的稀盐酸
(3)计算加入水的体积为 mL.(水的密度为1.0g/cm 3)
(4)配制稀盐酸时所需仪器有 (填序号)。
①量筒 ②玻璃棒 ③蒸发皿 ④胶头滴管 ⑤烧杯 ⑥托盘天平
[操作步骤]
步骤一:在A装置中加入足量石灰石,依次连接A、B、C装置,再向A中加入适量的稀盐酸。一段时间后,经检验A、B装置内的空气已排净。写出A中发生反应的化学方程式: 。
步骤二:待A中反应停止后,拆下C装置,再将D装置与A、B连接,关闭活塞K, (补全实验步骤),在D中收集实验所需的较纯净的CO 2。
步骤三:打开活塞K,用一支50mL注射器从D中缓慢抽取20mL CO 2,关闭K,再抽取20mL滴有紫色石蕊溶液的水溶液,用橡皮塞堵住注射器的针孔,轻轻振荡。观察到的现象: 。
[问题交流]步骤一中能充分证明A、B装置内的空气已排净的可靠方法是 。
[后续探究]……
实验室制取气体常用如图装置,请根据如图回答问题。
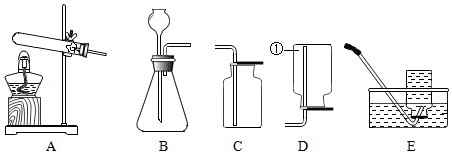
(1)写出图中标号仪器的名称:① 。
(2)实验室制取氢气的化学方程式为 ,若实验室用装置B制氢气,长颈漏斗的下端管口伸入液面下是为了防止 ,氢气的收集装置可选用 。氢气是一种高能燃料,点燃氢气前需要 。
(3)实验室将装置A和C组合,可制取的气体是 。
根据下列实验装置图,回答有关问题。
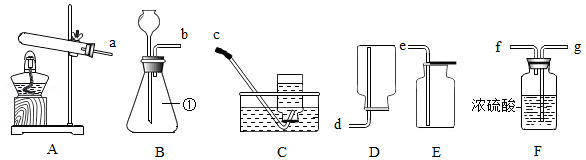
(1)图中标有①的仪器名称为 。
(2)实验室用加热熟石灰与氯化铵固体的方法可以制取氨气,其发生装置选用 。(填大写字母)
(3)实验室用锌粒和稀硫酸制取H2的发生装置选用 (填大写字母),反应的化学方程式为 。
(4)实验室用双氧水和二氧化锰制取一瓶干燥的氧气,所选仪器的接口连接顺字是 (填导管接口的小写字母)。
气体制备、收集是初中化学的重要知识。请结合如图回答有关问题。

(1)写出图中仪器a的名称: 。
(2)实验室用氯酸钾和二氧化锰制取氧气,应选择的发生装置为 (填字母),写出该反应的化学方程式: 。
(3)用装置C代替装置B制取二氧化碳的优点是 ;用D装置收集二氧化碳,则气体应从 (填"①"或"②")端进入。

(4)用质软的塑料瓶收集满两瓶二氧化碳气体。向其中一瓶加入约 体积的水(如图F所示),立即旋紧瓶盖,振荡。观察塑料瓶最终的现象: ;用注射器向另一瓶(瓶口用橡胶塞塞紧)气体中注入约 体积的水(如图G所示),振荡。观察塑料瓶最终的现象: ,产生该现象的原因: 。
金属材料对于促进生产发展、改善人类生活发挥了重大作用。
(1)铝具有很好的抗腐蚀性能,原因是 。
(2)一氧化碳的还原性可用于冶金工业,写出一氧化碳和氧化铜反应的化学方程式 。
(3)向含有硫酸铜和硫酸锌的混合溶液中,加入过量的铁粉,充分反应后过滤,得到滤液和滤渣,滤渣中含有的物质是 。
(4)下列保护金属资源的做法不正确的是 (填字母序号)。
A.任意开采矿物
B.回收利用废旧金属
C.铁制品存放在潮湿的环境中
D.用塑料代替金属材料制造管道
如图2为某钙片的商品标签,为测定钙片中钙元素的质量分数(假设钙片中其他物质不含钙元素,且不溶于水,也不与任何物质发生反应),某化学兴趣小组取20片钙片,进行如下实验:

(1)上述实验过程中发生反应的化学方程式为 。
(2)根据已知条件列出求解所加的稀盐酸中溶质质量(x)的比例式 。
(3)用36.5%的浓盐酸配制100g上述稀盐酸,所需浓盐酸的质量为 。
(4)钙片中钙元素的质量分数为 。
(5)若向滤液中加入5.4g水,所得溶液中溶质的质量分数为 。
(6)工厂生产钙片时若需碳酸钙120t,理论上需含氧化钙84%的生石灰的质量为 。
随着手机、电脑等移动设备的普及,人们对充电设备的要求越来越高。最近,某品牌氮化镓充电设备以体积小、功率大深受消费者喜爱。
(1)氮化镓(GaN)是充电设备中的核心材料。查阅资料得知:氮化镓中氮元素的化合价与氨气(NH3)中氮元素的化合价相同。由此可知,氮化镓中镓元素的化合价为 。
(2)氮化镓的制取可通过镓与氨气在高温下发生置换反应来实现,其反应的化学方程式为 。
金属材料的应用推动了社会的发展。新型材料的研制,已成为现代高新技术的重要物质基础。
(1)目前常用的1元硬币为钢芯镀镍合金,具有耐腐蚀、 等优点。
(2)镁和铝可熔炼成Mg17Al12镁合金,熔炼过程只能在真空中,不能在空气中进行的原因是 (写其中一个化学方程式)。
(3)某废弃物中可能含有Cu、CuO、Mg、Zn中的一种或几种,为确定其成分并回收金属,取样品进行如图实验。

①步骤Ⅱ的操作是 。
②步骤Ⅱ中产生的现象是 。步骤Ⅲ中锌和稀硫酸反应的化学方程式为 。
③若溶液C中只含一种溶质,则样品的成分是 。
④通过测氢气的质量,也可确定样品的成分,则w的值为 (用m和n的代数式表示)。
根据如图回答问题。

(1)反应原理
①加热高锰酸钾、分解过氧化氢溶液或加热氯酸钾均可产生氧气,其中分解过氧化氢溶液和加热氯酸钾时,加入二氧化锰在反应中起的作用是 。三种方法中,写出其中一个反应的化学方程式 。
②石灰石和稀盐酸反应产生二氧化碳的化学方程式为 。
(2)制取O 2和CO 2.连接如图的装置完成实验。
| 制取气体 |
A |
B |
C |
|
|
| 反应物 |
装置(填"甲"或"乙") |
物质 |
作用 |
作用 |
|
| O 2 |
① |
② |
水 |
③ |
接水 |
| CO 2 |
石灰石和稀盐酸 |
乙 |
④ |
干燥CO 2 |
⑤ |
| |
|
|
|
|
|
阅读下面科普短文
2020年3月8日,面对口罩核心材料熔喷布的需求井喷,国务院国资委指导推动相关中央企业加快生产线建设,为新冠肺炎疫情防控提供保障。
熔喷布主要以聚丙烯[(C3H6)n]为原料,纤维直径可以达到1~5微米,具有独特的毛细结构超细纤维,从而使熔喷布具有很好的过滤性、屏蔽性、绝热性和吸油性,是良好的口罩材料。
聚丙烯是丙烯(C3H6)的聚合物。全球丙烯的工业化生产工艺主要有裂解法、催化裂化法(FCC),甲醇制烯烃(MTO/MTP)、丙烷脱氢(PDH)和烯烃歧化法等,我国和全球丙烯的工业化生产工艺方法及份额分别如图1、图2所示:

中国丙烯产能扩张速度稳定,未来产能增量以PDH为主,因PDH的主要成本来自于原料丙烷,丙烷价格越低廉,项目盈利越可观。因此丙烯作为化工领域中重要的基础原料产品,合理布局及发展烯烃产业结构尤为重要。
依据文章内容,回答下列问题:
(1)口罩的核心材料熔喷布主要以 为原料,它是有机合成材料,而日常生活中用得最多的有机合成材料是塑料、 、合成橡胶。
(2)熔喷布是良好的口罩材料,是因为它具有很好的 、 等优点(任写两点)。
(3)写出丙烯完全燃烧的化学方程式 。
(4)一定条件下,丙烷气体(C3H8)分解可以制得丙烯气体,写出该反应的化学方程式 。
(5)我国生产丙烯份额最多的方法是 ;由图2可知2015﹣2025年,全球各地区采用裂解和FCC生产丙烯份颜均有下降趋势,而 工艺法所产丙烯份额有逐步上升趋势。
利用下列装置进行气体的制取实验,请问答下列问题:
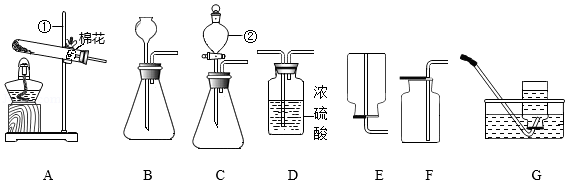
(1)写出仪器的名称:① ② 。
(2)实验室用过氧化氢溶液制取氧气时,若要制取一瓶干燥的氧气,必须使气体通过 (填字母,下同)装置,选用装置 收集,验满的方法是 。
(3)实验室用加热高锰酸钾固体的方法制取较纯净的氧气,选用发生装置 和收集装置G组合,检查该装置气密性的方法是:连接好仪器,把导管的一端浸入水中, ,证明装置连接完好、不漏气。
(4)实验室用电石固体与饱和食盐水常温下反应制取乙炔(C2H2)气体,同时有糊状 Ca(OH)2生成,发生装置选用C而不选用B的原因是 ;乙炔充分燃烧的化学方程式为 。
随着手机、电脑等移动设备的普及,人们对充电设备的要求越来越高。最近,某品牌氮化镓充电设备以体积小、功率大深受消费者喜爱。
(1)氮化镓(GaN)是充电设备中的核心材料。查阅资料得知:氮化镓中氮元素的化合价与氨气(NH3)中氮元素的化合价相同。由此可知,氮化镓中镓元素的化合价为 。
(2)氮化镓的制取可通过镓与氨气在高温下发生置换反应来实现,其反应的化学方程式为 。