材料是人类赖以生存和发展的重要物质,目前使用量最多的金属材料仍然是钢铁

(一)铁材料的有关知识
1.人类使用金属先后经历了"青铜"、"铁器"时代,直到近代才开始大量使用铝材料.
这也反映出Cu、Fe、Al三种金属的活动性由强到弱的顺序是 .
2.钢铁材料通常分为生铁和钢.如图1是我国1997年发行的纪念钢产量首次突破1亿吨的邮票.邮票通常密封保存在聚乙烯塑料袋中
①以上叙述中不涉及到的材料是 (选填序号).
A.合金 B.无机非金属材料 C.有机合成材料
②以赤铁矿为原料冶炼铁反应的化学方程式
③钢铁露置在空气中易生锈,请提出防止其生锈的一种措施 .
(二)铁及其化合物的实验
1.将Fe粉溶于稀H 2SO 4,此反应属于 (填基本反应类型).用点燃法检验生成的H 2前必须 .
2.向上述反应后的溶液中滴加NaOH溶液,生成白色Fe(OH) 2沉淀,随后沉淀变为灰绿色.
①生成Fe(OH) 2反应的化学方程式 .
②白色沉淀变为灰绿色的原因之一是部分Fe(OH) 2接触空气生成Fe(OH) 3,反应的化学方程式 .生成的Fe(OH) 3分解为Fe 2O 3.
③过滤、洗涤、低温干燥得到灰绿色固体,其组成为2FeSO 4•2Fe(OH) 2•Fe 2O 3〔相对分子质量为644].能证明固体已洗净的方法为 .
(三)灰绿色固体的热分解实验
兴趣小组称取此固体6.44g,在科研人员的指导下用如图2装置进行热分解实验.
【查阅资料】
①Fe(OH) 2在150℃~200℃时完全分解为FeO;
②FeSO 4在450℃~500℃时完全分解为Fe 2O 3,2FeSO 4 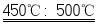 Fe 2O 3+SO 2↑+SO 3↑.
Fe 2O 3+SO 2↑+SO 3↑.
1.加热前后及过程中均通入N 2,加热前通N 2的目的是 .
2.控制温度在不同的范围对A中样品加热,测得剩余固体质量随温度的变化如图3所示.B装置中浓硫酸只能吸收SO 3和H 2O,当加热到t 1℃时,装置C中的现象为 .
①图3中E点对应的m 1= .
②图3中F点对应物质中Fe 2O 3的质量为 g.
③科研人员将F点所得剩余固体隔绝空气,在密闭容器中加热到1400℃,得到纯净的磁性Fe 3O 4.已知加热过程中发生两个反应,且反应前后固体总质量不变.请写出其中一个反应的化学方程式 .
绿矾(FeSO4•7H2O)是硫酸法生产太白粉的主要副产物,可用于制备Fe2O3,复印用Fe3O4粉、还原铁粉等,开发利用绿矾工艺是一项十分有意义的工作。某研究性小组展开了系列研究。
Ⅰ制备Fe2O3
【资料一】
(1)无水硫酸铜遇水变成蓝色的硫酸铜晶体。
(2)绿矾(FeSO4•7H2O)高温分解产生一种金属氧化物和几种气态非金属氧化物。
(3)SO2是无色有窒息性臭味的有毒气体,能使品红溶液褪色。
甲同学用如下装置制备Fe2O3并验证绿矾受热分解的其他产物;

实验过程中发现:A中有 色固体生成,B中无水硫酸铜变蓝,C中U形管内有无色晶体(SO3)析出,D中品红溶液褪色,装置E的作用是 ,绿矾高温分解的化学方程式为 。
Ⅱ制备Fe3O4
乙同学模拟生产复印用Fe3O4粉的实验流程如下:

【资料二】Fe(OH)2是一种白色难溶于水的固体,在空气中易被氧化。
FeSO4溶液中加入NaOH溶液,反应的化学方程式依次为① ,②4Fe(OH)2+O2+2H2O═4Fe(OH)3.由沉淀a获得Fe3O4的化学方程式为:Fe(OH)2+2Fe(OH)3═Fe3O4+4H2O
若制取Fe(OH)2,采取的实验操作是:向盛有5mL新制FeSO4溶液的试管中加入10滴植物油,然后用胶头滴管加煮沸的NaOH溶液(驱赶O2),胶头滴管的正确使用方法是 (填字母)。

Ⅲ制备还原铁粉
制备还原铁粉的工业流程如下:

(1)操作1的名称是 ,NH4HCO3和FeSO4溶液反应的化学方程式为 。
(2)若将14.06g粗还原铁粉(假设粗还原铁粉中杂质仅含少量FexC)在氧气流中完全反应,得到0.22gCO2,将相同质量的粗还原铁粉与足量稀硫酸反应,得到0.48gH2(FexC与稀硫酸反应不产生H2)。试通过计算确定FexC的化学式(请写出计算过程) 。
(3)粗还原铁粉经加工处理后变成纯还原铁粉,纯还原铁粉和水蒸气在高温条件下也可制得四氧化三铁,同时生成一种气体。其装置如图所示:

SAP材料吸水性强,湿润的SAP材料能为该反应持续提供水蒸气。实验开始一段时间后,观察到在肥皂液中有大量的气泡产生,此气泡用火柴即能点燃,同时有肥皂泡飘到空中。生成的气体是 ,干燥的SAP材料作用是 。
某同学取用生石灰时,发现装满生石灰的塑料试剂瓶已经膨胀破裂,如图:
(1)塑料试剂瓶膨胀破裂的原因是 ,反应的化学方程式为 .
(2)破裂后瓶内试剂会吸收空气中CO2生成CaCO3.为测定其中CaCO3的质量分数,兴取小组分别进行如下实验:
实验1:称取10.0g样品,加50.0g水溶解,搅拌、静置、过滤,将沉淀洗涤、干燥、称重.
实验2:称取10.0g样品,向其中加入足量稀盐酸,充分反应,收集产生的气体.
①根据实验1称重计算样品中CaCO3的质量分数可能偏高,原因是 .
②若实验2中收集的气体为2.2g,计算样品中CaCO3的质量分数.(请写出计算过程)

我国拥有地球上7%的耕地,但化肥使用量却占全球总量的35%,认识化肥,科学施肥至关重要。
(1)下列物质中,可用作磷肥的是 :
A.K 2SO 4 B.CO(NH 2) 2 C.KNO 3 D.Ca(H 2PO 4) 2
(2)NH 4Cl是常见的氮肥,不能与碱性物质混用,否则会因释放出 而损失肥效;
(3)过度使用化肥造成的后果有:① ;②水体富营养化等;
(4)"雷雨发庄稼"现象涉及的化学反应较为复杂,其中一个反应是NO 2与H 2O反应生成HNO 3和NO,写出该反应的化学方程式: ;该反应中。化合价发生改变的元素是_ (填元素符号)。
某实验小组在做“用澄清石灰水检验二氧化碳”的实验时,发现一个有趣的实验现象:

试管中浑浊现象为何消失?实验小组的同学对此实验进行了下列探究活动:
(1)根据已学知识,实验小组对CO2使澄清石灰水变浑浊的现象作出了合理的解释,其化学方程式为 。
(2)【查阅资料】
①碳酸盐一般不溶于水,如碳酸钙不溶于水。
②碳酸钙能与二氧化碳、水反应生成碳酸氢钙[Ca(HCO3)2],碳酸氢钙易溶于水。
③碳酸氢钙受热易分解,生成碳酸钙、二氧化碳、水。
从物质组成角度分类,碳酸氢钙应属于 。
A.氧化物 B.酸 C.碱 D.盐
写出碳酸氢钙受热分解的化学方程式 。
【提出问题】碳酸氢钙能与哪些物质反应呢?
【假设与猜想】猜想I:能与盐酸反应
猜想∐:能与氢氧化钠反应
……………
(3)【设计实验并验证】
实验步骤 |
实验现象 |
结论 |
实验一:取丙中少量液体于试管中,滴加稀盐酸 |
有 生成 |
猜想I成立 |
实验二:取丙中少量液体于试管中,滴加氢氧化钠溶液 |
有白色沉淀生成 |
猜想II成立 |
实验三:取丙中少量液体于试管中,加热 |
澄清液体又变浑浊 |
验证了资料描述 |
根据验证实验写出碳酸氢钙与盐酸反应的化学方程式 。
【讨论与反思】
该实验小组在实验中发现问题,并对问题进行不断探究。他们不但发现了新的物质,还了解了它的一些性质,并对生活中煮沸可以降低水的硬度、水垢的形成以及自然界中溶洞与钟乳石的形成有了更进一步的认识。
某项目学习小组进行了如下探究。
【查阅资料】
电导率越大,溶液导电性越强,离子浓度越大。
鸡蛋壳主要成分是CaCO3,其它成分对实验影响忽略不计。
鸡蛋壳与牙齿和含氟牙膏反应的化学原理相似。
【实验一】鸡蛋沉浮
将一个新鲜的鸡蛋放在盛有足量稀盐酸的烧杯中,可观察到鸡蛋一边冒气泡一边沉到底,一会儿又慢慢上浮,到接近液面时又下沉。
(1)冒气泡的原因 (化学方程式表示)。
(2)接近液面时又下沉的原因 。
【实验二】鸡蛋壳溶解
在烧杯中加入蒸馏水,插入电导率传感器,加入蛋壳粉,搅拌,测得电导率随时间的变化如图1。

(3)搅拌的目的是 。
(4)图1中,a﹣b段电导率变化的原因 。b﹣c段电导率基本不变的原因 。
【实验三】鸡蛋壳代替牙齿探究含氟牙膏能否预防龋齿
(5)查资料知,含氟牙膏(含氟成分为NaF)与蛋壳反应在表面生成氟化钙保护层。反应的化学方程式为 。
(6)先检查图2装置气密性,方法是 。再称取0.50g“牙膏处理过的蛋壳(用牙膏浆液浸泡、洗涤、晾干)”于锥形瓶中,用注射器抽取20mL3.5%的盐酸(模拟形成龋齿的酸环境),连接好装置,打开开关,将盐酸快速压人锥形瓶,关闭开关,测得压强随时间的变化如图3所示。用“未用牙膏处理的蛋壳”重复上述实验。

(7)图3中x﹣y段压强增大的主要原因 。
(8)根据实验三的数据分析,含氟牙膏 (填“能”或“不能”)预防龋齿,理由是 。
取4.4g部分被氧化的镁带样品,加入到147g溶质质量分数为10%的H 2SO 4溶液中,镁带和H 2SO 4均恰好完成反应.
(1)写出上述镁带在H 2SO 4溶液中发生反应的化学方程式 .
(2)反应完成后生成MgSO 4的质量为 g.
(3)该镁带样品中MgO的质量为 g.其中未被氧化与已被氧化的镁元素的质量比为 .
(4)若生成的MgSO 4溶液是不饱和溶液,求该溶液的质量为多少(写出计算过程)?
化学兴趣小组的同学在探究碱的化学性质时,完成了如图1所示的两个实验。实验后,小明同学将废液倒入同一废液缸中,发现混合废液浑浊并显红色。请你完成下列问题:
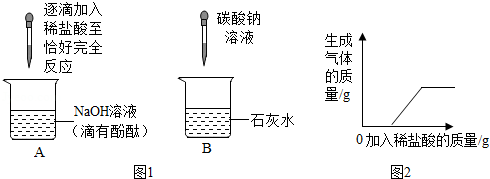
(1)A实验中发生反应的现象为 。
(2)B实验中发生反应的化学方程式是 。
(3)【提出问题】废液中,能使酚酞溶液变红的物质可能是哪些呢?
【作出猜想】猜想一:废液中,能使酚酞溶液变红的物质可能是NaOH;
猜想二:废液中,能使酚酞试液变红的物质还可能是 ;
猜想三:废液中,能使酚酞溶液变红的物质还可能是Ca(OH)2。
【实验验证】同学们对可能含有的碱性物质进行确定,取一定量的废液过滤,向滤液中逐滴加入稀盐酸,根据反应现象得到如图2所示的图象。
【结论】分析图象数据得出,废液中使酚酞变红的物质一定是 ,一定不是 。
【拓展提高】为了使以上废液实现安全排放,你的做法是 。
(1)向24.5g氯酸钾中加入少量二氧化锰,加热、充分反应后,生成氯化钾14.9g。则生成氧气的质量是 g,该反应的化学方程式是 。
(2)向盛有一定量硝酸银溶液的试管中加入14.9g氯化钾,恰好完全反应,过滤,得到120.2g滤液,求该硝酸银溶液的质量(写出计算步骤)
(1)向24.5g氯酸钾中加入少量二氧化锰,加热、充分反应后,生成氯化钾14.9g。则生成氧气的质量是 g,该反应的化学方程式是 。
(2)向盛有一定量硝酸银溶液的试管中加入14.9g氯化钾,恰好完全反应,过滤,得到120.2g滤液,求该硝酸银溶液的质量(写出计算步骤)
(1)向24.5g氯酸钾中加入少量二氧化锰,加热、充分反应后,生成氯化钾14.9g。则生成氧气的质量是 g,该反应的化学方程式是 。
(2)向盛有一定量硝酸银溶液的试管中加入14.9g氯化钾,恰好完全反应,过滤,得到120.2g滤液,求该硝酸银溶液的质量(写出计算步骤)
(1)向24.5g氯酸钾中加入少量二氧化锰,加热、充分反应后,生成氯化钾14.9g。则生成氧气的质量是 g,该反应的化学方程式是 。
(2)向盛有一定量硝酸银溶液的试管中加入14.9g氯化钾,恰好完全反应,过滤,得到120.2g滤液,求该硝酸银溶液的质量(写出计算步骤)
铝是重要的轻金属,广泛应用于航空、电讯和建筑领域。铝亦有其特殊的性质,试根据以下信息填空或简答。
(1)按金属的活动性顺序,铝比锌 。但是将铝片和锌粒分别投入稀硫酸中,铝片表面产生的气泡却比锌粒少而慢。为了探究铝与酸反应的规律,小强用相同质量、相同形状的光亮铝片设计如下实验。
实验一 |
实验二 |
实验三 |
实验四 |
|
实验现象 |
铝表面产生气泡很小且慢 |
铝表面产生大量气泡 |
铝表面产生大量气泡 |
铝表面产生大量气泡且快 |
(2)比较实验三、实验四说明铝与酸反应产生氢气的速率,与 有关。
(3)比较实验一、实验二说明铝与酸反应产生氢气的速率,可能与 、 粒子和温度、金属与酸的接触面积等多种因素有关。
(4)写出实验二中发生反应的化学方程式 。
(5)小芳将长条状铝片的一端放在酒精灯火焰上灼烧片刻,轻轻摇动铝条,受热一段会左右摇晃,却不像蜡烛那样滴落。为探究其原因,小芳查阅资料得知:铝的熔、沸点分别是660℃、2460℃;氧化铝的熔、沸点分别为2054℃、2980℃。
试解释上述实验现象: 。